1������� ������ԭ��Ӧ�������������о��й㷺����;���ᴩ�Ž�
��1����������������������з�����������ԭ��Ӧ����?��
��2��ˮ���������Ҫ��ɲ��֣��������к�������һ�����ʡ��������ֻ�����Ӧ������������ԭ��Ӧ�Ĺ�ϵ��Ҳ������ͼ���
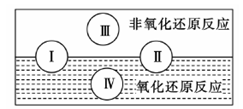
��д����ˮ�μӡ�ˮΪ��ԭ����Ϊ���͢���һ����ѧ����ʽ��?��
��3��NaNO2��һ��ʳƷ���Ӽ��������°�������KMnO4��Һ��NaNO2��Ӧ�����ӷ���ʽ�ǣ�

���벹����������ƽ����ʽ���������ת�Ƶķ������Ŀ��
��ijͬѧ��ȡ��7.9 g KMnO4�����壬������100 mL��Һ���ش��������⣺
��ʵ���У�ʹ������ƿʱҪ����Ƿ�©ˮ���������?��
�۲��淶��ʵ������ᵼ��ʵ�����������в�����ʹʵ����ƫС����?(�����)��
A�����ܽ������������Һ�彦���ձ���
B������ʱ��������ƿ�ϵĿ̶���
C�����ݺ�����ƿ��ҡ�Ⱥ��÷���Һ����ڿ̶��ߣ������ּ�������ˮ���̶���
��ijͬѧ��������õ�KMnO4��Һ�ζ�δ֪Ũ�ȵ�NaNO2��Һ��ȡ20 mLδ֪Ũ�ȵ�NaNO2��Һ����ƿ��ȡ������õ�KMnO4��Һ��________(���ʽ����ʽ��)�ζ��ܣ��ζ���ɺ�����KMnO4��Һ10 mL����NaNO2��Һ��Ũ��Ϊ________________��
�ο��𰸣���1��D?��2�� 2F2 + 2H2O =" 4HF" + O2
��3����? ?��������ƿ�м�������������ˮ������ƿ������ƿ�����Ƿ�©ˮ��������ƿ����ת180�ȣ����µ��ã����Ƿ�©ˮ?��ABC?����ʽ? 0.625mol��L�C1
?��������ƿ�м�������������ˮ������ƿ������ƿ�����Ƿ�©ˮ��������ƿ����ת180�ȣ����µ��ã����Ƿ�©ˮ?��ABC?����ʽ? 0.625mol��L�C1
�����������1��A��B��C���������仯��Dȼ���ǻ�ѧ��Ӧ���Ҷ�����������ԭ��Ӧ����2�����ֻ�����Ӧ����?������������ԭ��Ӧ��ֻ���û���Ӧ��ˮ����ԭ������ֻ����Ԫ�ر���������ϵ������ˮ�ķ�Ӧ��д����ѧ����ʽ��2F2 + 2H2O =" 4HF" + O2����3���ٷ�Ӧ��������Һ�н��У����Է�����Ӧ��дH+��Mn�Ļ��ϼ۽���5(+7��+2)��NԪ�صĻ��ϼ�����2(+3��+5)������MnO4�C��Mn2+����2��NO2�C��NO3�C����5�����ݵ���غ㣬H+��6������ԭ�Ӹ����غ�H2O��3���ڼ������ƿ�Ƿ�©ˮ�ķ���Ϊ��������ƿ�м�������������ˮ������ƿ�������ã���ƿ�����Ƿ�©ˮ��������ƿ����ת180�ȣ����µ��ã����Ƿ�©ˮ����A������Һ�彦���ձ��⣬������ʵ����ʵ�����С��������ҺŨ��ƫС��B������ʱ��������ƿ�ϵĿ̶��ߣ����ˮ������������ҺŨ��ƫС��C�����ּ�������ˮ���̶��ߡ������ˮ�����ӣ���ҺŨ��ƫС����ѡABC�����ữKMnO4��Һ��ǿ�����ԣ���������Ƥ�ܣ����Բ��ü�ʽ�ζ��ܶ�����ʽ�ζ�ʢװKMnO4��Һ�������ӷ���ʽ��֪KMnO4��NaNO2��2:5�����ʵ���֮�ȷ�Ӧ��KMnO4��Ũ��Ϊ��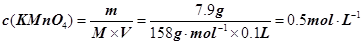 ����NaNO2��Һ��Ũ��Ϊ��
����NaNO2��Һ��Ũ��Ϊ��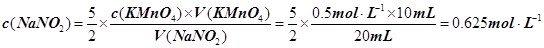 ��
��
�����Ѷȣ�һ��
2��ѡ���� Cl2��70���NaOHˮ��Һ�У���ͬʱ������������������ԭ��Ӧ����Ӧ��ȫ������Һ��NaClO��NaClO3�����ʵ�����Ϊ4��1������Һ��NaCl��NaClO�����ʵ���֮��Ϊ��
A��9��4
B��5��1
C��11��2
D��1��1 ( )
�ο��𰸣�A
�����������
�����Ѷȣ�һ��
3�������� ��128 gͭ����һ������Ũ�����У����ȣ�����ͭ�IJ��ϼ��٣���Ӧ���ɵ�������ɫ��dz����ͭ��Ӧ���ʱ��ͭƬ��ȫ��ʧ�������ռ���NO2��NO�Ļ������44.8 L���壨��״��������
��1��д�����������У��йط�Ӧ�Ļ�ѧ����ʽ___________��_________________��
��2����ɸ÷�Ӧ������Ҫ��ȡ10 mol/L��Ũ����_________mL��
��3�����������NO2�����Ϊ ?��NO�����Ϊ ??��
�ο��𰸣�(1��Cu + 4HNO3(Ũ) = Cu(NO3)2 + 2NO2��+ 2H2O?
3Cu + 8HNO3(ϡ) = 3Cu(NO3)2 + 2NO��+ 4H2O
��2��600 mL
��3��V(NO2)= 22.4L? V(NO)=" 22.4L"
���������(1) Cu + 4HNO3(Ũ) = Cu(NO3)2 + 2NO2��+ 2H2O?
3Cu + 8HNO3(ϡ) = 3Cu(NO3)2 + 2NO��+ 4H2O
ע�ⷽ��ʽ����ƽ�������ͷ���š�
��2��2Cu��6HNO3=2Cu(NO3)2��NO2����NO����3H2O
���ݻ�ѧ����ʽ��128 gͭ��2molCu���������Ҫ10 mol/L��Ũ���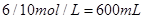
(3) NO2��NO�Ļ������44.8 L����״������,��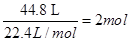 ����
����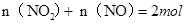 ��
��
��128gͭʧȥ���ӣ�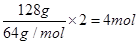 ����
����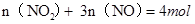 ?�ڣ��ɢ٢ڿɽ��
?�ڣ��ɢ٢ڿɽ��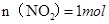 ��
��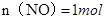 ����
����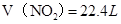 ,
, ��
��
�����������ۺ��Խ�ǿ��������ͭ��Ũ���ᡢϡ���ᷴӦ��֪ʶ�㣬����߿�����������ʱӦץס��ʧ�����غ㣬����Ϊ��
�����Ѷȣ�һ��
4��ѡ���� ���ڷ�Ӧ14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4������˵����ȷ����
A��ֻ������ͭ��������
B��SO42-�Ȳ������������ֲ��ǻ�ԭ����
C���������뱻��ԭ����Ԫ�ص�������Ϊ3��7
D������1mol����ͭ�μӷ�Ӧʱ���÷�Ӧת��1mol����
�ο��𰸣�C
������������⿼��������ԭ��Ӧ����һ���Ѷȣ�ѧ����ȷ��Ӧ�и�Ԫ�ػ��ϼ۵ı仯�ǽ��Ĺؼ���FeS2��Fe��SԪ�صĻ��ϼ��ǽ����Ѷȣ���ע��������ԭ��Ӧ�е����غ��������14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4��Ӧ�У�CuSO4��CuԪ�صĻ��ϼ���+2����Ϊ+1����FeS2��Fe�Ļ��ϼ�Ϊ+2��S�Ļ��ϼ�Ϊ-1����5����FeS2�У�һ����10��-1�۵�S,����7��S�Ļ��ϼ���-1���͵�-2���õ���������Ϊ7������Cu�õ���14�����ӣ��õ��ĵ�������Ϊ21������Ȼ����3��SԪ�صĻ��ϼ���-1���ߵ�+6�ۣ�ʧȥ������ҲΪ21�������ϵ����غ㡣��Cu2Sֻ�ǻ�ԭ������е�Cu��S���DZ���ԭ�õ��ġ�5molFeS2�μӷ�Ӧת�Ƶ�����Ϊ21mol������SO42-Ϊ�������FeS2��������������������ԭ����
A��������ͭ��CuԪ�صĻ��ϼ۽��ͣ�FeS2�в���SԪ�صĻ��ϼ�Ҳ���ͣ�������ͭ��FeS2���Ǹ÷�Ӧ�е�����������A����
B����FeS2�в���SԪ�صĻ��ϼ���-1���ߵ�+6�ۣ��������в���SO42-Ϊ���������B����
C���ɷ�Ӧ��֪��10��Sԭ���У���3��Sԭ��ʧȥ���ӣ�7��Sԭ�ӵõ����ӣ��������������뱻��ԭ�����������Ϊ3��7����C��ȷ��
D���ɵ����غ��֪��14mol����ͭ�μӷ�Ӧʱ��ת��21mol���ӣ�����1mol����ͭ�μӷ�Ӧʱ���÷�Ӧת��1.5mol���ӣ���D����ѡC��
�����Ѷȣ���
5��ѡ���� ��֪ICl��п��ˮ�ķ�Ӧ���£�2ICl��2Zn �T ZnI2��ZnCl2��ICl��H2O �T HCl��HIO������˵����ȷ���ǣ�?��
A��ZnCl2���������������ǻ�ԭ����
B��ZnI2���������������ǻ�ԭ����
C����ICl��ˮ��Ӧ�У�ICl����������H2O�ǻ�ԭ��
D��ICl��ˮ��Ӧ��������ԭ��Ӧ
�ο��𰸣�B
���������A��B���Ӧ�У�ZnԪ�صĻ��ϼ����ߣ�IԪ�صĻ��ϼ۽��ͣ���ZnI2���������������ǻ�ԭ�����A��B��ȷ��
B����Ӧ���У�IԪ�صĻ��ϼ۽��ͣ���IClֻ������������B����
C��D���Ӧ�У�û��Ԫ�صĻ��ϼ۱仯������������ԭ��Ӧ����C��D����
��ѡB��
����������������Ϣϰ�⣬ע�����ƵĹ��ɼ�ȷ�ж�ICl��IΪ+1�ۣ�ClΪ-1���ǽ����Ĺؼ���Ȼ�����û��ϼ���������Ӧ���ɡ�
�����Ѷȣ�һ��