1、选择题 胶体的最本质的特征是
A.丁达尔效应
B.可以通过滤纸
C.布朗运动
D.分散质颗粒的直径在1nm~100nm之间。
参考答案:D
本题解析:胶体的本质特征是胶体颗粒的大小,其他的性质都是由此而决定的,因此本题答案应选D。
本题难度:一般
2、选择题 以下关于化学实验中“先与后”的说法中正确的是
①加热试管时,先均匀加热,后局部加热;?
②用排水法收集气体后,先移出导管后撤酒精灯;
③制取气体时,先检验装置气密性后装药品;
④点燃可燃性气体如H2、CO等时,先检验气体纯度后点燃;
⑤做H2还原CuO实验时,先通H2后加热CuO,反应完毕后,先撤酒精灯待试管冷却后停止通H2;
⑥浓硫酸不慎洒到皮肤上,先迅速用干布擦去,后用水冲洗,再涂上3%~5%的NaHCO3溶液;若是其他酸,先用大量水冲洗后再涂上NaHCO3溶液;
⑦碱流到桌子上,先加稀醋酸溶液中和,后用水洗.
A.①②③⑤⑦
B.①②④⑤⑥
C.①②③④⑤
D.全部
参考答案:D
本题解析:分析:①试管加热时要防止局部骤热发生爆炸;
②用排水法收集氧气后,要防止液体倒吸炸裂试管;
③制取气体时,要先检查装置气密性;
④点燃可燃性气体是为防止爆炸要验纯;
⑤做H2还原CuO实验开始时要排除空气,结束时要防止金属铜被氧气氧化;
⑥浓硫酸具有强氧化性和腐蚀性,一定注意使用;万一滴到皮肤上,一定谨慎处理;
⑦碱流到桌子上,先加稀醋酸溶液中和,后用水洗,降低碱的腐蚀性.
解答:①试管加热时为防止局部骤热发生爆炸,先均匀加热,后局部加热,故①正确;
②用排水法收集气体后,为防止液体倒吸炸裂试管,应该先移出导管后撤酒精灯,故②正确;
③制取气体时,一定要先检查装置气密性后装药品,故③正确;
④点燃可燃性气体如H2、CO等时,为防止爆炸要验纯后点燃,故④正确;
⑤做H2还原CuO实验开始时要排除空气,先通入氢气,结束时要防止金属铜被氧气氧化,先撒酒精灯待试管冷却后停止通H2,故⑤正确;
⑥浓硫酸溶于水放出大量的热,并有强烈的腐蚀性,浓硫酸沾到皮肤或衣服上,应先用布试去,再用大量水冲洗,然后涂上3%-5%的NaHCO3溶液,若是其他酸,先用大量水冲洗后再涂上NaHCO3溶液,故⑥正确;
⑦碱流到桌子上,先加稀醋酸溶液中和降低碱的腐蚀性,后用水洗,故⑦正确;
故选D.
点评:本题考查化学实验的基本操作,注意化学实验操作的要领是解题的关键,题目难度不大.
本题难度:简单
3、选择题 用惰性电极电解下列溶液,一段时间后,停止电解,向溶液中加入一定质量的另一种物质(括号内),能使溶液完全复原的是
A.CuCl2 (CuO)
B.NaOH (NaOH)
C.CuSO4 (CuCO3)
D.NaCl (NaOH)
参考答案:C
本题解析:试题分析:惰性电极电解氯化铜溶液,电解产物是铜和氯气,因此应该加入氯化铜,A不正确;惰性电极电解氢氧化钠溶液,实质是电解水,加入的应该是水,B不正确;惰性电极电解硫酸铜溶液,生成物是铜、氧气和硫酸,所以需要加入的是氧化铜或碳酸铜,C正确;惰性电极电解氯化钠溶液,电极生成物是氯气、氢气和氢氧化钠,所以需要加入的是氯化氢,D不正确,答案选C。
考点:考查电解产物的判断和应用
点评:该题是中等难度的试题,也是高考中的常见考点,试题基础性强,侧重考查学生分析问题、解决问题的能力,有助于培养学生的逻辑思维能力和发散思维能力。该题的关键是准确判断电极产物并能灵活运用。
本题难度:困难
4、选择题 既可以用向上排空气法收集又可以用排水法收集的气体是
A.H2
B.O2
C.NH3
D.NO2
参考答案:B
本题解析:分析:和水、氧气不反应且密度大于空气的气体,不溶于水,可以采用向上排空气法收集又可以用排水法收集.
解答:A.氢气和水不反应,常温下和氧气不反应,但氢气密度小于空气密度,所以可以采用排水法或向下排空气法收集,故A错误;
B.氧气和水不反应,且密度大于空气密度,所以可以采用排水法或向上排空气法收集,故B正确;
C.氨气和水反应,所以不能用排水法收集,故C错误;
D.二氧化氮和水反应,所以不能用排水法收集,故D错误;
故选B.
点评:气体的收集方法与气体的溶解性、密度等物理性质密切相关,根据气体的溶解性及密度确定收集方法,难度不大.
本题难度:简单
5、填空题 雾霾含有大量的污染物SO2、NO。工业上变“废”为宝,吸收工业尾气SO2和NO,可获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素):
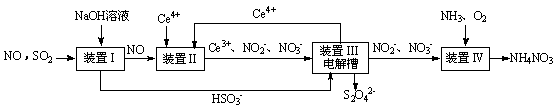
(1)装置Ⅰ中的主要离子方程式为 。
(2)含硫各微粒(H2SO3、HSO3-和SO32-)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数X(i)与溶液pH 的关系如图所示。
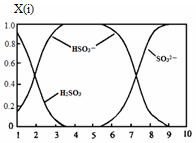
①若是0.1molNaOH反应后的溶液,测得溶液的pH=8时,溶液中个离子由大到小的顺序是 。
②向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因: 。
(3)写出装置Ⅱ中,酸性条件下的离子方程式 。
(4)装置Ⅲ还可以使Ce4+再生,其原理如下图所示。
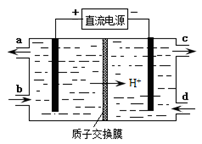
①生成Ce4+从电解槽的 (填字母序号)口流出。
②写出与阴极的反应式 。
(5)已知进入装置Ⅳ的溶液中,NO2-的浓度为a g・L-1,要使1 m3该溶液中的NO2-完全转化为NH4NO3,需至少向装置Ⅳ中通入标准状况下的O2 L。(用含a代数式表示,计算结果保留整数)
参考答案:(每空2分)
(1)SO2 + OH-="==" HSO3-
(2)①c(Na+>c(SO32-)>c(HSO3-)>c(OH-)>c(H+)
②HSO3- 在溶液中存在电离平衡:HSO3- SO32-+H+,加入CaCl2溶液后,Ca2++SO32-="==" CaSO3↓使电离平衡右移,c(H+)增大。
SO32-+H+,加入CaCl2溶液后,Ca2++SO32-="==" CaSO3↓使电离平衡右移,c(H+)增大。
(3)NO+2H2O+3Ce4+===3Ce3++NO3-+4H+、NO+H2O+Ce4+===Ce3++NO2-+2H+
(4)①a ②2HSO3-+4H++ 4e-="==" S2O32-+3H2O
(5)243a(242a、244a、5600a /23都给分)
本题解析:(1)装置Ⅰ中的将SO2变成了HSO3-,离子方程式是SO2 + OH-="==" HSO3-。
(2)①若是0.1molNaOH反应后的溶液,测得溶液的pH=8时,图像中的c(SO32-)>c(HSO3-),而c(OH-)=10-6mol/L,远小于c(OH-),故溶液中离子浓度为:c(Na+>c(SO32-)>c(HSO3-)>c(OH-)>c(H+)。②HSO3- 在溶液中存在电离平衡:HSO3- SO32-+H+,加入CaCl2溶液后,Ca2++SO32-="==" CaSO3↓使电离平衡右移,c(H+)增大。
SO32-+H+,加入CaCl2溶液后,Ca2++SO32-="==" CaSO3↓使电离平衡右移,c(H+)增大。
(3)在酸性条件下装置Ⅱ中,Ce4+将NO氧化为NO3-或NO2-,本身还原为Ce3+,有两个反应,即NO+2H2O+3Ce4+===3Ce3++NO3-+4H+、NO+H2O+Ce4+===Ce3++NO2-+2H+。
(4)装置Ⅲ使Ce3+→Ce4+,反应过程失去电子,在阳极发生,接电源正极,故生成Ce4+从电解槽的a口出来;阴极HSO3-得到电子生成S2O32,即2HSO3-+4H++ 4e-="==" S2O32-+3H2O。
(5)装置Ⅳ中的与O2和NO2-参加的反应:2NH3+2H++O2+2NO2-===2NH4NO3,n(O2)=n(NO2-)= ×1000L×a g・L-1/46g・mol-1,V(O2)=22.4L・mol-1 n(O2)= 243a。
考点:离子方程、电极反应式的书写及简单化学计算。
本题难度:困难