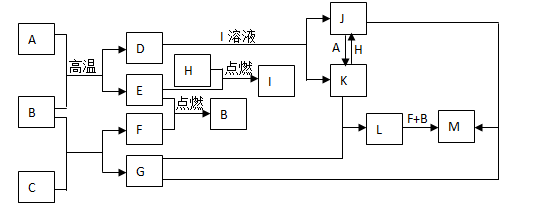
1、填空题 (6分)下列框图题中,已知A、E、F、H是单质,其中只有A是一种常见的金属单质,其它都是气体,且H是呈黄绿色;B是最常见液体,C是一种淡黄色粉末,G的焰色反应呈黄色,L是白色沉淀,M是红褐色沉淀。部分反应的某些产物未标出。
回答下列问题:
(1)写出C化学式:??I的电子式??;
(2)写出离子方程式:
K+H:??;
(3)写出化学方程式:
B+C:??;
参考答案:(6分)(1)Na2O2、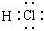 ;
;
(2)2Fe2++Cl2=2Fe3++2Cl-;(3)2Na2O2+2H2O=4NaOH+O2↑
本题解析:本题推断中题眼较多,①物质物理性质推断:H是呈黄绿色,单质为Cl2;B是最常见液体,可能为水;C是一种淡黄色粉末,化合物可能为Na2O2;G的焰色反应呈黄色,为钠的化合物;L是白色沉淀,M是红褐色沉淀,可能为Fe(OH)2和Fe(OH)3。②反应条件,A+B,可能为Fe与水的反应,E(g)+F(g)B(常见液体),E(g)+H(g)(黄绿色)I,JAHK(其可能为变价金属)。
本题难度:一般
2、简答题 已知化合物A、B、E的焰色反应均为黄色,常温下,A为淡黄色固体,D分子中含有22个电子,由A、B组成的混合物与其他物质间的转化关系如图所示(部分生成物未列出).回答下列问题: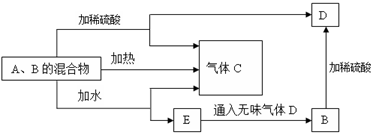
(1)写出A和C的化学式:A______,C______.
(2)混合物中加水后发生反应的化学方程式为:______.
(3)B→D反应的离子方程式为______.
参考答案:化合物A、B、E的焰色反应均为黄色,都含有Na元素,常温下,A为淡黄色固体,则A为Na2O2,A、B组成的混合物加水生成气体C为O2;含钠化合物B能与硫酸反应生成无色无味气体D,D分子中含有22个电子,D应是CO2,结合由A、B组成的混合物加热可以生成氧气,可推知B为NaHCO3,则E为Na2CO3,
(1)由上述分析可知,A为Na2O2,C为O2,故答案为:Na2O2;O2;
(2)混合物中加水后发生反应的化学方程式为:2Na2O2+4NaHCO3=4Na2CO3+O2↑+2H2O,故答案为:2Na2O2+4NaHCO3=4Na2CO3+O2↑+2H2O;
(3)B→D反应的离子方程式为:CO32-+2H+=CO2↑+H2O,故答案为:CO32-+2H+=CO2↑+H2O.
本题解析:
本题难度:简单
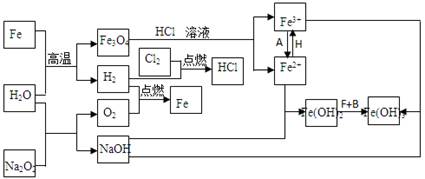
3、简答题 现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图1所示(图中有些反应的生成物和反应的条件没有标出).
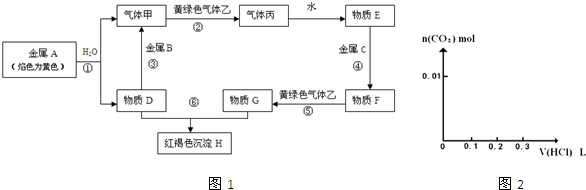
请回答下列问题:
(1)写出下列物质的化学式:B______、丙______、乙______.
(2)写出下列反应的离子方程式:
反应①______;
反应⑤______;
反应⑥______.
(3)将0.4gD和1.06gNa2CO3混合并配成溶液,向溶液中滴加0.1mol?L-1稀盐酸.在如图2所示的坐标系中画出能正确表示加入盐酸的体积和生成CO2的物质的量的关系图象.______.
参考答案:金属A颜色反应为黄色证明为Na,与水反应生成气体甲为H2,D为NaOH;金属B和氢氧化钠溶液反应,说明B为Al,气体甲和氯气反应生成丙为HCl,物质E为盐酸溶液,物质D氢氧化钠和物质G为反应生成红褐色沉淀H为Fe(OH)3,G为FeCl3,推断物质F为FeCl2,C为Fe,
(1)由上述分析可知,B为Al,丙为HCl,乙为Cl2,故答案为:Al;HCl;Cl2;
(2)反应①为2Na+2H2O=2Na++2OH-+H2↑,反应⑤为Cl2+2Fe2+=2Fe3++2Cl-,反应⑥为Fe3++3OH-=Fe(OH)3↓,
故答案为:2Na+2H2O=2Na++2OH-+H2↑;Cl2+2Fe2+=2Fe3++2Cl-;Fe3++3OH-=Fe(OH)3↓;
(3)0.4gNaOH和1.06gNa2CO3混合并配成溶液,向溶液中滴加0.1mol?L-1稀盐酸,先发生NaOH+HCl=NaCl+H2O,消耗0.1L盐酸,然后发生Na2CO3+HCl=NaCl+NaHCO3,消耗0.1L盐酸,且不生成二氧化碳,最后发生NaHCO3+HCl=NaCl+H2O+CO2↑,消耗0.1L盐酸生成0.01mol二氧化碳,如图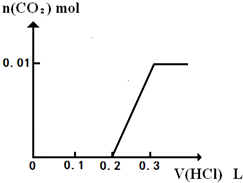 ,
,
故答案为: .
.
本题解析:
本题难度:一般
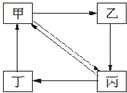
4、选择题 下表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
| 编号 | 甲 | 乙 | 丙 | 丁
①
Cu
CuO
CuSO4
Cu(NO3)2
②
Na2CO3
NaOH
NaHCO3
CO2
③
N2
NH3
NO
NO2
④
CH3CH2Br
C2H5OH
CH2=CH2
CH3CH3
|
A.①②③
B.①②③④
C.①③④
D.②③④