| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学必考知识点《物质的量》高频考点强化练习(2019年最新版)(二)
参考答案:D 本题解析:根据C="n/V" 得C="1mol/1L=1" mol/L,选D。 本题难度:一般 2、选择题 已知NH3和HCl都能用来做喷泉实验,若在标准状况下用两个大小不同的烧瓶分别收集满NH3和HCl气体,实验后两个烧瓶中溶液的关系是 |
参考答案:A
本题解析:在标准状况下用两个大小不同的烧瓶分别收集满NH3和HCl气体用来做喷泉实验,可知两者最后两烧瓶均充满溶液,可知两溶液的浓度与容积无关,均可根据公式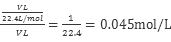 ,但两溶液的密度、摩尔质量均不相同,则质量分数不同,故A项正确。
,但两溶液的密度、摩尔质量均不相同,则质量分数不同,故A项正确。
考点:溶液浓度计算。
本题难度:一般
3、填空题 (9分)(1)明矾晶体可用来净水,它的化学式为 。
(2)反应KClO3+6HCl=KCl+3Cl2↑+3H2O 中氧化剂是 氧化剂和还原剂的物质的量之比:_______。
(3)加热10.0g碳酸钠和碳酸氢钠的混合物至质量不在变化,剩余固体的质量为8.45g,则混合物中碳酸钠的质量分数为 。 (填能或者不能)用澄清石灰水鉴别碳酸钠和碳酸氢钠溶液。
参考答案:(9分)(1)KAl(SO4)2・12H2O (1分)
(2)KClO3 (2分) 1:5 (2分) (3)42% (2分) 不能(2分)
本题解析:(1)明矾属于复盐,其化学式是KAl(SO4)2・12H2O。
(2)根据反应的方程式可知,氯酸钾中氯元素的化合价从+5价降低到0价,而氯化钾中氯元素的化合价从-1价升高到0价,所以氧化剂是氯酸钾,还原剂是氯化钾,二者的物质的量之比是1:5。
(3)碳酸氢钠受热分解的化学方程式是2NaHCO3 Na2CO3+H2O+CO2↑,根据题意可知,反应中固体质量减少1.55g,所以碳酸氢钠的质量是
Na2CO3+H2O+CO2↑,根据题意可知,反应中固体质量减少1.55g,所以碳酸氢钠的质量是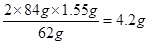 ,所以混合物中碳酸钠的质量分数为4.2÷10=42%。碳酸钠和碳酸氢钠都能和氢氧化钙反应生成白色沉淀碳酸钙,所以不能用澄清石灰水鉴别碳酸钠和碳酸氢钠溶液。
,所以混合物中碳酸钠的质量分数为4.2÷10=42%。碳酸钠和碳酸氢钠都能和氢氧化钙反应生成白色沉淀碳酸钙,所以不能用澄清石灰水鉴别碳酸钠和碳酸氢钠溶液。
考点:考查氧化还原反应的有关判断、依据碳酸氢钠分解的有关计算等
点评:如果是同一种元素的高价态和低价态之间发生氧化还原反应,则生成物的价态只能介于二者之间,且氧化产物的价态不能高于还原产物的价态,据此可以进行有关的判断。
本题难度:一般
4、选择题 设阿伏加德罗常数的值为NA,则下列说法正确的是
A.常温常压下,18.0g NH4+中所含的质子数为10 NA
B.111g CaCl2晶体中所含共用电子对的数目为2NA
C.常温下,2.7 g铝片投入足量的浓硫酸中,铝失去的电子数为0.3NA
D.室温下,8 g甲烷含有共价键数为2NA
参考答案:D
本题解析:A错,常温常压下,18.0g NH4+中所含的质子数为11 NA;B错,2晶体为离子晶体,不存在共用电子对;C错,常温下,铝遇冷的浓硫酸会发生钝化;D正确;
本题难度:一般
5、选择题 下列各组物质中,所含分子数一定相同的是?
[? ]
A.2g?H2和16?g?O2?
B.0.1mol HCl和2.24LAr?
C.150℃、1.01×105?Pa时,1L?CO2和1LH2O?
D.28g?CO和6.02×1022个O3
参考答案:B
本题解析:
本题难度:简单
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点整理《原电池原理.. | |