1、选择题 认识反应条件对化学反应的影响,对学好化学具有重要意义。下列说法正确的是
A.等体积的甲烷与氯气在光照条件下反应,一定只生成一氯甲烷和氯化氢
B.钠在敞口容器中长期存放或在空气中燃烧的产物一定是Na2O2
C.溶液中盐与盐的复分解反应,一定不会有气体产生
D.向苯酚钠溶液中通入少量CO2或过量CO2,产物中一定含有NaHCO3
参考答案:D
本题解析:
A、甲烷与氯气在光照条件下发生取代反应,甲烷中的氢原子可被取代生成一氯甲烷、二氯甲烷、三氯甲烷及四氯化碳和氯化氢
B、钠在敞口容器中长期存放被氧化为Na2O,而在空气中燃烧的产物是Na2O2
C、错误,例如:铵盐与碱加热可产生氨气
D、由于酸性:碳酸>苯酚>HCO3―,故向苯酚钠溶液中通入少量CO2或过量CO2,产物一定为NaHCO3
故答案为D
本题难度:一般
2、推断题 【三选一----物质结构与性质】?
有?X、Y、Z、W四种元素,其中X是周期表中原子半径最小的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29。
请回答下列问题:
(1)由X、Y构成的10电子化合物的分子式为___________;基态Y原子的核外电子排布式为___________;
(2)离子Z3-的中心原子轨道杂化类型为____________,离子Z3-?的空间构型为___________;
(3)化合物ZX3的沸点比化合物YX4的高,其主要原因是____________?。
(4)元素Y的一种氧化物与元素Z的一种氧化物互为等电子体,元素Z的这种氧化物的分子式是______________。
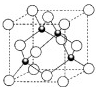
(5)元素W的一种氯化物晶体的晶胞结构如图所示,该氯化物的化学式是____________,它可与浓盐酸发生非氧化还原反应,生成配合物H2WCl3,反应的化学方程式为_____________。
参考答案:(1)CH4?;? 1s22s22p2
(2)sp杂化?;?直线型?
(3)NH3分子间存在氢键
(4)N2O
(5)CuCl?; CuCl+2HCl=H2CuCl3? (或CuCl+2HCl=H2[CuCl3])
本题解析:
本题难度:一般
3、选择题 下列哪一个参数近似会造成元素的性质最相似
A.第一电离能
B.电负性
C.原子半径
D.电子层构型
参考答案:C
本题解析:从原理上说,不同的几种元素的上述几种参数近似,都可能造成元素性质在某些方面有相似之处,但当元素的原子半径近似时元素性质更接近一些,例如40号元素锆和72号元素铪,它们原子半径近似,元素性质非常接近,以至于使用很多方法都不能将它们分离开来。
本题难度:一般
4、选择题 已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述中正确的是
A.原子半径:A>B>D>C
B.原子序数:d>c>b>a
C.离子半径:C>D>B>A
D.元素的第一电离能:A>B>D>C
参考答案:C
本题解析:
本题难度:一般
5、选择题 下列操作和现象与结论均正确的是(?)
选项
| 操作
| 现象
| 结论
|
A
| 向盐酸酸化的Ba(NO3)2溶液中通入SO2
| 有白色沉淀生成
| BaSO3难溶于酸
|
B
| 向等浓度的KCl、KI混合液中滴加AgNO3溶液
| 先出现黄色沉淀
| Ksp(AgCl)>Ksp(AgI)
|
C
| 溴乙烷与NaOH水溶液共热后,加HNO3酸化,滴加AgNO3溶液
| 出现淡黄色沉淀
| 溴乙烷含溴元素
|
D
| 取久置的Na2O2粉末,向其中滴加过量的盐酸
| 产生无色气体
| Na2O2没有变质
|
?
参考答案:BC
本题解析:盐酸酸化的硝酸钡溶液中相当于有硝酸,在通入SO2,SO2容易被硝酸氧化,故生成难溶的BaSO4沉淀,A错误;Ksp(AgCl)>Ksp(AgI),所以在等浓度的KCl、KI混合液中滴加AgNO3溶液时先生成更难溶的淡黄色沉淀AgI,B正确;检验溴乙烷中的溴元素的方法、操作、现象均正确,C正确;久置的过氧化钠容易和空气中的CO2气体反应生成碳酸钠,碳酸钠滴加盐酸也会产生气体(CO2),所以不能通过产生气体就判断过氧化钠没变质,D错误;故选BC。
本题难度:一般