1、选择题 下列各组离子在指定条件下,能大量共存的是( )
①在含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN-
②使pH试纸变深蓝的溶液中:K+、CO32-、Na+、AlO2-
③水电离的c(H+)=10-13mol/L的溶液中:ClO-、CO32-、NO3-、NH4+、SO32-
④在加入铝粉能产生H2的溶液中:NH4+、Fe2+、SO42-、NO3-
⑤使甲基橙变红的溶液中:MnO4-、NO3-、SO42-、Na+、Fe3+
⑥能使碘化钾淀粉试纸变蓝的溶液中:Na+、NH4+、S2-、Br-.
A.①③
B.②⑤
C.①②⑤
D.③⑥
参考答案:①因在含大量Fe3+的溶液中,Fe3+、SCN-能结合生成络离子,则不能大量共存;
②pH试纸变深蓝的溶液中存在大量OH-,该条件下该组离子不发生反应,则能大量共存;
③水电离的c(H+)=10-13mol/L的溶液,水的电离受到抑制,可能为酸或碱的溶液,H+能分别为ClO-结合生成弱电解质,与CO32-、SO32-结合生成气体和水,OH-与NH4+结合生成弱电解质,则不能大量共存;
④加入铝粉能产生H2的溶液可能为酸或碱的溶液,碱溶液中OH-与NH4+结合生成弱电解质,酸溶液中Fe2+、NO3-发生氧化还原反应,则不能大量共存;
⑤甲基橙变红的溶液显强酸性,该条件下该组离子不发生反应,则能大量共存;
⑥使碘化钾淀粉试纸变蓝的溶液,含有氧化性较强的物质,而S2-具有较强的还原性,能发生氧化还原反应,则不能大量共存;
显然②⑤组离子在指定条件下能大量共存,故选B.
本题解析:
本题难度:一般
2、选择题 下列各组离子一定能大量共存的是
A.在强碱性溶液中: NH4+、Na+、NO3-、CO32-
B.能使紫色石蕊试液变蓝的溶液中:Ca2+、Fe2+、AlO2-、Cl-
C.某无色溶液中:Cu2+、Al3+、NO3-、SO42-
D.含有大量H+的溶液中:Na+、K+、Al3+、NO3-
参考答案:D
本题解析:A选项,铵离子与碱溶液不能大量共存。B选项,紫色石蕊试液变蓝的溶液为酸性,不能与偏铝酸根共存。C选项,铜离子为蓝色。故错误。D选项,正确。
本题难度:一般
3、选择题 常温下,下列各组离子在指定溶液中一定能大量共存的是(?)
A.1.0 mol・L-1的KNO3溶液:H+、Fe2+、Cl-、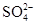
B.甲基橙呈红色的溶液: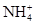 、Ba2+、
、Ba2+、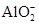 、Cl-
、Cl-
C.pH=12的溶液:K+、Na+、CH3COO-、Br-
D.与铝反应产生大量氢气的溶液:Na+、K+、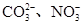
参考答案:C
本题解析:A项,KNO3中的 与H+在一起,相当于硝酸,能将Fe2+氧化为Fe3+,A项不能大量共存;B项,甲基橙呈红色说明溶液中含大量的H+,H+能与
与H+在一起,相当于硝酸,能将Fe2+氧化为Fe3+,A项不能大量共存;B项,甲基橙呈红色说明溶液中含大量的H+,H+能与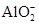 反应,B项不能大量共存;C项,pH=12的溶液中含大量的OH-,与K+、Na+、CH3COO-、Br-均不反应,可以大量共存,C项正确;D项,与铝反应产生氢气,可能是较强酸性溶液(含大量H+),也可能是强碱性溶液(含大量OH-),H+可以与
反应,B项不能大量共存;C项,pH=12的溶液中含大量的OH-,与K+、Na+、CH3COO-、Br-均不反应,可以大量共存,C项正确;D项,与铝反应产生氢气,可能是较强酸性溶液(含大量H+),也可能是强碱性溶液(含大量OH-),H+可以与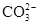 反应,与题目要求“一定能大量共存”不符,D项错误。
反应,与题目要求“一定能大量共存”不符,D项错误。
限定条件的离子共存题的分析方法
解答此类题目的原则是:离子在所给条件下互不反应,判断的步骤是:先看条件,后看反应。本题就是一个带有“限定条件”的典型题目,它代表了今后高考的命题方向。“限定条件”的设置主要为:溶液的酸碱性、直接说明溶液中已含有某种离子、溶液是否带有颜色等,另外,还要特别注意是否发生“氧化还原反应”,它是高考命题较为稳定的角度。
本题难度:一般
4、选择题 下列叙述正确的是(?)
A.将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO42-)>c(NH4+)
B.两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2
C.pH=11的NaOH的溶液与pH=3的醋酸溶液等体积混合,滴入石蕊试液呈红色
D.向0.1 mol/L的氨水中加入少量硫酸铵固体,则溶液中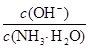 增大
增大
参考答案:C
本题解析:由电荷守恒可知c(NH4+)+c(H+)=2c(SO42-)+c(OH-),当pH=7时,c(NH4+)=2c(SO42-),故A项错;醋酸是弱酸,浓度越大,电离程度越小,当两溶液pH相差1时,c1≠10c2,B项错;pH=11的NaOH与pH=3的醋酸等体积混合后溶液显酸性,滴入石蕊试液呈红色,C项对;氨水存在电离平衡:NH3・H2O?NH4++OH-,加(NH4)2SO4固体,平衡左移,导致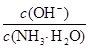 减小,D项错。
减小,D项错。
本题难度:一般
5、选择题 室温下,某未知溶液中 ,且含有大量Al3+和NO3-,检验此溶液中是否大量存在以下6 种离子;①SiO32-②NH4+③Fe2+ ④Na+ ⑤HCO3-⑥Cl-,其中不必检验就能加以否定的离子是(?)
,且含有大量Al3+和NO3-,检验此溶液中是否大量存在以下6 种离子;①SiO32-②NH4+③Fe2+ ④Na+ ⑤HCO3-⑥Cl-,其中不必检验就能加以否定的离子是(?)
A.①③⑤
B.②③④
C.①②⑥
D.④⑤⑥
参考答案:A
本题解析:由题意知,溶液呈强酸性,即有大量的H+,且含有Al3+和NO3-:
2H+ + SiO32-=H2SiO3↓;Fe2+ 在酸性条件下可被NO3-氧化;HCO3- + H+ =CO2↑+ H2O ;
本题难度:一般