1、选择题 下列各组离子中,因发生氧化还原反应而不能大量共存的是
[? ]
A.Fe3+、H+、SO42-、ClO-
B.Fe3+、Fe2+、SO42-、NO3-
C.Al3+、Na+、SO42-、CO32-
D.K+、H+、Cl-、MnO4-
参考答案:D
本题解析:
本题难度:一般
2、选择题 小东欲配制含有大量下列各离子的溶液,其中能实现的是(?)
A.K+、H+、SO42-、OH-
B.Na+、Ca2+、CO32-、NO3-
C.Na+、H+ 、Cl-、CO32-
D.Na+、Cu2+、Cl-、SO42-
参考答案:D
本题解析:略
本题难度:一般
3、选择题 下列关于电解质溶液的正确判断是
[? ]
A.在pH= 12的溶液中,K+、Cl-、HCO3-、Na+可以常量共存
B.在pH =O的溶液中,Na+、NO3-、SO32-、K+可以常量共存
C.由O.l moI/L元碱BOH溶液的pH=10,可推知BOH溶液存在BOH= B++OH-
D.由0.lmoI/L一元酸HA溶液的pH =3,可推知NaA溶液存在A-+H2O HA-+OH-
HA-+OH-
参考答案:D
本题解析:
本题难度:一般
4、填空题 在a、b两支试管中,分别装入足量Na2CO3粉末,然后向两支试管中分别加入相同物质的量浓度、相同体积的稀盐酸和稀醋酸。填写下列空白。
(1)a、b两支试管中的现象:相同点是__________,不同点是__________________。原因是__________________。
(2)a、b两支试管中生成气体的速率开始时是a__________b,反应完毕后生成气体的总体积是a__________b,原因是__________________。
参考答案:(1) 都产生无色气泡 产生气泡的快慢程度不同,a中产生气泡快 c(H+)不同,a中c(H+)大
(2)大于 等于 开始反应时盐酸中c(H+)大,但两者H+的总物质的量相等
本题解析:盐酸是强酸,醋酸是弱酸,所以在浓度相等的条件下,盐酸和碳酸钠的反应速率快。但由于二者的物质的量是相等的,所以最终生成的气体体积相等。
点评:该题是基础性试题的考查,难度不大。试题基础性强,侧重对学生基础知识的巩固和训练,有利于培养学生灵活运用基础知识解决实际问题的能力。
本题难度:一般
5、选择题 根据表中信息,判断下列叙述中正确的是
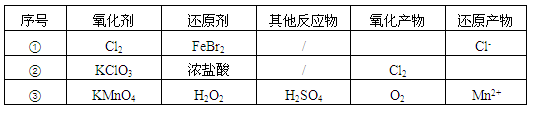
A.表中①组的反应只可能有一种元素被氧化和一种元素被还原
B.氧化性强弱的比较: KClO3>Fe3+>Cl2>Br2
C.由表中①②组反应推测:ClO3-、Br-、H+、Fe2+不能在浓溶液中大量共存
D.表中③组反应的离子方程式为:2MnO4-+ 3H2O2 + 6H+=2Mn2+ + 4O2↑+ 6H2O
参考答案:C
本题解析:A.表中①组的反应若Cl2过量,则发生反应:2Fe2++4Br-+3Cl2 = 2Fe3+ + 2Br2 + 6Cl-;若Cl2少量,则发生反应:2Fe2++Cl2 = 2Fe3++ 2Cl-;相对量的多少不同,被氧化的元素种类不同。错误。B.在氧化反应反应中,一般是氧化剂的氧化性大于氧化产物的氧化性。KClO3+6HCl(浓)  KCl+ 3Cl2↑+3H2O,证明氧化性:KClO3>Cl2;2NaBr+Cl2 =2NaCl+ Br2;证明氧化性:Cl2>Br2; 2FeBr2 + 2Br2= 2FeBr3,证明氧化性:Br2>Fe3+。因此氧化性KClO3>Cl2>Br2>Fe3+。错误。C.在浓溶液中ClO3-、Br-、H+、Fe2+会发生氧化反应反应而不能大量共存。正确。D.表中③组反应的离子方程式为:2MnO4-+ 5H2O2 + 6H+=2Mn2+ + 5O2↑+ 8H2O
KCl+ 3Cl2↑+3H2O,证明氧化性:KClO3>Cl2;2NaBr+Cl2 =2NaCl+ Br2;证明氧化性:Cl2>Br2; 2FeBr2 + 2Br2= 2FeBr3,证明氧化性:Br2>Fe3+。因此氧化性KClO3>Cl2>Br2>Fe3+。错误。C.在浓溶液中ClO3-、Br-、H+、Fe2+会发生氧化反应反应而不能大量共存。正确。D.表中③组反应的离子方程式为:2MnO4-+ 5H2O2 + 6H+=2Mn2+ + 5O2↑+ 8H2O
本题难度:一般