1、选择题 下列说法正确的是?(?)?
A.PH=0的溶液中,K+、I-、SO42-、Cl-可以大量共存
B.在无色溶液中,Na+、Fe3+、HCO3-、NO3-可以大量共存
C.在显中性的水溶液中,c(OH-)不一定等于
D.纯水的PH一定等于7
参考答案:A
本题解析:略
本题难度:一般
2、选择题 某溶液含有下列离子,加入Ba(OH)2溶液后,溶液中哪种离子数目不会减少( )
A.CO32-?
B.NH4+
C.SO42-
D.NO3-
参考答案:A.因CO32-与Ba2+反应生成沉淀,则离子数目减少,故A不选;
B.NH4+与OH-反应生成氨气,则离子数目减少,故B不选;
C.因SO42-与Ba2+反应生成沉淀,则离子数目减少,故C不选;
D.NO3-与Ba(OH)2溶液不反应,则离子数目不变,故D选;
故选D.
本题解析:
本题难度:一般
3、选择题 常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3-
B.甲基橙呈黄色的溶液:I-、Ba2+、AlO2-、Cl-
C.c(H+)=1.0×10-13mol/L溶液中C6H5O-、K+、SO42-、Br-
D.1.0?mol?L-1的KNO3溶液:H+、Fe2+、Cl-、SO42-
参考答案:A、与铝反应产生大量氢气的溶液可能是酸溶液或碱溶液:Na+、K+、CO32-、NO3-,酸溶液中碳酸根离子不能大量存在,故A不符合;
B、甲基橙呈黄色溶液P溶液PH>4.4,溶液可能是酸、中性、碱;在酸溶液中AlO2-不能大量存在,故B不符合;
C、c(H+)=1.0×10-13mol/L溶液,依据离子积常数计算可知溶液呈碱性,C6H5O-、K+、SO42-、Br-,离子可以大量存在,故C符合;
D、1.0 mol?L-1的KNO3溶液存在硝酸根离子,H+、Fe2+、Cl-、SO42-在酸溶液中的Fe2+离子被氧化,不能存在,故D不符合;
故选C.
本题解析:
本题难度:简单
4、选择题 下列说法正确的是
A.中和等体积、等物质的量浓度盐酸和醋酸溶液,盐酸所需NaOH溶液多于醋酸
B.常温下,20 LpH=12的Na2CO3溶液中含有的OH-离子数为0.2NA
C.向0.1 mol/LCH3COOH溶液中加入少量CH3COONa固 体,溶液中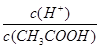 增大
增大
D.一定温度下,10mL 0.50mol・L―1 NH4Cl溶液与20mL 0.25mol・L―1 NH4C1溶液含NH4+物质的量相同
参考答案:B
本题解析:A、由c?V可知n(HCl)=n(CH3COOH),故中和 NaOH能力相同,错误;B、常温下,c(OH―)=Kw/10―pH=0.01mol/L,由c?V可知n(OH―)=0.2mol,由n?NA可知,N(OH―)=0.2NA,正确;C、增大c(CH3COO―),CH3COOH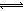 CH3COO―+H+的电离平衡左移,c(H+)减小,n(CH3COOH)增大,则
CH3COO―+H+的电离平衡左移,c(H+)减小,n(CH3COOH)增大,则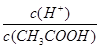 减小,但电离平衡常数Ka=
减小,但电离平衡常数Ka=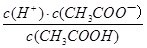 不变,错误;D、由c?V可知n(NH4Cl)均为0.005mol,但是NH4Cl是盐,NH4+能部分水解,且越稀越水解,则前者所含n(NH4+)略小于后者,错误。
不变,错误;D、由c?V可知n(NH4Cl)均为0.005mol,但是NH4Cl是盐,NH4+能部分水解,且越稀越水解,则前者所含n(NH4+)略小于后者,错误。
本题难度:一般
5、选择题 下列各组离子在指定溶液中一定能大量共存的是
A.水电离的c(H+)=1×10-13mol/L的溶液中:Na+、Ba2+、Cl―、NO3―
B.使酚酞变红色的溶液:Na+、Cu2+、HCO3-、NO3-
C.在酸性条件下:Fe2+、Cl-、NO3-、K+
D.在无色溶液中:Al3+、Cl-、 K+、AlO2-
参考答案:A
本题解析:B项溶液为碱性,Cu2+、HCO3不能与OH-共存,错误;C项在酸性条件下,Fe2+和NO3-因反应氧化还原反应而不能大量共存,错误;D项Al3+与AlO2-因发生双水解而不能大量共存,错误。
本题难度:一般