1、选择题 在一定条件下,氯酸钾与碘发生反应:2KClO3+I2====2KIO3+Cl2↑。由此可以推断下列相应的结论不正确的是(? )
A.该反应属于置换反应
B.还原性:I2>Cl2
C.非金属性:I2>Cl2
D.氧化性:KClO3>I2
参考答案:C
本题解析:这是学生比较陌生的一个化学反应,表面上看似乎是I2置换出Cl2。I2的氧化性强于Cl2,但仔细分析,可发现碘是失电子的,在化学反应中作还原剂,即氧化性:KClO3>I2。根据同一反应中强氧化剂与强还原剂生成弱还原剂和弱氧化剂的反应规律,可知还原性:I2>Cl2。再根据置换反应的概念,A项叙述正确。C项非金属性的概念是相对于元素而言,而不是具体的物质,故C项错误。
本题难度:简单
2、选择题 下列不能用来区别二氧化硫 和二氧化碳两种气体的试剂是
和二氧化碳两种气体的试剂是
A 澄清的石灰水 B 酸性高锰酸钾溶液 C 溴水 D 品红溶液
参考答案:A
本题解析:略
本题难度:简单
3、选择题 关于非金属元素O、N、S、Cl的叙述,正确的是
A.在通常情况下,其单质均为气体
B.非金属性按O、N、S、Cl顺序依次递减
C.每种元素只能形成一种氢化物
D.都属于主族元素
参考答案:D
本题解析:A:硫在常温下为固态,不正确
B:氯的非金属性强于硫,排除
C:氮元素的氢化物有多种,例如NH3、N2H2、HN3等,排除
D:正确
本题难度:简单
4、实验题 下图是一个制取氯气并以氯气为原料进行特定反应的装置:
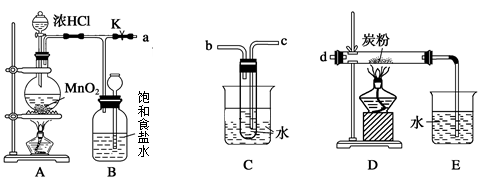
(几种气体的溶解度:常温常压下,1体积水可溶解CO2、Cl2、HCl分别为1、2、500体积)
(1)A是氯气发生装置,其中的离子反应方程式为?;
(2)要将C装置接入B和D之间,正确的接法是a→______,______ →d。
(3)实验开始时,先点燃A处的酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃D处酒精灯,连接上E装置。Cl2通过C瓶后再进入D。D装置的硬质玻璃管内盛有炭粉,发生氧化还原反应,其产物为两种气体,且体积比为1∶4。试写出D中发生反应的化学方程式?,装置C的作用是?;为了使C装置发挥更好的作用,可向烧杯中加入浓硫酸,加入浓硫酸的作用是
?。
(4)在A、B、C、D、E装置中有一处需要改进,说明需要改进的理由并画出改进后的
装置图?。
(5)D处反应完毕后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有Cl2产生,此时B中的现象是?。
参考答案:
(1)4H++2Cl-+MnO2 ="==" Mn2++2H2O+Cl2↑
(2)c? b(1分)
(3)2Cl2+2H2O(g)+C ="==" 4HCl +CO2
吸收Cl2中的HCl气体,提供D处所需水蒸气;
浓硫酸稀释时放出大量的热,促进试管里的水蒸发,减少氯气的溶解。(1分)
(4)尾气的吸收需要改进,否则容易出现因为HCl气体的极易溶解导致倒吸现象的出现;
防倒吸装置均可,图略。
(5)瓶中液面下降,长颈漏斗内液面上升。
本题解析:(2)C装置是洗气装置,应长导管进气,短导管出气。
(3)C中盛放的水,可以吸收随氯气挥发出的HCl,但同时也会有水蒸气混入Cl2中,因此和碳单质反应时,水蒸气也会参与,根据原子守恒,产生的气体只能是HCl和CO2,。根据产物的体积之比,可写出方程式。
C有提供反应所需水蒸气的作用,加入的浓硫酸在稀释时会放出大量热,可促进试管中水的蒸发,同时可减少氯气的溶解。
(4)尾气中含有易溶于水的HCl,直接通入水中易发生倒吸,因此应改为防倒吸装置。
(5)关闭K后,多余的氯气进入B中,使B中压强增大,因此B中液面下降,长颈漏斗中液面上升。
本题难度:一般
5、实验题 实验室用下列仪器和药品制取干燥纯净的氯气。
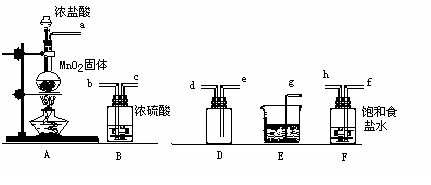
小题1:按气流从左到右,装置正确的连接顺序为(?)接(?)接(?)接(?)接(?)接(?)接(?)接(?)(填各接口字母)
小题2: 装置F的作用是??,装置E的作用是?。
小题3:装置A和E中的反应化学方程式为 :
:
小题4:某校化学兴趣小组称取8.7g二氧化锰与足量10mol/L的浓盐酸反应,理论上可制得氯气的体积(标准状况)V1 = ??L
小题5:若该小组量取了10mol/L的浓盐酸40ml,与足量的二氧化锰反应,理论上产生氯气的体积为V2(标准状况),则V1?V2(填“>”、“<”或“=”),原因是?
参考答案:
小题1:(? a?)( f?)( h?)(? b?)( c?)(? e?)( d?)( g?)
小题2:?除掉氯气中混有的氯化氢?,?吸收多余的氯气?。
小题3: ?A :MnO2+4HCl(浓)
?A :MnO2+4HCl(浓)  ?MnCl2+Cl2↑+2H2O? E: Cl2+2NaOH=NaCl+NaClO+H2O 。
?MnCl2+Cl2↑+2H2O? E: Cl2+2NaOH=NaCl+NaClO+H2O 。
小题4:2.24 L
小题5:>?原因是随着反应进行,盐酸浓度减小,稀盐酸不与二氧化锰反应
本题解析:实验室制取氯气的药品是浓盐酸和二氧化锰,由于浓盐酸具有挥发性,所以氯气中会混入氯化氢,所以在收集之前需要除去氯化氢,利用饱和食盐水来除氯化氢。因为需要高燥的氯气,因此还要通过浓硫酸进行干燥,然后才能收集。因为氯气的密度大于空气的,所以可通过向上排气法进行收集。氯气有毒,最好需要进行尾气处理,以防止污染空气。吸收多于的氯气可用氢氧化钠溶液。根据反应MnO2+4HCl(浓)  ?MnCl2+Cl2↑+2H2O可知,每消耗87g二氧化锰,就可以生成22.4L标准状况下的氯气,所以8.7g二氧化锰可生成2.24L氯气。40ml 10mol/L的浓盐酸的物质的量是0.4mol,根据反应式可知理论上应该生成0.1mol氯气。但由于在反应过程中盐酸的浓度逐渐降低,当降低到一定程度时,二氧化锰就不能再氧化盐酸,所以实际生成的氯气体积要小于0.1mol。
?MnCl2+Cl2↑+2H2O可知,每消耗87g二氧化锰,就可以生成22.4L标准状况下的氯气,所以8.7g二氧化锰可生成2.24L氯气。40ml 10mol/L的浓盐酸的物质的量是0.4mol,根据反应式可知理论上应该生成0.1mol氯气。但由于在反应过程中盐酸的浓度逐渐降低,当降低到一定程度时,二氧化锰就不能再氧化盐酸,所以实际生成的氯气体积要小于0.1mol。
本题难度:一般