1、填空题 (11分)下图是一个化学过程的示意图。

(1)请回答图中甲池是______装置,其中OH-移向________极(填“CH3OH”或“O2”)
(2)写出通入CH3OH的电极的电极反应式_________。
(3)向乙池两电极附近滴加适量紫色石蕊试液,附近变红的电极为_________极(填“A”或“B”),并写出此电极反应的电极反应式____________。
(4)乙池中反应的离子方程式为____________。
(5)当乙池中B(Ag)极的质量增加5.40g时,乙池的pH是________(若此时乙池中溶液的体积为500mL);此时丙池某电极析出1.60g某金属,则丙中的某盐溶液可能是_______(填序号).
A.MgSO4
B.CuSO4
C.NaCl
D.AgNO3
参考答案:(1) 原电池? CH3OH?
(2)? CH3OH-6e-+8OH-=== CO32-+6H2O?
(3)? A? 4OH--4e-=== O2↑+2H2O?
(4)4Ag+ + 2H2O =" 4Ag" + O2↑ + 4H+
(5)? 1? BD
本题解析:(1)燃料电池是化学能转变为电能的装置,属于原电池,燃料电池中,投放燃料的电极是负极,投放氧化剂的电极是正极,原电池放电时,电解质溶液中氢氧根离子向负极移动,即向投放甲醇的电极移动,故答案为:原电池;CH3OH;
(2)该燃料电池中,甲醇失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为:CH3OH-6e-+8OH-=CO32-+6H2O;
(3)乙池有外接电源属于电解池,连接原电池正极的A是阳极,连接原电池负极的B是阴极,电解硝酸银溶液时,A电极上氢氧根离子放电导致电极附近氢离子浓度大于氢氧根离子浓度,溶液呈酸性,加热紫色石蕊试液呈红色,电极反应式为4OH--4e-=O2↑+2H2O;
(4)电解硝酸银溶液时,银离子得电子生成银、水失电子生成氧气和氢离子,离子方程式为4Ag++2H2O=4Ag+O2↑+4H+;
(5)当乙池中B(Ag)极的质量增加5.40g时,设氢离子浓度为xmol/L,
4Ag++2H2O=4Ag+O2↑+4H+;
432? 4mol
5.40g? 0.5xmol
x=0.1,则溶液的pH=1;
阴极上析出金属,则在金属活动性顺序表中金属元素处于H元素后,根据串联电池中转移电子数相等知,丙中析出金属元素需要的电子等于或小于乙池中转移电子数,据此确定含有的金属元素,析出5.40g时转移电子是0.05mol,
A、硫酸镁中镁元素处于H元素前,所以阴极上不析出金属单质,故错误;
B、电解硫酸铜溶液时,阴极上析出1.60g铜需要转移电子0.05mol,故正确;
C、氯化钠中钠元素处于氢元素前,所以阴极上不析出金属单质,故错误;
D、电解硝酸银溶液时,阴极上析出1.60g银需要转移电子0.0148mol<0.05mol,故正确;
故选BD。
本题难度:一般
2、选择题 下列叙述中,可以说明金属甲的活动性比金属乙的活动性强的是
[? ]
A.在氧化还原反应中,甲原子失去的电子比乙原子失去的电子多
B.同价态的阳离子,甲比乙的氧化性强
C.甲能跟稀盐酸反应放出氢气而乙不能
D.将甲、乙作电极组成原电池时,甲是正极
参考答案:C
本题解析:
本题难度:一般
3、选择题 由A、B、C、D四种金属按表中装置进行实验,下列叙述中正确的是( )
实验装置与现象
|
装置
甲
乙
丙
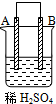

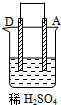
现象
二价金属A不断溶解
C的质量增加
A上有气体产生
|
A.装置甲中的B金属是原电池的负极
B.装置乙中的C金属是原电池的阴极
C.装置丙中的D金属是原电池的正极
D.四种金属的活泼性顺序是D>A>B>C
参考答案:A、原电池中负极金属失电子,金属质量减轻,所以A是负极,故A错误;
B、原电池的两个电极名称是正极和负极,电解池的两个电极名称是阴极和阳极,金属质量增加的极即C极为正极,故B错误;
C、在原电池中,只有正极才会产生气体,所以丙中的A金属是原电池的正极,故C错误;
D、原电池的负极金属活泼性强于正极金属,所以各个装置金属的活泼性:A>B,B>C,D>A,即D>A>B>C,故D正确.
故选D.
本题解析:
本题难度:简单
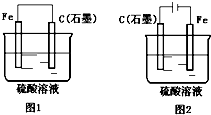
4、选择题 如图是化学能与电能相互转换的两套装置,对此两套装置的分析正确的是( )
A.两装置中,铁电极上均有较大量气体产生
B.图2装置中铁片上发生氧化反应
C.石墨电极上发生的电极反应均为:2H++2e-=H2↑
D.随着反应的进行,图1中溶液的pH增大,图2中溶液的pH减小