1、填空题 不同元素的气态原子失去最外层一个电子所需要的能量(设其为E)如图所示。试根据元素在周期表中的位置,分析图中曲线的变化特点,并回答下列问题。

(1)同主族内不同元素的E值变化的特点是____________________。各主族中E值的这种变化特点体现了元素性质的____________变化规律。
(2)同周期内,随原子序数增大,E值增大。但个别元素的E值出现反常现象。试预测下列关系中正确的是
____(填写编号)
①E(砷)>E(硒) ②E(砷)<E(硒) ③E(溴)>E(硒) ④E(溴)<E(硒)
(3)估计1mol气态Ca原子失去最外层一个电子所需能量E值的范围____<E<____。
(4)10号元素E值较大的原因__________。
参考答案:(1)随着原子序数的增大,E值变小;周期性
(2)①③
(3)419;738
(4)10号元素是氖,其最外层电子的排布已达8电子稳定结构
本题解析:
本题难度:一般
2、填空题 图表法、图象法是常用的科学研究方法.
(Ⅰ)电离能是指由蒸气状态的孤立原子失去电子形成阳离子需要的能量.从中性原子中移去第一个电子所需要的能量为第一电离能(I1),移去第二个电子所需要的能量为第二电离能(I2),依次类推.
现有5种元素L、M、N、O、P,其I1~I3分别如下表,根据表中数据判断其中的金属元素有______,稀有气体元素是______,最活泼的金属是______,显二价的金属是______.
| 元?素 | I1/eV | I2/eV | I3/eV
L
13.0
23.9
40.0
M
4.3
31.9
47.8
N
5.7
47.4
71.8
O
7.7
15.1
80.3
P
21.6
41.1
65.2
|
(Ⅱ)某温度时,在一个5L的密闭容器中,M、P、Q三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:
(1)该反应的化学方程式为______
(2)若M、P、Q均为气体,反应达平衡时:
①体系的压强是开始时的______倍;从反应开始到平衡气体M的平均反应速率为______
②若此时只将容器的体积扩大为原来的2倍,达新平衡时,容器内温度将降低(容器不与外界进行热交换),则该反应为______反应(填“放热”或“吸热”);达新平衡时,容器内混合气体的平均分子量比原平衡时______(填增大、减小或相等).
(3)此反应达平衡后,若只加大体系压强,M的物质的量增加,若M是气体,则Q的聚集状态是______.
参考答案:I.由题意知,电离能越小,失电子越容易,该元素金属性越强,因为 M、N、O的电离能较小,所以 M、N、O是金属;P的第一、第二、第三电离能都比较大,所以是稀有气体;第一电离能最小的是?M,所以其金属性最强;O元素的第一电离能和第二电离能差比第三电离能和第二电离能的差小很多,所以显二价的金属是O.
故答案为:M、N、O; P;?M;?O.
II.(1)反应平衡前后P、Q的物质的量减少,M的物质的量增加,所以P、Q是反应物,M是生成物;
减少或增加的物质的量为参加反应的物质的量,P参加反应的物质的量为(0.8-0.6)=0.2mol,Q参加反应的物质的量为(0.8-0.5)mol=0.3mol,M参加反应的物质的量为(0.2-0)mol=0.2mol,同一反应中参加反应的各物质的物质的量之比等于其计量数之比,所以P、Q、M的计量数之比为2:3:2.
故答案为:2P+3Q?2M?
(2)①在温度、容器的容积不变的条件下,体系中混合气体的物质的量与其压强成正比,反应前混合气体的物质的量为(0.8+0.8)mol=1.6mol,平衡后混合气体的物质的量为:(0.6+0.5+0.2)mol=1.3mol,所以体系的压强是开始时的1316.
v(M)=△nV△t=0.2mol5L2min=0.02?mol/L?min.
故答案为:1316;? 0.02?mol/L?min.
②增大体积,容器内压强减小,减小压强,平衡向逆反应方向移动,温度降低,说明逆反应吸热,所以正反应放热;
达新平衡时,混合气体的物质的量增大,混合物的质量不变,所以其平均摩尔质量减小,即相对分子质量减小.
故答案为:放热;减小.
(3)若只加大体系压强,M的物质的量增加,说明平衡向正反应方向移动,即生成物的气体计量数小于反应物的,如
M是气体,那么Q的聚集状态一定是气态.
故答案为:气态.
本题解析:
本题难度:一般
3、选择题 下列图示中横坐标是表示元素的电负性数值,纵坐标表示同一主族的五种元素的序数的是( )
A.
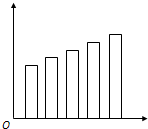
B.
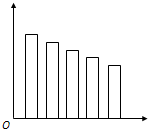
C.
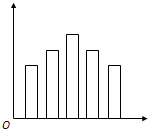
D.
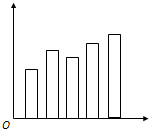
参考答案:B
本题解析:
本题难度:一般
4、选择题 下列说法正确的是
[? ]
A.第一电离能大的原子一定不能发生化学反应
B.X、Y位于同周期,X电负性大于Y电负性则X的第一电离能一定大于Y第一电离能
C.在所有元素中,氦的第一电离能最大
D.元素的电负性越大则元素的非金属性越弱
参考答案:C
本题解析:
本题难度:一般
5、简答题 思思同学在总结“构造原理、能量最低原理、泡利原理、洪特规则”后得出了:“在同一原子里,没有运动状态完全相同的电子存在”的结论。你认为此结论是否正确,请说明理由。
参考答案:正确。因为不同能层、不同能级、不同轨道上的电子运动状态不同,在同一轨道上运动的两个电子,因自旋方向相反,其电子运动状态也不相同
本题解析:
本题难度:一般