1、选择题 已知:Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16 ,Ksp(Ag2CrO4)=2.0×10-12,则下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是
A.AgCl>AgI> Ag2CrO4
B.Ag2CrO4>AgCl>AgI
C.AgCl> Ag2CrO4>AgI
D.Ag2CrO4>AgI>AgCl
参考答案:B
本题解析:试题分析:根据对应化学式相似的AgCl和AgI来说Ksp越小Ag+浓度越小,即AgCl>AgI;假设Ag2CrO4饱和溶液中Ag+的浓度为x,则CrO42-的浓度为0.5x,由溶度积常数的表达式可知Ksp(Ag2CrO4)=x2×0.5x=0.5x3=2.0×10-12,x3=4.0×10-12,即X=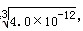 所以Ag2CrO4>AgCl,
所以Ag2CrO4>AgCl,
故顺序为:Ag2CrO4>AgCl>AgI.
考点:溶度积常数
点评:本题主要考查溶度积常数的概念和有关计算,做题时注意不同物质的化学式是否相似,如不同,可用溶度积常数计算
本题难度:一般
2、选择题 向3mo l ・ L-1的NaOH溶液100mL中缓缓地通入4.48L(标准状况)二氧化碳气体,充分反应后,溶液中离子浓度由大到小排列顺序正确的是
A.c(Na+) > c(CO32-) > c(HCO3-) > c(OH-) > c(H+)
B.c(Na+) > c(CO32-) = c(HCO3-) > c(OH-) > c(H+)
C.c(Na+) > c(HCO3-) >c(OH-) > c(CO32-) > c(H+)
D.c(Na+) > c(HCO3-) > c(CO32-) >c(OH-) > c(H+)
参考答案:D
本题解析:n(NaOH)=0.3mol ,n(CO2)=0.2mol ,二者发生化学反应后生成Na2CO3和NaHCO3 .n(Na2CO3)=n(NaHCO3)=0.1mol,转化 为等浓度的Na2CO3和NaHCO3的混合器溶液.故c(Na+) > c(HCO3-) > c(CO32-) >c(OH-) > c(H+)选(D)项
本题难度:困难
3、选择题 下列有关物质的用途(括号内为用途),错误的是.
A.晶体硅(半导体材料)
B.二氧化硅(制光导纤维)
C.水玻璃(用作黏合剂)
D.单质硅(作耐火材料)
参考答案:D
本题解析:单质硅的熔点比SiO2低(或使用排除法).
本题难度:一般
4、选择题 在0.1 mo l ・ L-1 Na2CO3溶液中, 下列关系式正确的是
A.c(Na+)=2c(CO32-)
B.c(OH-)=c(H+)+c(HCO3-)+c(H2CO3)
C.c(HCO3-)>c(H2CO3)
D.c(Na+)
参考答案:C
本题解析:由于CO32-水解,故c(Na+)>2c(CO32-),CO32-水解以第一步为主,故c(HCO3-)>c(H2CO3)由水电离产生的c(H+)与水电离产生的c(OH-)相等,而部分H+被结合生成HCO3― 和H2CO3故c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3),由物料守恒有c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3)综上分析选(C)项。
本题难度:简单
5、选择题 若要区别硫酸铜溶液和氢氧化铁胶体,最简单的方法是
A.观察外观
B.丁达尔效应
C.过滤
D.加热
参考答案:A
本题解析:正确解法:本题易错选B选项,究其原因是忽视题目中“最简单”的要求.硫酸铜溶液和氢氧化铁胶体具有不同的颜色,不必用丁达尔效应,仅从外观上就可以区分二者.
点评:溶液和胶体是两种不同的分散系,它们的性质差异是前者没有丁达尔效应,后者有丁达尔效应,因此,常利用丁达尔效应区别二者,但也要注意题目的要求从而合理选择.
本题难度:简单