1��ѡ���� �������ӷ���ʽ��д��ȷ����
A��Ba(OH)2��Һ�������NaHCO3��Һ��� Ba2++2OH-+2HCO3- BaCO3��+CO32-+H2O
BaCO3��+CO32-+H2O
B�����������Һ��ͨ������SO2���壺Ca2++2ClO��+SO2+H2O CaSO3��+2HClO
CaSO3��+2HClO
C����������ˮ��Ӧ 2K +2 H2O 2K+ +2 OH��+ H2��
2K+ +2 OH��+ H2��
D������������������Һ�ķ�Ӧ H+ + OH�� H2O
H2O
�ο��𰸣�C
���������
��ȷ�𰸣�C
A��Ba2++OH-+HCO3- BaCO3��H2O ;B��Ca2++2ClO��+SO2+H2O
BaCO3��H2O ;B��Ca2++2ClO��+SO2+H2O CaSO4��+HClO��H�� ��Cl�D?D��CH3COOH + OH��
CaSO4��+HClO��H�� ��Cl�D?D��CH3COOH + OH�� H2O��CH3COO�D
H2O��CH3COO�D
�����Ѷȣ���
2�������
��1��ͨ����С�մ������Һ��ȥCO2�е�HCl����Ӧ�����ӷ���ʽΪ��?��
������NaOH��Һ��ԭ����?��Ҳ������Na2CO3��ԭ����?���������ӷ���ʽ��ʾԭ��
��2��.���������ӷ���ʽ��д�ɻ�ѧ����ʽ��
CO32- + 2H+? =? CO2�� +? H2O?
Ag+? +? Cl-=? AgCl��??
�ο��𰸣���8�֣���1��HCO3- +H+ = H2O+CO2����CO2+2OH- = H2O+CO32- ��H2O+CO32- +CO2=2HCO3-[
(2)Na2CO3+2HCl===NaCl+CO2��+H2O��AgNO3+NaCl===AgCl+NaNO3(�𰸲�Ψһ��ÿ��2��)
���������ͨ����С�մ������Һ��ȥCO2�е�HCl����Ӧ�����ӷ���ʽΪHCO3- +H+ = H2O+CO2����������NaOH��Һ��ԭ����CO2+2OH- = H2O+CO32-��Ҳ������Na2CO3��ԭ����H2O+CO32- +CO2=2HCO3-
��2��CO32- + 2H+===CO2�� + H2O��ʾ������̼������ǿ�ᷴӦ��Ag+ + Cl-===AgCl����ʾ����������(AgNO3)������������εķ�Ӧ����
�����Ѷȣ�һ��
3��ѡ���� ����ȷ��ʾ���з�Ӧ�����ӷ���ʽ��
A��������������ͨ����������Һ�У�H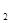 S+2Fe
S+2Fe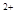 =2Fe
=2Fe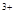 +S��+2H
+S��+2H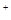
B����������ϡ���ᷴӦ��3Fe+8H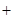 +2NO
+2NO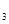
 =3Fe
=3Fe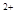 +4H
+4H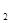 O+2NO��
O+2NO��
C����AlCl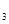 ��Һ�е��������ˮ��Al
��Һ�е��������ˮ��Al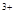 +4NH
+4NH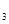 H
H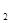 O=AlO
O=AlO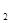
 +4NH
+4NH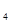
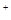 +2H
+2H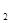 O
O
D�������ʵ�����Ba(OH)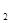 ��NaHSO
��NaHSO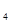 ����Һ�з�Ӧ��Ba
����Һ�з�Ӧ��Ba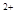 +OH
+OH +HSO
+HSO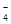 =BaSO
=BaSO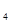 ��+H
��+H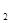 O
O
�ο��𰸣�D
���������A���ɲ��غ㣬B������������Ӧ��ӦΪFe3+��C�ˮ��������ܸ�Al(OH)3��Ӧ����ѡD��
���������ӷ���ʽ�����ж�Ҫע�⣺���Ƿ���Ͽ���ʵ�����Ƿ���������غ㡢���Ƿ���ϵ���غ㡢���Ƿ���ϵ�ʧ������ȡ����ܵ���������ʲ�����ӡ�ע������������������ȡ�
�����Ѷȣ�һ��
4������� ij��ɫ��Һ��Na+��Ag+��Ba2+��Al3+��Fe3+��AlO2-��MnO4-��CO2-3��SO42-�е���������ɣ�ȡ����Һ��������ʵ�飺
��A��ȡ��Һ�������������ϡ���ᣬ���������ɣ��õ���Һ�ף�
��B������Һ�����ټ������̼�������Һ�����������ɣ�������ɫ�����ң��õ���Һ����
��C������Һ���м������Ba��OH��2��Һ�����������ɣ�������ɫ��������
��������ʵ��ش��������⣺
��1����Һ��һ�������ڵ�������______��
��2��һ�����ڵ�������______��
��3�����ɳ����ҵ����ӷ�Ӧ����ʽ��______��
�ο��𰸣���1��ȡ��Һ�������������ϡ���ᣬ���������ɣ�����Һ�к�������CO32-����һ������Ag+��Ba2+��Al3+��
Fe3+����Щ������CO32-���ӷ�Ӧ���ɳ��������ܴ������棬������Һ�ĵ����ԣ���Һ��һ������Na+���ӣ�
��Һ��ɫ����MnO4-���ʴ�Ϊ��Ag+��Ba2+��Al3+��Fe3+��MnO4-��
��2�����ݣ�1���ķ����ͽ����Һ�к���CO32-��Na+���ӣ���Һ�׳����ԣ��ټ������̼�������Һ�����������ɣ�������ɫ������Ӧ�Ƿ�����Al3++3HCO3-=Al��OH��3��+3CO2��������Ӧ����Al3+���ӣ���ԭ��Һ��Ӧ����AlO2-���ӣ��ʴ�Ϊ��Na+��AlO2-��CO32-��
��3��Al3+����ˮ������ԣ�HCO3-����ˮ��ʼ��ԣ����߷�����ٽ���ˮ������Al��OH��3������CO2���壬��Ӧ�ķ���ʽΪAl3++3HCO3-=Al��OH��3��+3CO2�����ʴ�Ϊ��Al3++3HCO3-=Al��OH��3��+3CO2����
���������
�����Ѷȣ�һ��
5��ѡ���� �������ӷ���ʽ�У���ȷ��
A����AlCl3��Һ�м��������ˮ��Al3+ + 3NH3��H2O =Al(OH)3�� + 3NH4+
B������ʯ������������У�CO32-��2H��= CO2����H2O
C��ϡ�����Ba(OH)2��Һ��Ӧ��Ba2����OH����H����SO42-=BaSO4����H2O
D����CuSO4��Һ�м���Ba(OH)2��Һ��Ba2+ + SO42- =BaSO4��
�ο��𰸣�A
���������A����ˮ��������ܽ�����������A��ȷ��B������ʯ�����������ʣ�Ӧ���û�ѧʽ��ʾ��B����ȷ��C�������϶�����ɣ�Ӧ����Ba2����2OH����2H����SO42-��BaSO4����2H2O��C����ȷ��D����Ӧ�л���������ͭ��ɫ�������ɣ�D����ȷ����ѡA���Ȼ��������������ʣ�Ӧ���л�ѧʽ��ʾ��A����ȷ��B��ȷ��C���������Ʋ��㣬�����������Ⱥ������ӷ�Ӧ��C����ȷ��D�е�ɲ��غ㣬����ȷ����ѡB��
�����������Ǹ߿��еĸ�Ƶ�⣬�����е��Ѷȵ����⣬���ض�ѧ��������������ѵ����������Ҫ��ȷ�ж����ӷ���ʽ��ȷ���ķ���һ�㣬����1����鷴Ӧ�ܷ�������2����鷴Ӧ��������Ƿ���ȷ����3���������ʲ���Ƿ���ȷ����4������Ƿ�����غ��ϵ���磺�����غ�͵���غ�ȣ�����5������Ƿ����ԭ��ѧ����ʽ��Ȼ��������ü��ɡ���������������ѧ���������⡢��������������
�����Ѷȣ�һ��