|
�߿���ѧ֪ʶ���ܽᡶ���ӷ�Ӧ�����⼼�ɣ�2019�����°棩(��)
2020-07-08 01:31:10
�� �� �� ��
|
1������� ��15�֣�ij����Һ������Fe2+��Fe3+��Ag+��Ba2+��Al3+��Ca2+��NH4+�����ӣ�����������ʵ�飨�����ᡢ�NH3ˮ��Br2ˮ���ǹ����ģ���

����ʵ������
��1���ж�����Һ������Ba2+��Ca2+���ӣ���д�����ɡ���_________��
��2��д����ѧʽ������A_________������D_________������E_________��
��3��д���������ӷ�Ӧ����ʽ��
��ˮ������ҺA�е�ij���ӣ�_________��
����C��������NaOH��Һ������һ�ֳ����ܽ⣺_________��
�ο��𰸣���1������Ba2+��Ca2+�����е�һ�ֻ����֣���ΪBaSO4������ˮ��CaSO4����ˮ��2�� A��AgCl��? D��Fe��OH��3��? E ��Al��OH��3
��3�� 2Fe2++Br2=2Fe3++2Br-?��Al��OH��3+OH��=AlO2��+2H2O
�������������A���ж�ΪAgCl������Ag+�Ѵ���Һ�г�������ҺA������Fe2+�ѱ���ˮ����ΪFe3+������BaSO4������ˮ��CaSO4����ˮ�����жϳ���B�����Ƕ���֮һ��Ҳ���������ǵĻ���Al��OH��3��Fe��OH��3��������ˮ������C�����Ƕ���֮һ���������ǵĻ���������C����Al��OH��3���������NaOH��Һ������NaAlO2������ҺD���ù���NaOH��Һ����C����ʣ�����D�����жϳ���D��Fe��OH��3��HAlO2�DZ�H2CO3�������ᣬCO2�������׳���֮��������HCO3����Al��OH��3���dz���E��
AlO2��+CO2+2H2O=Al��OH��3��+HCO3��
�����Ѷȣ�һ��
2��ѡ���� ����1 mol HCl��1 mol MgSO4�Ļ����Һ�м���1 mol/L Ba(OH)2��Һ������ͼ������ȷ��ʾ�������������ʵ���(n)�����Ba(OH)2��Һ�����(V)֮���ϵ����(����)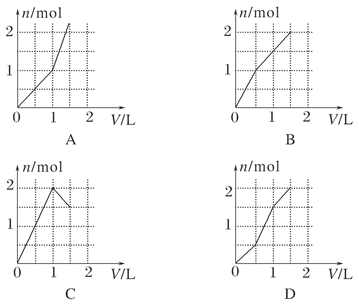
�ο��𰸣�D
�������������Ba(OH)2���ᷢ��H����OH��===H2O��Ba2����SO42��===BaSO4����Mg2����2OH��===Mg(OH)2����������0.5 mol Ba(OH)2ʱ����������ٵ��������BaSO4����������Mg(OH)2������������Ba(OH)2 1 molʱSO42��������ȫ������1.5 mol Ba(OH)2ʱ��Mg2���ֳ�����ȫ����ѡD��
�����Ѷȣ�һ��
3������� (14��)����п�������ᡢ�´ɡ����¡�ҽҩ�����ӡ���ѧ�ȹ�ҵ����Ҫԭ�ϡ�����
��п��ƷΪԭ���Ʊ���������п�����������������£�

��1��.��������õ���������Һ�к���Zn2����SO42����������Fe2����Cu2���� ����Mn2���� ����Mn2����
���ʡ�����A�������ǵ�����Һ��pH��5 4������A���ѡ��________��
A��NH3.H2O
B��Na2CO3
C��H2SO4
D��ZnO
| ��֪25��ʱ���ֽ������Ӵӿ�ʼ�γ��������������������ȫʱ��Һ��pH���±���
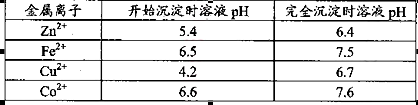
���¶���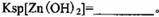 �� ��
��2�� KMnO4�������dz�ȥMn2����Fe2������KMnO4��Mn2����Ӧ�����ӷ���ʽΪ_____________________________________������Һ�� ������1 ������1 ����Һ��Fe2�������ĵ�KMnO4������Ϊ________g��������λ��Ч���֣��� ����Һ��Fe2�������ĵ�KMnO4������Ϊ________g��������λ��Ч���֣���
��3������Cu2����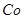 2���������û���Ӧ��ȥ��������B��_________�� 2���������û���Ӧ��ȥ��������B��_________��
��4�������յij����� �����ɸó����Ļ�ѧ����ʽΪ________�� �����ɸó����Ļ�ѧ����ʽΪ________��
��μ���ó����Ƿ�ϴ����________________________________��
�ο��𰸣���ÿ��2�֣���14�֣�
��1��? D? ; 1.0��10-20.2
��2��2MnO4�D+3Mn2+ + 2H2O = MnO2+ 4H+?��? 26.33
��3���
��4��3ZnSO4 + 5NH3��H2O?+ NH4HCO3 = ZnCO3��2Zn(OH)2��H2O�� + 3 (NH4)2SO4��
�����һ�ε�ϴ��Һ�е���1��2��BaCl2��Һ���������Ե������������ϴ����
�����������1�������̵�Ŀ�����Ʊ�����п������Ϊ�˲������µ����ʣ���Ҫѡ������п ������Һ��pHֵ����ѡD��Zn(OH)2��ȫ����ʱc(Zn2+)=1��10-5mol/L��c��OH-��=1��10-14/1��10-6.4=1��10-7.6mol/L�����Ը��¶���Zn(OH)2��Ksp= c��OH-��2��c(Zn2+)=1.0��10-20.2
��2����������ͼ��֪�����������غ��ж������̳������֣�����KMnO4��Mn2����Ӧ���ɶ������̣����ӷ���ʽΪ2MnO4�D+3Mn2+ + 2H2O = MnO2+ 4H+?�����ݵ�ʧ�����غ���ɣ�����MnO4-��3Fe2+,1m3�ĸ���Һ��n(Fe2+)=0.5mol������ҪKMnO4������Ϊ0.5mol/3��158g/mol=26.33g��
��3������Cu2����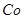 2���������û���Ӧ��ȥ��ͬ����Ϊ�˲��������µ����ʣ�BӦ��п�ۣ� 2���������û���Ӧ��ȥ��ͬ����Ϊ�˲��������µ����ʣ�BӦ��п�ۣ�
��4������ZnCO3��2Zn(OH)2��H2OӦ���ڼ���̼������백ˮ������ģ���Һ�е�����п��֮��Ӧ���ɵij��������Ի�ѧ����ʽΪ3ZnSO4 + 5NH3��H2O?+ NH4HCO3 = ZnCO3��2Zn(OH)2��H2O�� + 3 (NH4)2SO4�� �ó����л����ܺ�����������ӣ����Լ���ϴ���Ƿ�ɾ��ķ������Ǽ�������������Ƿ���ڣ��������Ϊ�����һ�ε�ϴ��Һ�е���1��2��BaCl2��Һ���������Ե������������ϴ����
�����Ѷȣ�һ��
4������� ijǿ������ҺX����Ba2+��Al3+��N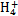 ��Fe2+��Fe3+��C ��Fe2+��Fe3+��C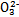 ��S ��S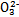 ��S ��S ��Cl-��N ��Cl-��N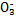 �е�һ�ֻ���,ȡ����Һ����ʵ��,ʵ����������: �е�һ�ֻ���,ȡ����Һ����ʵ��,ʵ����������:
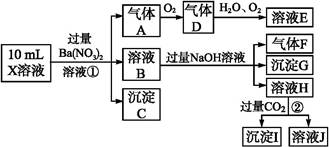
����������Ϣ,�ش���������:
(1)��ҺX�г�H+��϶����е�������������;����ȷ���Ƿ��е�������������,��Ҫȷ�����������ӵĴ���,��ɿ��Ļ�ѧ����������������������������?
(2)����G�Ļ�ѧʽΪ��������?
(3)д���й����ӷ���ʽ:
�����������A��������������������?
��������ɳ���I��������������������?
(4)����ⶨA��F��I��Ϊ0.01 mol,10 mL X��Һ��n(H+)="0.04" mol,������C���ʵ���0.07 mol,��˵��(1)�в���ȷ���������Ӵ��ڵ�����������������������������?
�ο��𰸣�(1)Al3+��N ��Fe2+��S ��Fe2+��S ��Cl-��Fe3+��ȡ����X��Һ�����Թ���,���뼸��KSCN��Һ,��Һ�����ɫ˵����Fe3+,�������˵����Fe3+(û��ȡ����ȡ���۷�) ��Cl-��Fe3+��ȡ����X��Һ�����Թ���,���뼸��KSCN��Һ,��Һ�����ɫ˵����Fe3+,�������˵����Fe3+(û��ȡ����ȡ���۷�)
(2)Fe(OH)3
(3)3Fe2++N +4H+ +4H+ 3Fe3++NO��+2H2O��Al 3Fe3++NO��+2H2O��Al +CO2+2H2O +CO2+2H2O Al(OH)3��+HC Al(OH)3��+HC
(4)������Fe3+�϶�����ʱ,����Cl-����,��Ϊ�϶����ڵ����ӵ�����������
���������ǿ������ҺXһ������C ��S ��S ;��������Һ����Ba(NO3)2��Һ����г���C����,��֪X�к���S ;��������Һ����Ba(NO3)2��Һ����г���C����,��֪X�к���S ,һ����Ba2+;��������Aֻ��ΪNO,����X�к��л�ԭ������Fe2+,��N ,һ����Ba2+;��������Aֻ��ΪNO,����X�к��л�ԭ������Fe2+,��N ;��ҺB�к��� Fe3+,����GΪFe(OH)3;������F��֪X�к���N ;��ҺB�к��� Fe3+,����GΪFe(OH)3;������F��֪X�к���N ,�ɲ���ڿ�֪X�к���Al3+;(4)n(NO)="0.01" mol��n(NH3)="0.01" mol��n[Al(OH)3]="0.01" mol��n(H+)="0.04" mol��n(BaSO4)="0.07" mol,����ԭ�Ӽ����ϼ��غ��֪��Һ�к���:n(Fe2+)="3n(NO)=0.03" mol��n(N ,�ɲ���ڿ�֪X�к���Al3+;(4)n(NO)="0.01" mol��n(NH3)="0.01" mol��n[Al(OH)3]="0.01" mol��n(H+)="0.04" mol��n(BaSO4)="0.07" mol,����ԭ�Ӽ����ϼ��غ��֪��Һ�к���:n(Fe2+)="3n(NO)=0.03" mol��n(N )="0.01" mol��n(Al3+)="0.01" mol��n(H+)="0.04" mol��n(S )="0.01" mol��n(Al3+)="0.01" mol��n(H+)="0.04" mol��n(S )="0.07" mol,���ݵ���غ�2n(Fe2+)+n(N )="0.07" mol,���ݵ���غ�2n(Fe2+)+n(N )+3n(Al3+)+n(H+)="0.14" mol=2n(S )+3n(Al3+)+n(H+)="0.14" mol=2n(S ) )
�����Ѷȣ�һ��
5��ѡ���� ���������мȲ��ܷ���ˮ�ⷴӦҲ���ܷ�����ԭ��Ӧ����
A.������
B.����
C.�Ҵ�
D.����
�ο��𰸣�C
�������������ˮ����������Ǻ��Ҵ������ܷ�����ԭ��Ӧ�����Ҵ���
�����Ѷȣ���
| 
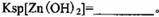 ��
�� ������1
������1 ����Һ��Fe2�������ĵ�KMnO4������Ϊ________g��������λ��Ч���֣���
����Һ��Fe2�������ĵ�KMnO4������Ϊ________g��������λ��Ч���֣��� 2���������û���Ӧ��ȥ��������B��_________��
2���������û���Ӧ��ȥ��������B��_________�� �����ɸó����Ļ�ѧ����ʽΪ________��
�����ɸó����Ļ�ѧ����ʽΪ________��