1�������� ��1��ijһ��Ӧ��ϵ�е������У�HCl��SnCl2��H2SnCl6��As��H3AsO3��H2O����֪��HCl�Ƿ�Ӧ��֮һ��
��д������ƽ�÷�Ӧ�Ļ�ѧ����ʽ��_____________________
���ڸ÷�Ӧ�У��õ��ӵ�������______________����������Ԫ����__________________��
���ڷ�Ӧ�У�ÿת��1mol���ӣ�����HCl_______________mol��
��2����2.5g̼���ơ�̼�����ƺ��������ƵĹ���������ȫ�ܽ���ˮ���Ƴ�ϡ��Һ��Ȼ�������Һ����μ���1mol��L-1�����ᣬ�������������������CO2���������״������ϵ����ͼ��ʾ��
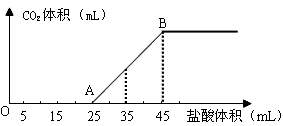
��д��OA����������Ӧ�����ӷ���ʽ______________________________________��
�ڵ�����35mL����ʱ������CO2�����Ϊ___________mL����״������
�ο��𰸣���1����12HCl+3SnCl2+2H3AsO3==3H2SnCl6+2As+6H2O����H3AsO3��+2�۵�Sn����2?
��2����H++OH-==H2O��CO32-+H+==HCO3-����224
���������
�����Ѷȣ�һ��
2������� ��Ӧ5NH4NO3=4N2+2HNO3+9H2O�б�������N�뱻��ԭ��N�ĸ�������______������ת�Ƶ�������______��
�ο��𰸣���5NH4NO3�T2HNO3+4N2��+9H2O�ķ�Ӧ�У���Ԫ����笠���-3������Ϊ0�ۣ�����������Ԫ�����������+5�۽���Ϊ0�ۣ�����ԭ���������ǻ�ԭ����Ҳ������������ݵ���ת���غ㣬��֪�������ĵ�ԭ���뱻��ԭ�ĵ�ԭ�����ʵ���֮��Ϊ��5-0����[0-��-3��]=5��3��һ����������к���һ��Nԭ�ӣ����Ա�������N�뱻��ԭ��N�ĸ�������5��3���÷�Ӧ��笠�������NԪ��ʧȥ������=5[0-��-3��]=15��
�ʴ�Ϊ��5��3��15��
���������
�����Ѷȣ�һ��
3������� ������һ�ֿ��Է�����硢�ŵ��װ�á���һ�������ڳ��ͷŵ�ʱ�����ķ�Ӧ�ǣ�
NiO2+Fe+2H2O Fe(OH)2+Ni(OH)2
Fe(OH)2+Ni(OH)2
(1)�������طŵ�ʱ���õ��ijһ�缫������ԭ��Ӧ��������________(�����)��
A��NiO2 B��Fe C��Fe(OH)2 D��Ni(OH)2
(2)�ô����طֱ�������������Һ�������·��ת����0.02 mol e-���ҵ��صĵ缫��Ϊ���Ե缫��
�Իش��������⣺
�ٵ��M(NO3)x��Һʱijһ�缫������a g M�������M�����ԭ������Ϊ____________(�ú���a��x���ı���ʽ��ʾ)��
�ڵ�⺬��0.01 mol CuSO4��0.01 mol NaCl�Ļ����Һ100 mL�����������������ڱ�״���µ������________L�����������Һ��ˮϡ����1 L����ʱ��Һ��pH��____________________��
�ο��𰸣�(1)A��
(2)��50ax����0.168��2
���������
�����Ѷȣ�һ��
4������� KMnO4��Һ��ŨHCl��Ӧ��������Cl2��2KMnO4+16HCl=2KCl+2MnCl2+5Cl2��+8H2O������71����������μӷ�Ӧ���Ȼ���Ϊ���ٿˣ����������Ȼ����Ƕ��ٿˣ�
�ο��𰸣���������71����������μӷ�Ӧ���Ȼ�������Ϊx����
2KMnO4+16HCl=2KCl+2MnCl2+5Cl2��+8H2O
? 584? 355
? x? 71?
��584x=35571�����x=116.8g�����ݷ���ʽ���Կ����������з�Ӧ�������У�������������Ͳμӷ�Ӧ�����������֮����5��8�����������Ȼ��������Ϊ116.8g��58=73g��
����μӷ�Ӧ���Ȼ���Ϊ116.8�ˣ����������Ȼ�����73�ˣ�
���������
�����Ѷȣ�һ��
5��ѡ���� P�����ڷ�Ӧ4P+3KOH+3H2O=3KH2PO2+PH3��
A.������
B.����ԭ
C.�ȱ������ֱ���ԭ
D.��δ��������δ����ԭ
�ο��𰸣�C
���������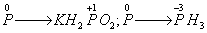 ��P�ڷ�Ӧ�л��ϼ۴�0����-3��ͬʱ��0���ߵ�+1����P���ʼȱ������ֱ���ԭ��
��P�ڷ�Ӧ�л��ϼ۴�0����-3��ͬʱ��0���ߵ�+1����P���ʼȱ������ֱ���ԭ��
�����Ѷȣ�һ��