1、计算题 (5分)石油化工是江苏省的支柱产业之一。聚氯乙烯是用途十分广泛的石油化工产品,某化工厂曾利用下列工艺生产聚氯乙烯的单体氯乙烯:
CH2==CH2+Cl2→CH2Cl―CH2Cl?①
CH2Cl―CH2Cl→CH2="=CHCl+HCl?" ?②
已知反应①中二氯乙烷的产率(产率= ×100%)为98%,反应②中氯乙烯和氯化氢的产率均为95%,则2.8 t乙烯可制得氯乙烯
×100%)为98%,反应②中氯乙烯和氯化氢的产率均为95%,则2.8 t乙烯可制得氯乙烯 __________t,同时得到副产物氯化氢__________t。(计算结果保留1位小数)
__________t,同时得到副产物氯化氢__________t。(计算结果保留1位小数)
注意 :以下二题仅选做其中一题,如果二题都做以25题为标准得分。
:以下二题仅选做其中一题,如果二题都做以25题为标准得分。
参考答案:5.8? 3.4
本题解析:略
本题难度:一般
2、选择题 下列液体中,滴入水中会出现分层现象,但在滴入热的氢氧化钠溶液中时分层现象会逐渐消失的是(不考虑有机物的挥发)
A.溴乙烷
B.乙醇
C.橄榄油
D.苯乙烯
参考答案:AC
本题解析:A、溴乙烷不溶于水,但在热的NaOH溶液会发生水解生成乙醇(易溶于水);B、乙醇与水不分层;C、橄榄油属于酯类不溶于水,与水分层,在热的NaOH作用下水解生成高级脂肪酸钠和甘油,均可溶于水;D、苯乙烯不与NaOH反应,仍分层。
本题难度:一般
3、选择题 我们所吃的豆腐是一种
A.豆浆的聚沉物
B.蛋白质
C.脂肪
D.淀粉
参考答案:B
本题解析:大豆含有丰富的蛋白质,豆腐是大豆经过浸泡、磨细、煮沸、过滤、凝聚等过程制得的,副产品为豆浆和豆清。
本题难度:一般
4、实验题 (8分)现有四种烃:①C2H6? ②C2H4? ③C2H2? ④C6H5CH3
(1)易发生取代反应的烃是(填序号,下同) ___________,易发生加成反应的是___________。
(2)碳碳键的键长由长到短的顺序为___________。
(3)在空气中燃烧时,能产生浓烟的是___________,其原因是___________。
(4)将其通入(或滴入)KMnO4酸性溶液中,能使之褪色的有______________________。
(5)③与HCl的反应产物在一定条件下合成高分子化合物的反应方程式为________________。
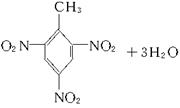
(6)④与浓H2SO4、浓HNO3反应生成TNT的化学方程式为____________________________。
参考答案:(1)①④? ②③
(2)①>④>②>③
(3)③④?碳的质量分数大
(4)②③④
(5)nCH2==CHCl

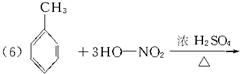
本题解析:(1)烷、苯及苯的同系物易发生取代反应,烯、炔易发生加成反应。
(2)碳原子间共用电子对越多的键能越大,键长越短。
(3)碳含量高的烃燃烧不充分,产生浓烟。
(4)烯、炔、苯的同系物能使KMnO4酸性溶液褪色
本题难度:简单
5、判断题 人体缺碘会影响正常的的生命活动,为提高人体的素质,食物补碘已引起人们的重视。试回答下列问题:
(1)成年人体内缺碘会产生的病症是?(?)
A.甲亢? B. 侏儒症? C.地方性呆小症? D. 地方性甲状腺肿
(2)我国缺碘病区甚广,防止缺碘病的主要措施是食盐加碘。1996年我国政府以国家的方式规定食盐添加剂是KIO3,不使用KI的原因可能是?(?)
A. KI口感苦涩? B.有毒? C. KI 在储运过程中易变质?D. KI价格昂贵
(3)人从食物中摄取碘后,碘在便在甲状腺中积存。在甲状腺内,通过有关化学反应后形成甲状腺素,甲状腺素的合成过程可表示为:
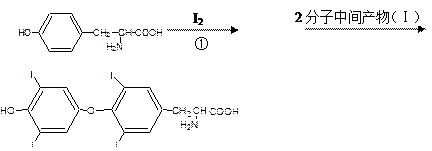 ?
?
中间产物
(甲状腺素)+产物Ⅱ
甲状腺素的分子式?,中间产物(Ⅰ)的结构简式为?;
产物(Ⅱ)的名称为?,
(4)我国是世界上严重缺碘的地区,全国约有四亿多人缺碘。1991年,我国政府向全世界做出了“到2000年在全国消灭碘缺乏病”的庄严承诺。我国政府为了消灭碘缺乏病,在居民的食用盐中均加入了一定量的碘酸钾(KIO3),以确保人体对碘的摄入量。已知在溶液中 IO3-可和I-发生反应:IO3-+5I-+6H+=3I2+3H2O,根据此反应,可用试纸和一些生活中常见的物质进行实验,证明在食盐中存在IO3-。可供选用的物质有:①自来水,②蓝色石蕊试纸,③碘化钾淀粉试纸,④淀粉,⑤食盐,⑥食醋,⑦白酒。进行上述实验时必须使用的物质是
A.①③ B. ③⑥ C. ②④⑥ D. ①②④⑤⑦
参考答案: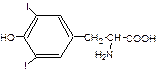 (1)D?
(1)D?
(2)A、C?
(3)C15H11NO4I4?丙氨酸(或α―氨基丙酸)
(4)B
本题解析:碘是甲状腺素的重要组成元素,婴幼儿呆小症,成人缺碘会导致地方性甲状腺肿。碘盐是防治缺碘病症的措施之一,碘盐中用的最多的是KIO3,较少用KI,因为KI口感苦涩,且碘离子易被空气中氧气氧化。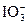 与
与 反应需要提供酸性环境,为此需要使用CH3COOH(食醋的主要成分),产生的I2用淀粉检验。甲状腺素的合成路线是
反应需要提供酸性环境,为此需要使用CH3COOH(食醋的主要成分),产生的I2用淀粉检验。甲状腺素的合成路线是
 ?
?
+ I2
本题难度:一般