1������� Ϊ��֤ľ̿��Ũ���ᷴӦ���������ж�������Ͷ�����̼��ѡ����ͼ����������ʢ���ʣ�����װ����ʵ��װ�ã��Իش��������⣮
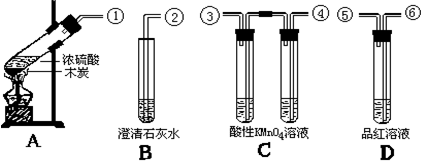
��1����ʵ������У����������������˳��A��B��C��D��װ�õ�����Ӧ���ǣ�______��������ĸ���ţ�
�����ܵ�����˳��Ӧ���ǣ�______���������ַ��ţ�
��2���Թ�B��C��D�и���ʲô�����ܱ�ʾ�Ѽ��������̼����������
B��Ϊ______��
C��Ϊ______��
����ȡ����֧���Ը��������Һ�Թܵ���ҪĿ����______��D��Ϊ______��
��3��д��Aװ���з�Ӧ��ѧ����ʽ��______��
�ο��𰸣���1��ʵ��Ŀ������֤ľ̿��Ũ���ᷴӦ���������ж�������Ͷ�����̼�����ڶ�������Ͷ�����̼���ܹ�ʹ����ʯ��ˮ����ǣ����Լ��������̼֮ǰӦ��������������Ȼ���ٳ�ȥ�������������������̼������װ������˳��Ϊ��ADCB��װ��C�����dz�ȥ��������ϴ��װ���еĵ���Ӧ�ò��ó����̳���ʽ�����Ե�������˳��Ϊ���٢ޢݢܢۢڣ�
�ʴ�Ϊ��ADCB���٢ޢݢܢۢڣ�
��2���Թ�B���������̼������Ϊ����ʯ��ˮ����ǣ��Թ�C��Ŀ��Ϊ���������Ը��������Һ��ȥ���������������Ը��������Һ�����Ƿ��������������Ϊ���ڶ�֧�Թ������Ը��������Һ��ɫ����һ֧�Թ������Ը��������Һ����ɫ���Թ�Dװ��Ʒ����Һ�����ڼ����������Ĵ��ڣ�����ΪƷ����Һ��ɫ��
�ʴ�Ϊ������ǣ��ڶ�֧�Թ������Ը��������Һ��ɫ����һ֧�Թ������Ը��������Һ����ɫ���������Ը��������Һ��ȥ���������������Ը��������Һ�����Ƿ������Ʒ����Һ��ɫ��
��3��̼��Ũ���ᷴӦ�Ļ�ѧ����ʽΪ��C+2H2SO4��Ũ����.CO2��+2SO2��+2H2O��
�ʴ�Ϊ��C+2H2SO4��Ũ����.CO2��+2SO2��+2H2O��
���������
�����Ѷȣ�һ��
2��ѡ���� ���������ԡ���ԭ�Ե�ǿ�������������ʵĽṹ�йأ��������ʵ�Ũ�Ⱥͷ�Ӧ�¶ȵ��йأ����и������У�����Ũ�Ȳ�ͬ���ܷ�����ͬ������ԭ��Ӧ���ǣ�������
A��Cu��HNO3��Һ
B��Cu��FeCl3��Һ
C��Zn��H2SO4��Һ
D��Fe��HCl��Һ
�ο��𰸣���A��Cu��HNO3��Һ�У���ΪŨ���ᣬ����Cu+4HNO3�TCu��NO3��2+2NO2��+2H2O����Ϊϡ���ᣬ����3Cu+8HNO3�T3Cu��NO3��2+2NO��+4H2O����A�������⣻
B��Cu��FeCl3��Һ�У�����Ũ�ȴ�С��ֻ����Cu+2FeCl3�T2FeCl2+CuCl2����B���������⣻
C��Zn��H2SO4��Һ�У���Ϊϡ���ᣬ����Zn+H2SO4�TZnSO4+H2������ΪŨ���ᣬ����Zn+2H2SO4��Ũ��?��?.?ZnSO4+SO2��+2H2O����C�������⣻
D��Fe��HCl��Һ�У�����Ũ�ȴ�С��ֻ����Fe+2HCl=FeCl2+H2������D���������⣻
��ѡAC��
���������
�����Ѷȣ���
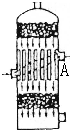
3��ѡ���� �����Ṥҵ�����У�Ϊ��������SO2��ת�������ܳ���������ܣ��������м����Ƚ������ĽӴ��ң���ͼ���������ܱ���ϵ���������������A������������Ϊ��������
A��SO2
B��SO3��O2
C��SO2��SO3
D��SO2��O2