1、简答题 某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究.
(1)写出试管B中的实验现象______.
(2)写出A中反应的化学方程式______
(3)继续向A试管中加入H2O2,发现铜片溶解,反应的离子方程式为:______.
若仍不补充浓硫酸,只要求使铜片溶解,也可以加入(填写两种属于不同类别物质的化学式)______、______.
(4)B试管口的棉花应沾有的试剂是______.
(5)小组成员向反应后的溶液中加入足量的氧化铜,使剩余的硫酸全部转化为硫酸铜,过滤后,将滤液加热浓缩,冷却结晶制得硫酸铜晶体(CuSO4?xH2O).小组成员采用加热法测定该晶体里结晶水x的值.
①在他们的实验操作中,至少称量______次;
②下面是其中一次实验的数据:
| 坩埚质量 | 坩埚与晶体的总质量 | 加热后坩埚与固体总质量
11.7g
22.7g
18.9g
|
根据上表数据计算判断x的实侧值比理论值(x=5)______(填“偏大”、“偏小”),这次实验中产生误差的原因可能是______(填序号)
A.硫酸铜晶体中含有不挥发的杂质?B.实验前晶体表面有湿存水
C.加热时有晶体飞溅出去?D.加热失水后露置在空气中冷却.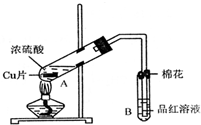
参考答案:(1)二氧化硫具有漂白性,能使品红褪色,故答案为:品红溶液褪色;
(2)铜与浓硫酸在加热条件下反应生成硫酸铜和二氧化硫气体,反应的化学方程式为Cu+2H2SO4?△?.?CuSO4+SO2↑+2H2O,故答案为:Cu+2H2SO4?△?.?CuSO4+SO2↑+2H2O;
(3)在酸性条件下,过氧化氢具有强氧化性,能氧化Cu而生成铜离子和水,反应的方程式为Cu+H2O2+2H+=Cu2++2H2O,根据铜能与铁离子、硝酸根离子反应,也可选用Fe2O3或NaNO3,
故答案为:Cu+H2O2+2H+=Cu2++2H2O;Fe2O3;NaNO3;
(4)二氧化硫为有毒气体,不能排放到空气中,根据二氧化硫为酸性气体,应用NaOH溶液吸收,故答案为:NaOH(溶液);
(5)①实验中为准确测定结晶水的值,应分别测定坩埚的质量、坩埚与晶体的总质量,以此测定晶体的质量,然后称量加热后坩埚与固体总质量,之后再加热一次以判断晶体是否完全分解,总共称量4次,故答案为:4;
②该实验晶体的质量为22.7g-11.7g=11g,硫酸铜的质量为18.9g-11.7g=7.2g,水的质量为22.7g-18.9g=3.8g,则n(CuSO4)=7.2g160g/mol=0.045mol,n(H2O)=3.8g18g/mol=0.21mol,所以
x=0.210.045=4.7,小于5,硫酸铜晶体中含有不挥发的杂质,加热失水后露置在空气中冷却等都会造成硫酸铜的质量偏大,水的质量偏小,而实验前晶体表面有湿存水或加热时有晶体飞溅出去,会造成质量差偏大,结果偏大.
故答案为:偏小;AD.
本题解析:
本题难度:一般
2、填空题 (1)目前,我国采用“接触法”制硫酸。有关接触法制硫酸的下列说法中,正确的是_________。
A.二氧化硫的接触氧化在合成塔中发生
B.吸收塔得到的硫酸浓度为98%
C.煅烧含硫48%的黄铁矿时,若FeS2损失了2%,则S损失4%
D.接触室中适宜条件是V2O5催化剂、高温、常压
E.接触室中采取高温是为了提高催化剂的活性和提高SO2的转化率
(2)硫酸工厂排放的尾气中,含少量二氧化硫。为防止污染大气,在排放前必须进行尾气处理并设法进行综合利用。硫酸工厂排放尾气中的SO2通常用足量石灰水吸收,然后再用稀硫酸处理。
①写出上述过程的化学反应方程式:_____________________
②清说出这种尾气处理方法的优点(写出两点即可):_________________
③若某硫酸厂每天排放的1万立方米(标准状况)尾气巾含0.2%(体积分数)的SO2,通过上述方法处理,理论上需生石灰_______kg。
(3)某研究小组用NaOH溶液吸收尾气中的二氧化硫,将所得的Na2SO3溶液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴阳膜组合循环再生机理如图所示,a、b离子交换膜将电解槽分为三个区域,电极材料为石墨。
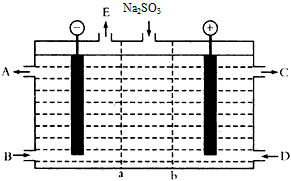
①图中a表示____(填“阴”或“阳”)离子交换膜。 Na2SO3 A-E分别代表生产中的原料或产品,其中C为硫酸,则A表示_______,E表示__________。
②阳极的电极反应式为____________________。
参考答案:(1)D
(2)①SO2+Ca(OH)2=CaSO3↓+H2O、CaSO3+H2SO4=CaSO4+SO2↑+H2O;②原料生石灰、硫酸价格便宜且容易获得;可得到石膏副产品;产生的SO2含量较高可返回作为原料(任写两点即可);③50
(3)①阳;NaOH溶液;氢气;②SO42--2e-+H2O=2H++SO42-
本题解析:
本题难度:一般
3、填空题 为了确定CH3COOH ,?OH及H2CO3的酸性强弱,有人设计一个简单的一次性完成实验的装置图如右所示:(每空2分共8分)
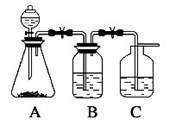
(1)若锥形瓶中装有一易溶于水的正盐固体,则A中发生反应的离子方程式为?
(2)装置B中盛放的试剂是??,它的作用是 ?
(3)实验中观察到C中出现的主要现象是?
?.
参考答案:(1)2CH3COOH+CO2-3=2CH3COO--+CO2↑+H2O
(2)饱和NaHCO3溶液 除去CO2中混有的CH3COOH
 (3)C中溶液变浑浊
(3)C中溶液变浑浊
本题解析:酸性: CH3COOH>H2CO3>?OH>HCO3-;用2CH3COOH+Na2CO3=2CH3COONa+ CO2↑+H2O 来证明CH3COOH强于H2CO3;用CO2+H2O+?ONa →? OH+ NaHCO3,来证明H2CO3酸性大于? OH,中间为了避免CH3COOH挥发来对实验造成干扰,用饱和NaHCO3溶液 除去CO2中混有的CH3COOH。
本题难度:简单
4、选择题 浓硫酸与下列物质反应时,既表现强酸性又表现强氧化性的是( )
A.赤热的木炭
B.蔗糖遇浓硫酸变黑并膨胀
C.亚硫酸钠
D.铜片
参考答案:A.赤热的木炭和浓硫酸反应生成SO2、CO2和水,没有盐生成,S元素的化合价降低,只表现为强氧化性,故A错误;
B.蔗糖遇浓硫酸变黑,体现了浓硫酸的脱水性,木炭和浓硫酸反应生成SO2、CO2和水,蔗糖膨胀,S元素的化合价降低,表现为强氧化性,故B错误;
C.亚硫酸钠和浓硫酸发生反应生成硫酸钠、水和二氧化碳,有盐生成,但S元素的化合价不变,只表现为强酸性,故C错误;
D.铜片和H2SO4(浓)反应生成CuSO4、二氧化硫和水,有盐生成,S元素的化合价降低,既表现强酸性又表现强氧化性,故D正确;
故选D.
本题解析:
本题难度:简单
5、选择题 A、B两种有机物组成的混合物,当混合物的总质量相等时,无论A、B两种有机物以何种比例混合,完全燃烧后生成的二氧化碳质量都相等,符合这一条件的有机物组合是
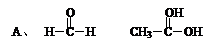 ?
?
B、C6H6? C6H5OH
C、CH3OH? HOCH2CH2OH? D、CH4? C10H8O2
参考答案:AD
本题解析:据题意,完全燃烧后生成的CO2的质量相等,则要求两物质中碳元素的质量分数相同。
A、CH2O与C2H4O2,含碳元素质量分数相同
B、C6H6与C6H6O,含碳元素质量分数不同
C、CH4O与C2H6O2,含碳元素质量分数不同
D、CH4中含1个碳原子同时含4个氢原子,C10H8O2中可将2个氧原子的质量看作32个氢原子的质量,则可视为含有10个碳原子同时含有40个氢原子,即含碳元素的质量分数相同
故本题答案为A、D。
本题难度:简单