1��ѡ���� ����ͼʾ���Ӧ�������������
[? ]
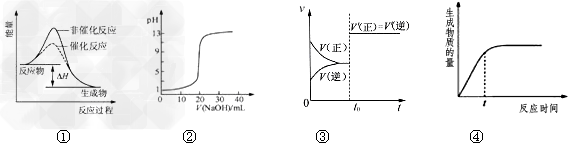
A.ͼ�ٱ�ʾij���ȷ�Ӧ�ֱ����С�����������·�Ӧ�����е������仯
B.ͼ�ڱ�ʾ0.1000?mol/LNaOH��Һ�ζ�20.00mL?0.1000?mol/LHCl��Һ���õ��ĵζ�����
C.ͼ�۱�ʾ�Ѵ�ƽ���ij��Ӧ����t0ʱ�ı�ijһ������Ӧ������ʱ��仯����ı������һ���Ǽ������
D.ͼ�ܱ�ʾij���淴Ӧ����������淴Ӧʱ��仯�����ߣ���ͼ֪tʱ��Ӧ��ת�������
�ο��𰸣�B
���������
�����Ѷȣ�һ��
2��ѡ���� ����ʵ������У�������ǣ�������
A������5%ʳ����Һʱ����������ʳ�η����ձ��м�������ˮ�����ܽ�
B��ͭ�ᾧˮ�����ⶨʱ������С�������ȣ���ֹ����ɽ�
C���ⶨδ֪NaOH��ҺŨ��ʱ����ʽ�ζ������ñ���Һ��ϴ2-3��
D������0.1mol/L��H2SO4��Һʱ������ȡ��ŨH2SO4��������ƿ�м�ˮϡ��
�ο��𰸣�D
���������
�����Ѷȣ�һ��
3������� ijѧ��������֪���ʵ���Ũ�ȵ��������ζ����ⶨδ֪���ʵ���Ũ�ȵ�����������Һ��ѡ���̪��ָʾ��������գ�
��1���ñ���������Һ�ζ����������������Һʱ�����ְ�����ʽ�ζ��ܵĻ���������ҡ����ƿ���۾�ע��______��ֱ�������һ���������Һ��______��Ϊ______�����Ұ�����ڲ��ָ���
��2�����в����У�����ʹ��������������Һ��Ũ��ֵƫ�͵���______
A����ʽ�ζ���δ�ñ�������Һ��ϴ��ֱ��ע���������Һ
B���ζ�ǰʢ������������Һ����ƿ������ˮϴ����û�и���
C����ʽ�ζ����ڵζ�ǰ�����ݣ��ζ���������ʧ
D����ȡ�������ʱ���ζ�����ʱ���Ӷ���
��3��ijѧ����������ʵ��ֱ��¼�й��������£�
| ����� | ������������
��Һ�����/mL | 0.1000mol/L����������mL��
�ζ�ǰ�̶�
�ζ���̶�
��Һ���/mL
��һ��
25.00
0.00
26.11
26.11
�ڶ���
25.00
1.56
30.30
28.74
������
25.00
0.22
26.31
26.09
|
��ѡ�����к��������ݼ����������������Һ�����ʵ���Ũ�ȣ�c��NaOH��=______��
�ο��𰸣���1������к͵ζ�ʱ���۾�Ҫע����ƿ����Һ����ɫ�仯���ζ��յ�ʱ��Һ��ɫ�ɺ�ɫͻ��Ϊ��ɫ���Ұ�����ڲ���ɫ���Ұ�����ڲ���ɫ��
�ʴ�Ϊ����ƿ����Һ��ɫ�ı仯����ɫ����ɫ��
��2��A����ʽ�ζ���δ�ñ�������Һ��ϴ��ֱ��ע���������Һ����Һ��Ũ��ƫС�����V������ƫ����c�����⣩=c(��)��V(��)V(����)��֪���ⶨc��NaOH��ƫ��A����
B���ζ�ǰʢ������������Һ����ƿ������ˮϴ����û�и������Һ�����ʵ������䣬��V��������Ӱ�죬����c�����⣩=c(��)��V(��)V(����)��֪���ⶨc��NaOH����Ӱ�죬��B����
C����ʽ�ζ����ڵζ�ǰ�����ݣ��ζ���������ʧ�����V������ƫ����c�����⣩=c(��)��V(��)V(����)��֪���ⶨc��NaOH��ƫ��C����
D����ȡ�������ʱ���ζ�����ʱ���Ӷ��������V������ƫС������c�����⣩=c(��)��V(��)V(����)��֪���ⶨc��NaOH��ƫ�ͣ���D��ȷ��
��ѡD��
��3���������ݵ���Ч�ԣ���ȥ��2�����ݣ���1��3��ƽ������V�����ᣩ=26.11mL+26.09mL2=26.10mL��
���ݷ�Ӧ����ʽ HCl+NaOH�TNaCl+H2O
0.0261L��0.1000mol/L 0.025L��C��NaOH��
��C��NaOH��=0.0261L��0.1000mol/L0.025L=0.1044mol/L��
�ʴ�Ϊ��0.1044mol/L��
���������
�����Ѷȣ�һ��
4������� ��1���������е�����ѧ��ѧʵ�����м��ֳ���������������ƿ����ʽ�ζ��ܡ���ʽ�ζ��ܡ��¶ȼơ���Ͳ��������ƽ����ͨ©�������������ձ���
����Ҫ�����к͵ζ�ʵ�飬��ȱ�ٵIJ���������______��
����Ҫ��̼���ƹ�������һ�����ʵ���Ũ�ȵ�̼������Һ����ȱ�ٵIJ���������______��
��2��ijѧ����һ֧�Թ��а�һ����˳��ֱ�������м�����Һ��һ����Һֻ��һ�Σ���
A��KI��Һ?B��������Һ?C��NaOH��Һ?D��ϡH2SO4?E����ˮ��
������Һ��ɫ������˳��仯����ɫ���ػ�ɫ����ɫ����ɫ����ɫ��
������Һ��ɫ�ı仯���жϼ�������ҩƷ��˳���ǣ���д��ţ�______��
��3��������֪������ȼ������ˮ��Ȼ�������ϱ���������ȼ��ʱ������ˮ�⣬��������һ���ijͬѧ����ͼ��ʾ��ʵ��װ�ã���֤�ò���Ĵ��ڣ�ʵ�鲽�輰�������£���H2���鴿����������ű��飮
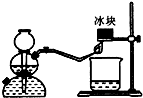
����С�ձ��ڼ����������ữ��ϡKI������Һ����С�ձ����ڱ����·���
�۲쵽�ձ�����Һ����ɫ�������ɫ��
������һ��С�ձ��ڼ����������ữ��ϡKMn04��Һ����С�ձ����ڱ����·����۲쵽�ձ�����Һ�������ɫ������д����һ����Ľṹʽ��______��
������ʵ���п��Թ��ɳ��ò���Ļ�ѧ������______��
�ο��𰸣���1�������к͵ζ�ʵ��IJ��������У���ʽ�ζ��ܡ���ʽ�ζ��ܡ���ƿ���ʴ�Ϊ����ƿ��
��������һ�����ʵ���Ũ�ȵ�̼������Һ��Ҫ��������������ƽ��ҩ�ס��ձ�����������һ����������ƿ����ͷ�ιܣ��ʴ�Ϊ����ͷ�ιܣ�
��2��KI��Һ����ˮ��Ӧ���ɵ��ʵ⣬������ˮ���ػ�ɫ������������Һ����Һ����������NaOH��Һ��Ӧ���ɵ⻯�ơ������ƺ�ˮ����ɫ��ȥ���⻯�ƺ͵��������������������ɵ��ʵ⣬��Һ�������ʴ�Ϊ��A��E��B��C��D��?
��3�����������������������������KI�����ɵ��ʵ⣬��Һ�������������������������ԣ���KMn04��Һ�������������������������⣬��Һ��ɫ���������������˻�ԭ�ԣ�
�ʴ�Ϊ��H-O-O-H�������Ժͻ�ԭ�ԣ�
���������
�����Ѷȣ�һ��
5������� ��һ����2.5g̼���ơ�̼�����ƺ��������ƹ���������ȫ����ˮ�У��Ƴ�ϡ��Һ��Ȼ�������Һ����μ���1 mol/L���ᣬ�����������������CO2���������״������ϵ����ͼ��ʾ
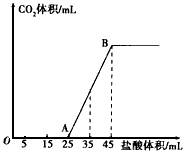
(1)д��OA����������Ӧ�����ӷ���ʽ_________________��
(2)������35mL����ʱ������������̼�����Ϊ___________mL ����״������
(3)ԭ�������Na2CO3����������Ϊ____________��
������������Ҫ�ĵ��ʣ��Dz������Ļ�����Ʒ֮һ���α�����ܵĺϳɰ������й��������ǵ¹���ѧ�ҹ�����1905�귢���ģ���ϳ�ԭ��Ϊ��N2(g)+3H2(g)2NH3(g) ;��H = - 92.4 kJ/mol������˻����1918���ŵ������ѧ�����Իش��������⣺
(4)���з������ʺ�ʵ������ȡ��������____������ţ���
A������ʯ���еμ�Ũ��ˮ B������Ũ��ˮ
C��ֱ���������͵����ϳ� D�����Ȼ����Һ�еμ�Ũ����������Һ
(5)�ϳɰ���ҵ�в�ȡ�����д�ʩ������������ԭ�����͵���__________������ţ���
A�����ýϸ�ѹǿ(20 MPa��50 MPa) B������500��ĸ���
C��������ý������ D�������ɵİ�Һ������ʱ����ϵ�з��������δ��Ӧ��N2��H2ѭ�����ϳ�����
(6)�����ֻ���ϢϵͳDIS(����ͼI��ʾ�����ɴ����������� �ɼ����ͼ�������)���Բⶨ������ˮ��Ũ�ȡ�����ʽ�ζ���ȷ��ȡ0.500 0mol/L������Һ25.00 mL���ձ��У��øð�ˮ���еζ����������Ļ����ʾ����Һ�ĵ��������氱ˮ����仯��������ͼ����ʾ��
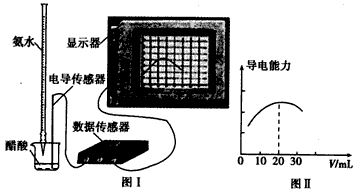
���õζ���ʢ��ˮǰ���ζ���Ҫ��_____________��ϴ2��3�顣
���Լ���ð�ˮ��Ũ�ȣ�__________________��
����������£��ᵼ��ʵ����c(NH3��H2O)ƫ�͵���________________��
A���ζ�����ʱ���Ӷ���
B����ȡ25.00 mL������Һʱ��δ����ʢ��Һ��ϴ�ζ���
C���ζ�ʱ����������ˮ�����ձ���
(7)1998��ϣ������ʿ��´�ѧ��Marnellos��Stoukides���ø����ӵ����Ե�SCY�մɣ��ܴ���H+����ʵ���˸��³�ѹ�¸�ת���ʵĵ绯ѧ�ϳɰ�����ʵ��װ������ͼ��

�����ĵ缫��ӦʽΪ___________________________
�ο��𰸣�
(1)H++OH-=H2O��CO32-+H+=HCO3-
(2)224
(3)42.4%
(4)CD
(5)AD
(6)���������ⰱˮ����0. 6250mol/L����AC
(4)N2+6e-=2N3-
���������
�����Ѷȣ�����