| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学必考知识点《电解质和非电解质》高频试题巩固(2019年最新版)(八)
参考答案:A 本题解析:①硫的非金属性比较弱,已知Fe与S能直接化合生成FeS,则Cu与S可直接化合生成Cu2S,错误;②已知CaCO3与稀硝酸反应生成CO2,但硝酸具有氧化性,则CaSO3与稀硝酸反应生成硫酸,得不到SO2,错误;③已知Br2与Fe反应生成FeBr3,但碘的非金属性比较弱,I2与Fe生成FeI2,错误;④已知Fe与CuSO4溶液反应,活泼的金属能置换出不活泼的金属,则推测Fe与AgNO3溶液也能反应,正确;⑤已知NaOH是强电解质,其饱和溶液导电能力很强,Ca(OH)2也是强电解质,但其饱和溶液中离子浓度小,其饱和溶液导电能力较弱,错误,答案选A。 本题难度:一般 2、选择题 下列说法正确的是 ( ) |
参考答案:C
本题解析:电解质是指在水溶液或熔融状态下能导电的化合物,与溶解性无关,例如:NH3极易溶于水但是非电解质,A错误;熔融状态只破坏离子键不破坏共价键,液态氯化氢不能导电,B错误;而NaCl是离子化合物,液态时能导电,C正确;钠是单质不是化合物故既不是电解质也不是非电解质,D错误。答案选C。
本题难度:一般
3、选择题 下列各组物质,前者是混合物,后者是纯净物的是
A.水玻璃 玻璃
B.石油 盐酸
C.干冰 铝热剂
D.氯水 液氯
参考答案:D
本题解析:A、水玻璃是硅酸钠水溶液为混合物,玻璃是混合物;B、石油是各种烷烃、环烷烃的混合物,盐酸是氯化氢的水溶液是混合物;C、干冰是固态二氧化碳是纯净物,铝热剂是铝与氧化铁的混合物;D、氯水是氯的水溶液是混合物,液氯是液态的氯气是纯净物;答案选D。
考点:物质的分类
本题难度:简单
4、填空题 (6分)下列物质:①Na2SO4 ②HNO3 ③KClO3 ④NaHCO3⑤Ar ⑥H2 ⑦H2O ⑧NaOH
属于酸的是: 属于碱的是: 属于氧化物的是: (填序号)
参考答案:②; ⑧; ⑦
本题解析:酸:电离出来的阳离子都是氢离子的化合物为酸;碱:电离出来的阴离子都是氢氧根的为碱;氧化物:两种元素,其中一种为氧元素!
本题难度:一般
5、填空题 (8分)从盐酸、硫酸、石灰水、烧碱、氢氧化钡、纯碱、硝酸钠、氯化钡(均为溶液)八种物质中选出四种,使得各线条相连的物质均能发生反应且生成难溶物。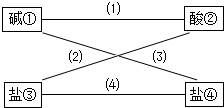
(1)写出下列各物质的化学式:
② ③
(2)写出连线(2)的化学方程式:
写出物质④的电离方程式:
(3)写出连线(1)的离子方程式: 。
参考答案:(1)H2SO4、BaCl2
(2)Ba(OH)2 + Na2CO3=BaCO3↓ + 2NaOH Na2CO3 = 2Na+ + CO32-
(3)Ba2++2OH-+2H++SO42- = BaSO4↓+ 2H2O
本题解析:硫酸与氢氧化钡反应会产生沉淀,故①是氢氧化钡,②是硫酸,硫酸与氯化钡反应有沉淀生成,故③是氯化钡,氢氧化钡与纯碱反应有沉淀生成,故④是纯碱,故答案为:
(1)②H2SO4;③BaCl2;(2)连线(2)的化学方程式为:Ba(OH)2 + Na2CO3=BaCO3↓ + 2NaOH;物质④的电离方程式为:Na2CO3 = 2Na+ + CO32-;连线(1)的离子方程式为:Ba2++2OH-+2H++SO42- = BaSO4↓+ 2H2O。
考点:考查物质的分类和性质。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学必考知识点《硫酸》高频.. | |