1、选择题 常温下,在溶液中可发生以下反应:
①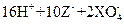 ===
===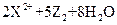 ,
,
②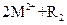 ===
===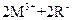 ,③
,③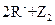 ===
===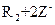 ,
,
由此判断下列说法错误的是(?)
A.还原性强弱顺序为: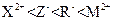
B.Z元素在反应①中被氧化,在③中被还原
C.常温下可发生反应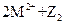 ===
===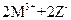
D氧化性强弱顺序为: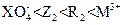
参考答案:D
本题解析:略
本题难度:简单
2、选择题 氯酸质量分数超过40%时会发生分解,反应可表示为:8HClO3=3O2↑+2Cl2↑+4HClO4+2H2O,下列说法正确的是( )
A.氧化性比较HClO4>HClO3
B.氧化产物只有HClO4
C.氯酸分解后的混合气体平均相对分子质量为47.6
D.该反应转移电子数为12e-
参考答案:A、反应中氯元素化合价由HClO3中+5价升高为HClO4中+7价,HClO3是氧化剂,HClO3属于氧化产物,所以氧化性比较HClO3>HClO4,故A错误;
B、反应8HClO3=3O2↑+2Cl2↑+4HClO4+2H2O中,氯元素化合价由+5价升高为+7价,由+5价降低为0价;氧元素化合价由-2价升高为0价,所以氧化产物是O2、HClO4,故B错误;
C、混合气体为氧气和氯气,二者物质的量之比为3:2,所以平均相对分子质量为3×32+2×713+2=47.6,故C正确;
D、反应8HClO3=3O2↑+2Cl2↑+4HClO4+2H2O中,氯元素化合价由+5价升高为+7价,由+5价降低为0价;氧元素化合价由-2价升高为0价,反应中只有氯元素的化合价降低由+5价降低为0价,根据氯气计算转移电子数为2×2×(5-0)=20,故D错误.
故选C.
本题解析:
本题难度:简单
3、选择题 从海水中提取溴的过程中涉及到反应:Br2 + SO2 + 2H2O =" 2HBr" + H2SO4,下列说法正确的是
A.Br2在反应中被氧化
B.SO2在反应中表现还原性
C.H2SO4是还原产物
D.1 mol氧化剂在反应中失去2 mol电子
参考答案:B
本题解析:根据方程式可知,在反应中溴元素的化合价从0价降低到-1价,得到1个电子,即单质溴是氧化剂。SO2中S元素的化合价从+4价升高到+6价,失去2个电子,SO2是还原剂。其中溴化氢是还原产物,硫酸是氧化产物,答案选B。
点评:该题是基础性试题的考查,也高考中的常见考点。试题紧扣教材,意在培养学生灵活运用基础知识解决实际问题的能力。该题的关键是明确氧化还原反应中有关概念的含义以及判断依据,然后结合方程式灵活运用即可。
本题难度:简单
4、选择题 已知Co2O3在酸性溶液中易被还原成Co2+,且Co2O3、Cl2、FeCl3、I2的氧化性依次减弱。下列叙述中,正确的是
[? ]
A.Cl2通入FeI2溶液中,可存在反应3Cl2+6FeI2= 2FeCl3 +4FeI3
B.每1 mol Co2O3在酸性溶液中被还原生成Co2+时转移1 mol e-
C.FeCl3溶液能使淀粉KI试纸变蓝
D.I2是ⅦA族元素形成的单质,具有较强的氧化性,可以将Co2+氧化成Co2O3
参考答案:C
本题解析:
本题难度:一般
5、选择题 下列装置或实验操作正确的是( )
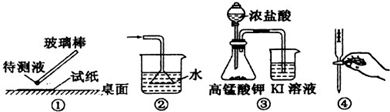
A.①用pH试纸测某溶液的酸碱性
B.②吸收氨气制氨水
C.③探究氧化性:KMnO4>Cl2>I2
D.④中和滴定实验
参考答案:A.用pH试纸测某溶液的酸碱性,PH试纸放在玻璃片上,不能放在桌子上,故A错误;
B.吸收溶解度较大的气体时,漏斗应刚好接触溶液,不是深入到溶液内,故B错误;
C.锥形瓶中发生反应:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,氧化性KMnO4>CL2,烧杯中发生反应:Cl2+2KI=2KCl+I2,氧化性Cl2>I2,故C正确;
D.滴定过程中,需要控制活塞和振荡锥形瓶,即左手旋转滴定管的玻璃活塞,右手不停摇动锥形瓶,故D错误;
故选C.
本题解析:
本题难度:简单