1、选择题 向甲、乙两个容积均为1 L的恒容容器中,分别充入2 mol A,4 mol B和1 mol A,2 mol B。相同条件下,发生下列反应:A(g)+2B(g) xC(g) ΔH<0。测得两容器中c(A)随时间t的变化如图所示,下列说法正确的是? ( )
xC(g) ΔH<0。测得两容器中c(A)随时间t的变化如图所示,下列说法正确的是? ( )

A.x可能等于3
B.向平衡后的乙容器中充入氦气可使A的转化率降低
C.将乙容器单独升温,c(A)可达到0.78 mol/L
D.若向甲容器中再充入2 mol A,4 mol B,平衡时甲容器中c(A)大于1.56 mol/L
参考答案:C
本题解析:分析可知甲装置相当于在乙装置基础上加压,但比乙中A浓度的2倍小,说明平衡正移,正向为气体体积减小的反应,所以可知x不能等于3,只能小于3,A错;恒温恒容,通惰性气体,平衡不移动,转化率不变,B错;升温,平衡逆向移动,c(A)增大,可达到0.78 mol/L,C正确;若向甲容器中再充入2 mol A,4 mol B,平衡正向移动,c(A)小于1.56 mol/L,D错。
本题难度:一般
2、填空题 (14分)
含硫化合物在工业生产中有广泛的用途。
(1)对于可逆反应2SO2(g)+O2(g)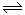 2SO3(g) △H<0,下列研究目的和图示相符的是?
2SO3(g) △H<0,下列研究目的和图示相符的是?
(填序号)
序号
| A
| B
| C
| D
|
目的
| 压强对平衡的影响
| 温度对转化率的影响
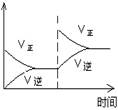
| 增加O2浓度对速率的影响
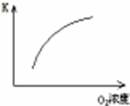
| 浓度对平衡常数的影响
|
图示
| 
| 
| 
| 
|
(2)在5000C有催化剂存在的条件下,向容积为2L的甲乙两个密闭容器中均充入2molSO2和1molO2。甲保持容积不变,乙保持压强不变,充分反应后,均达平衡状态,此时SO3的体积分数甲
?乙。(填“>”“<”或“="”" )
(3)向2L的甲容器中充入2molSO2、1molO2,测得SO2的平衡转化率与温度的关系如下图所示。
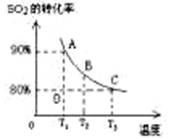
Ⅰ.在T1温度下,反应进行到状态D时,v正?v逆。(填“>”“<”或“="”" )
Ⅱ.T3温度下,平衡时测得反应放出的热量为Q1,在相同温度下若再向容器中通入2molSO2、1molO2,重新达到平衡,测得反应又放出热量Q2 。则下列说法中正确的是?。(填序号)
A.相同温度下新平衡时容器中的压强是原平衡时的两倍
B.Q2一定大于Q1
C.新平衡时SO2的转化率一定大于80%
(4)在甲容器中充入一定量的SO2和1.100molO2,在催化剂作用下加热,当气体的物质的量减少0.315mol时反应达到平衡,此时测得气体压强为反应前的82.5%,则SO2的转化率为?。
(5)若用氢氧化钠溶液吸收SO2气体恰好得到酸式盐,已知该酸式盐溶液呈弱酸性,则溶液中各离子浓度由大到小的顺序为?。(用离子浓度符号表示)
(6)一定温度下,用水吸收SO2气体,若得到pH=5的H2SO3溶液,则溶液中亚硫酸氢根离子和亚硫酸根离子的物质的量浓度之比为? ?。(已知该温度下H2SO3的电离常数:Ka1=1.0×10-2mol/L,Ka2=6.0×10-3mol/L)
参考答案:(每空2分,共14分)?
(1) C (有错计0分)
(2)? <?
(3)? I? >? II? B C(对一个计1分,有错计0分)
(4)? 90%?
(5)? c (Na+)?>c (HSO3―) >c (H+)>c (SO32―)>c (OH―) (有错计0分 )
?(6)1/6 ×10-2 或1.67 ×10-3
本题解析:(1)A、由图可知,P1>P2,压强增大,平衡正向移动,三氧化硫的体积分数应增大,与图不符,错误;B、该反应为放热反应,温度升高,平衡逆向移动,二氧化硫的转化率降低,与图不符,错误;C、增加氧气得浓度,正反应速率增大,逆反应速率不变,平衡正向移动,与图符合,正确;D、氧气浓度增大,但温度不变,平衡常数不变,与图不符,错误,答案选C。
(2)开始时甲、乙两容器的压强相同,达平衡时,甲容器的压强小于乙,所以甲容器需增大压强才能达到乙容器的压强,而增大压强,平衡正向移动,三氧化硫的体积分数增大,所以SO3的体积分数甲<乙;
(3)I、T1温度时A点代表此温度的二氧化硫平衡转化率,D点的二氧化硫的转化率低于A点,说明反应未达平衡,所以v正>v逆;
II、恒温恒容时再向甲容器中通入2molSO2、1molO2,反应物浓度是原来的2倍,在原平衡的基础上,平衡正向移动,正向是气体压强减小的方向,所以达新平衡时压强大于原平衡时的压强但小于两倍原平衡的压强,放出的热量比Q1多,二氧化硫的转化率提高,所以答案选BC;
(4)设充入二氧化硫的物质的量为amol,每消耗2mol 二氧化硫,气体的总物质的量减少1mol,现在气体的物质的量减少0.315mol,说明消耗二氧化硫0.63mol,消耗氧气0.315mol,生成三氧化硫0.63mol,根据恒温下压强之比等于气体物质的量之比,有(a-0.63+0.63+1.1-0.315)/(a+1.1)=82.5%,解得a=0.7,所以SO2的转化率为0.63mol/0.7mol×100%=90%;
(5)二氧化硫与氢氧化钠反应得酸式盐为亚硫酸氢钠,溶液呈酸性,说明HSO3―的电离程度大于水解程度,溶液中离子浓度的大小顺序为 c (Na+)?>c (HSO3―) >c (H+)>c (SO32―)>c (OH―)
(6)溶液中的c (H+)=1×10-5mol/L,平衡时Ka2=6.0×10-3mol/L=c (SO32―)c (H+)/c (HSO3―),所以c (HSO3―)/c (SO32―)="c" (H+)/Ka2=1/6 ×10-2。
本题难度:困难
3、选择题 在密闭容器中进行反应X2(g)+3Y2(g)  ?2Z2(g),若X2、Y2、Z2的起始浓度分别为0.1 mol/L、0.3 mol/L、0.2 mol/L,达到平衡时下列物质的浓度可能为(? )
?2Z2(g),若X2、Y2、Z2的起始浓度分别为0.1 mol/L、0.3 mol/L、0.2 mol/L,达到平衡时下列物质的浓度可能为(? )
A. X2为0.2 mol/L
B. Y2为0.2 mol/L
C. Z2为0.4 mol/L
D. Y2为0.6 mol/L
参考答案:B
本题解析:由于该反应是可逆反应,则反应物或生成物的浓度不可能是0。A中X2为0.2 mol/L,则需要消耗0.2 mol/L的Z2 2,此时生成物的浓度都是0,不可能;同样分析可知,选项CD不可能,因此正确的答案选B。
点评:该题是基础性试题的考查,主要是考查学生对可逆反应特点上完了解掌握情况,旨在培养学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和灵活应变能力。
本题难度:一般
4、填空题 (5分)可逆反应3A(g) 3B(?)+C(?)? △H>0达到化学平衡后,
3B(?)+C(?)? △H>0达到化学平衡后,
(1)升高温度,用“变大”、“变小”、“不变”或“无法确定”填空。
a.若B、C都是气体,气体的平均相对分子质量①?;
b.若B、C都不是气体,气体的平均相对分子质量?② ;
c.若B是气体,C不是气体,气体的平均相对分子质量③ ;
(2)如果平衡后保持温度不变,将容器体积增加一倍,新平衡时A的浓度是原来的60%,则B是④?态,C是⑤?态。
参考答案:①变小?②不变?③变小?④固态或液态?⑤气态(各1分共5分)
本题解析:可逆反应3A(g) 3B(?)+C(?)? △H>0?,
3B(?)+C(?)? △H>0?,
气体的平均相对分子质量=m气体总/n气体总
a.若B、C都是气体,反应前后,气体质量守,而且该反应是气体体积增大的反应,升高温度 ,平衡向正向移动,即向体积增大的方向移动, 所以气体的平均相对分子质量变小。
b.若B、C都不是气体,只有反应物是气体所以反应前后,气体的平均相对分子质量不变。
若B是气体,C不是气体,反应前后,气体质量减少,而气体体积反应前后不变,所以气体的平均相对分子质量变小;如果平衡后保持温度不变,将容器体积增加一倍,如果平衡不再移动,新平衡时A的浓度是原来的50%,但是新平衡时A的浓度是原来的60%,说明平衡向逆反应方向移动,即,减小压强,平衡向体积增大的方向移动,该方向是逆向,所以反应前的气体体积数大于反应后的气体体积数,则B是固态或液态? C是气态。
点评:解答此类试题要求学生对反应前后体积变化的反应,气体的平均相对分子质量是不是变化,要看气体的平均相对分子质量=m气体总/n气体总中气体总质量和气体总的物质的量是不是变化来分析。
本题难度:一般
5、填空题 工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大损害,必须进行处理。常用的处理方法有两种。
方法1:还原沉淀法
该法的工艺流程为:CrO42-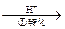 Cr2O72-
Cr2O72- Cr3+
Cr3+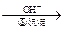 Cr(OH)3↓
Cr(OH)3↓
其中第①步存在平衡:2CrO42-(黄色)+2H+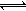 Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O
⑴若平衡体系的pH=2,该溶液显?色。
⑵能说明第①步反应达平衡状态的是? ?。
?。
a. Cr2O72-和CrO42-的浓度相同? b.2v(Cr2O72-)=v(CrO42-)? c.溶液的颜色不变
⑶第②步中,还原1molCr2O72-离子,需要?mol的FeSO4 7H2O。
7H2O。
方法2:电解法
该法用Fe做电极电解含Cr2O72-的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀。
⑷用Fe做电极的原因为?。
⑸在阴极附近溶液pH升高的原因是(用电极反应解释)?,溶液中同时生成的沉淀还有?。
⑹写出Cr2O72--变为Cr3+的离子方程式___________________;
参考答案:
本题解析:略
本题难度:一般