1、选择题 NA表示阿伏加德罗常数,下列说法不正确的是
A.1.8 g的NH+4离子中含有的电子数为NA
B.0.3 mol N2和0.7 mol O2的混合气体在标准状况下的体积约为22.4 L
C.物质的量浓度为0.5 mol/L的MgCl2溶液中,所含Cl-的个数为NA
D.2.4 g金属镁变为镁离子时失去的电子数为0.2NA
参考答案:C
本题解析:A项1.8 g的NH+4离子物质的量是0.1mol,含有的电子为1mol,电子数为NA;B项任何气体包括混合气体在标准状况下1mol体积约为22.4 L;C项没有给出体积,不知道具体的氯离子的物质的量;D项2.4 g金属镁为1mol,失去的电子数为0.2mol。
点评:阿伏加德罗常数是高考常考知识点,综合性强,容量大,需要学生对高中阶段的原子结构、物质结构、物质性质、反应规律等均要掌握清楚,本题属于中等题。
本题难度:一般
2、选择题 设NA为阿伏加德罗常数的数值,下列说法正确的是(?)。
A.1 mol・L-1 NaCl溶液含有NA个Na+
B.1 mol Cu和足量稀硝酸反应产生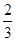 NA个NO分子
NA个NO分子
C.1 L 0.1 mol・L-1氨水含有0.1NA个OH-
D.1 mol Fe2+与足量的H2O2溶液反应,转移2NA个电子
参考答案:B
本题解析:由于没有提供1 mol・L-1 NaCl溶液的体积,则溶液所含Na+数目无法确定,A项错误;根据Cu与稀硝酸的反应:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,则反应生成的n(NO)=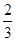 n(Cu),其分子数目为
n(Cu),其分子数目为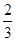 NA,B项正确;C项氨水中的NH3・H2O为弱电解质,不能完全电离,1 L 0.1 mol・L-1氨水中OH-数目小于0.1NA;D项中Fe2+被氧化成Fe3+,1 mol Fe2+转移1 mol电子,即NA个电子。
NA,B项正确;C项氨水中的NH3・H2O为弱电解质,不能完全电离,1 L 0.1 mol・L-1氨水中OH-数目小于0.1NA;D项中Fe2+被氧化成Fe3+,1 mol Fe2+转移1 mol电子,即NA个电子。
本题难度:一般
3、选择题 下列数量的各物质:①0.5molNH3,②标准状况下22.4LHe,③4℃时9mlH2O,④0.2molH3PO4中,所含原子个数由大到小的顺序是( )
A.②③④①
B.④③②①
C.①④③②
D.①④②③
参考答案:C
本题解析:
本题难度:简单
4、选择题 将9.2g金属钠投入到足量水中,得ag溶液;9.6g镁投入到足量盐酸中(与水等质量),得到bg溶液,则反应后两溶液质量的关系是 (?)
A.a>b
B.a=b
C.a<b
D.无法判断
参考答案:B
本题解析:将9.2g金属钠与水反应后生成H2的质量为0.4g;9.6g镁投入到足量盐酸中生成H2的质量为0.8g;设足量盐酸(与水等质量)的质量为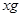 ,则
,则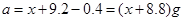 ;
;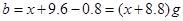 ,因此可得
,因此可得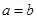 。故答案为B。
。故答案为B。
点评:本题是对物质反应的计算,属于基础题。解题时,对于计算溶液的质量时,应考虑加入的物质(形成溶液),以及“跑出去”的物质(气体),对于形成溶液的,应加;对于生成气体的,应减。
本题难度:一般
5、选择题 NA代表阿伏加德罗常数的数值,下列叙述正确的是(?)
A.在H2O2+Cl2=2HCl+O2反应中,每生成32 g氧气,转移4NA个电子
B.常温常压下,33.6 L Cl2与56 g Fe充分反应,转移电子数为3NA
C.标准状况下分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g
D.在1 L 0.2 mol・L-1的硫酸铁溶液中含有的铁离子数为0.4NA
参考答案:C
本题解析:A、H2O2中O元素是-1价,所以每生成32g氧气,转移2NA个电子,错误;B、常温常压下,气体摩尔体积不为22.4L/mol,所以氯气的物质的量无法计算,错误;C、标准状况下分子数为NA的CO、C2H4混合气体的物质的量为1mol,CO、C2H4的摩尔质量相同都是28g/mol,所以混合气体的质量为28g,正确;D、铁离子水解使铁离子数目小于0.4NA,错误,答案选C。
本题难度:一般