1、填空题 标准状态下质量比为14:15的N2和NO气体,N2和NO的物质的量之比为____________,密度之比为
______________如将其混合氮原子和氧原子的个数比为_________________。
参考答案:1:1;14:15;3:1
本题解析:
本题难度:一般
2、选择题 NA代表阿伏加德罗常数值,下列说法正确的是
A.78gNa2O2所含有的离子数为3NA
B.1mol甲基中含有电子数为10NA
C.7.1g氯气与足量NaOH溶液反应转移的电子数为0.2NA
D.1molC10H22分子中共价键总数为22NA
参考答案:A
本题解析:A:Na2O2所含有的离子为Na+及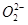 ,个数比2:1,故78gNa2O2(1mol)所含有的离子数为3NA,正确
,个数比2:1,故78gNa2O2(1mol)所含有的离子数为3NA,正确
B:甲基为中性原子团,含有9个电子,故1mol甲基中含有电子数为9NA
C:氯气与碱液发生的是自身氧化还原反应:Cl2+2NaOH=NaCl+NaClO+H2O,只有一个电子转移,故7.1g氯气(0.1mol)与足量NaOH溶液反应转移的电子数为0.1NA
D:1molC10H22分子中共价键总数为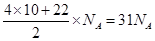
答案为A
本题难度:简单
3、选择题 在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是( )
A.甲的相对分子质量比乙的相对分子质量小
B.甲的摩尔体积比乙的摩尔体积小
C.甲中所含的原子数比乙中的所含的原子数少
D.甲中所含的分子数比乙中的所含的分子数少
参考答案:A、在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则根据ρ=mV可知,甲体积小于乙体积,在同温同压下,物质的量之比等于体积之比,说明甲气体的物质的量小于乙气体的物质的量,所以根据M=mn可知,甲的相对分子质量比乙的相对分子质量大,故A错误;
B、在相同温度和压强下,气体的摩尔体积相等,故B错误;
C、甲体积小于乙体积,在同温同压下,物质的量之比等于体积之比,说明甲气体的物质的量小于乙气体的物质的量,即甲的分子数小于乙,但不能确定甲乙原子数关系,故C错误;
D、甲体积小于乙体积,在同温同压下,物质的量之比等于体积之比,说明甲气体的物质的量小于乙气体的物质的量,即甲的分子数小于乙,故D正确.
故选D.
本题解析:
本题难度:简单
4、选择题 设NA为阿伏加德罗常数,下列说法中正确的是
A.Cl2的摩尔质量与NA个Cl2分子的质量相等。
B.活泼金属从盐酸中置换出1molH2,转移电子数为NA
C.500mL0.5mol・L-1Al2(SO4)3溶液中,含SO42-数目为0.75NA
D.同温同压下,2g H2和22.4LO2所含分子数为NA
参考答案:C
本题解析:A:两者仅数值上相同,但单位不同,不正确
B:由反应2H++2e-=H2↑可知,置换出1molH2,转移电子数为2NA
C:该溶液中SO42-数目为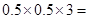 0.75NA
0.75NA
D:非标准状况,无法计算氧气的量,不正确
答案为C
本题难度:一般
5、选择题 下列说法中正确的是
[? ]
A. CO2的摩尔质量为44g
B. 6.02×1022个H2SO4分子的质量为9.8g
C. 标准状况下,22.4L盐酸所含的氯化氢质量为36.5g
D. 同温同压下,无法判断等物质的量的CH4和CO原子个数比
参考答案:B
本题解析:
本题难度:简单