1、选择题 下表中的因果关系完全正确的是
A.A
B.B
C.C
D.D
参考答案:B
本题解析:分析:A.通气后混合液中产生的ClO-被H2O2还原,发生激烈反应,产生能量较高的氧分子,他立即转变为普通氧分子,将多余的能量以红光放出;
B.溶度积小的不溶;
C.氨气与二氧化碳反应生成碳酸铵;
D.硅与浓硫酸和浓硝酸不反应.
解答:A.通气后混合液中产生的ClO-被H2O2还原,发生激烈反应,产生能量较高的氧分子,他立即转变为普通氧分子,将多余的能量以红光放出,体现H2O2的还原性,故A错误;
B.ZnS能溶解在稀盐酸中,CuS不能溶解在稀盐酸中,溶度积小的不溶,则CuS的Ksp比ZnS的Ksp小,故B正确;
C.氨气与二氧化碳反应生成碳酸铵,再与BaCl2溶液反应生成碳酸钡沉淀,氨气为反应物,故C错误;
D.硅与浓硫酸和浓硝酸不反应,硅能与氢氟酸反应,故D错误;
故选B.
点评:本题考查化学实验方案的评价,侧重于考查学生的综合运用化学知识的能力和评价能力,题目难度不大,注意把握相关物质的性质以及实验原理的分析.
本题难度:一般
2、选择题 下列有关实验装置进行的相应实验,能达到实验目的是

A.用图1装置制取乙烯并验证乙烯的性质
B.用图2装置配制银氨溶液
C.用图3装置萃取溴水中的溴,并把溴的苯溶液从下口放出
D.用图4装置验证浓硫酸的脱水性和强氧化性
参考答案:D
本题解析:分析:A.应在浓硫酸作用下制备乙烯;
B.应在硝酸银溶液中滴加氨水;
C.苯的密度比水小;
D.蔗糖在浓硫酸作用下生成碳和二氧化硫气体.
解答:A.制取乙烯,应用乙醇在浓硫酸作用下加热到170℃,并除去乙醇,防止干扰实验现象,故A错误;
B.制备银氨溶液,应在硝酸银溶液中滴加氨水,至沉淀恰好溶解时为止,故B错误;
C.苯的密度比水小,溴的苯溶液从上口倒出,故C错误;
D.蔗糖在浓硫酸作用下生成碳和二氧化硫气体,蔗糖颜色变黑,表现浓硫酸的脱水性,生成气体可使酸性高锰酸钾溶液褪色,说明生成二氧化硫气体,表现硫酸的强氧化性,故D正确.
故选D.
点评:本题考查化学实验方案的评价,涉及物质的制备、分离和检验等实验操作,侧重于物质性质的考查,题目难度不大.
本题难度:简单
3、填空题 以黄铁矿为原料生产硫酸的工艺流程图如下
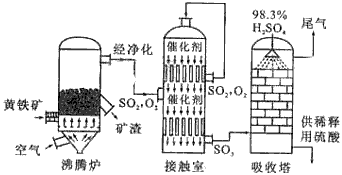
(1)将燃烧黄铁矿的化学方程式补充完整4_______+11O2 2Fe2O3+8SO2
2Fe2O3+8SO2
(2)接触室中发生反应的化学方程式是_________________________。
(3)依据工艺流程图判断下列说法正确的是(选填序号字母)_______________。
a.为使黄铁矿充分燃烧,需将其粉碎
b.过量空气能提高SO2的转化率
c.使用催化剂能提高的SO2反应速率和转化率
d.沸腾炉排出的矿渣可供炼铁
(4)每160gSO3气体与H2O化合放出260.6kJ的热量,该反应的热化学方程是__________________________。
(5)吸收塔排出的尾气先用氨水吸收,再用浓硫酸处理,得到较高浓度的和铵盐。
①SO2既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的Br2。SO2吸收Br2的离子方程式是__________________________。
② 为测定该铵盐中氮元素的质量分数,将不同质量的铵盐分别加入到50.00mL相同浓度的溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量。部分测定结果:铵盐质量为10.00g和20.00g 时,浓硫酸增加的质量相同;铵盐质量为30.00g时,浓硫酸增加的质量为0.68g;铵盐质量为40.00g时,浓硫酸的质量不变。
计算:该铵盐中氮元素的质量分数是________%; 若铵盐质量为15.00g。
浓硫酸增加的质量为__________。 (计算结果保留两位小数)
参考答案:(1)FeS2
(2)2SO2+O2 2SO3
2SO3
(3)abd
(4)SO3(g)+H2O(l)==H2SO4(l);△H=-130.3kg/mol
(5)①SO2+Br2+2H2O==4H++2Br-+SO42-;②14.56;2.31g
本题解析:
本题难度:困难
4、选择题 接触法制硫酸的过程中,对废气、水、渣、热的处理正确的是
①尾气用氨水处理
②污水用石灰乳处理
③废渣用来制水泥、炼铁
④设置热锅炉产生蒸气、供热或发电
A.①②③④都正确
B.只有①②③正确
C.只有②③④正确
D.只有①②④正确
参考答案:A
本题解析:
本题难度:困难
5、选择题 从下列实验事实所引出的相应结论正确的是
A.A
B.B
C.C
D.D
参考答案:A
本题解析:分析:A.反应物浓度越大,反应速率越大;
B.化学反应中,催化剂参与反应过程;
C.醋酸为弱酸,不能完全电离;
D.增大压强,正逆反应速率都增大.
解答:A.当其他条件不变时,增大反应物浓度,活化分子的浓度增大,有效碰撞的次数增多,则反应速率增大,故A正确;
B.化学反应中,催化剂参与反应过程,降低反应的活化能,加快反应速率,但反应前后催化剂的质量和性质不变,故B错误;
C.醋酸为弱酸,不能完全电离,氢离子浓度相同时,醋酸浓度大,与足量的锌反应,生成氢气体积大,故C错误;
D.增大压强,正逆反应速率都增大,故D错误.
故选A.
点评:本题考查较为综合,涉及影响反应速率的实验探究、弱电解质的电离以及催化的作用,题目难度不大,注意相关基础知识的积累.
本题难度:简单