| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
�߿���ѧ֪ʶ��������������ʵ���ƽ�⡷����ǿ����ϰ��2019��Ѻ��棩(��)
�ο��𰸣�A ��������� �����Ѷȣ�һ�� 3������� ��6�֣���֪ij�¶���CH3COOH�ĵ��볣��K=1.6��10-5�����¶�����20mL0.01mol/LCH3COOH��Һ����μ���0.01mol/L KOH��Һ����pH�仯��������ͼ��ʾ�������¶ȱ仯������ش������й����⣺ �ο��𰸣���1��4��l0-4 �����������1��K= �����Ѷȣ�һ�� 4��ѡ���� ����ʱ����pH��6��CH3COOH��Һ��ˮϡ��1000������Һ�е� |
�ο��𰸣�C
�����������pH��6��CH3COOH��Һ��ˮϡ��1000������ҺpH������9����ʱ��Һ�ӽ����ԣ�pH��7����ѡC��
���㣺������ҺPH�ļ��㡣
�����Ѷȣ�һ��
5������� ��16�֣�
��1�������й�ʵ�����������˵���д������?
A��ʵ����������FeCl3��Һʱ���Ƚ�FeCl3����һ������Ũ�����У��ټ�����ˮϡ��������Ũ��
B���ù㷺pH��ֽ����Na2S��Һ��pHʱ����pH=10.5
C���ζ���ϴ��������ˮ��ϴ����ע���Һ�����к͵ζ�ʵ��
D�����������Һ���������������ͨ��һ����HCl����ʱ���������Һ�ɻָ�����ԭ��һ��
��2��������������ʽ���뷽��ʽ��??
��3����������Һ����μ�������������Һ�������Ӹպó�����ȫʱ�����ӷ�Ӧ�ܷ���ʽΪ��?
��4��25��ʱ����0.1mol/L�İ�ˮ�м��������Ȼ�粒��壬�������ܽ�����ҺpH��С����Ҫԭ���ǣ�����ţ�?��
A����ˮ���Ȼ�立�����ѧ��Ӧ
B���Ȼ����Һˮ�������ԣ�������c(H+)
C���Ȼ������ˮ���������������ӣ������˰�ˮ�ĵ��룬ʹc(OH�D)��С
��5�������£������0.1mol NH4Cl��0.05mol NaOHȫ������ˮ���γɻ����Һ(��������ʧ)��?��?�������ӵ����ʵ���֮�ͱ�OH�D��0.05mol��
�ο��𰸣���1��BC ?��2��Al(OH)3?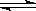 H++AlO2-+H2O
H++AlO2-+H2O
��3��2Al3++3SO42-+3Ba2++6OH- = 3BaSO4 ��+ 2Al(OH)3��
��4��C ?��5��NH4+��H+����4�֣�����Ը��֣�
�����������
�����Ѷȣ�һ��
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ�����л�ѧ֪ʶ���ܽᡶ��ѧ��Ӧ��.. | |
| �����Ŀ |