1���ƶ��� ��10�֣�A��J����ѧ��ѧ���������ʣ�����֮���ת����ϵ����ͼ��ʾ�����ֲ�������ȥ������֪A��һ�ָ��۵����ʣ�D��һ�ֺ���ɫ���塣
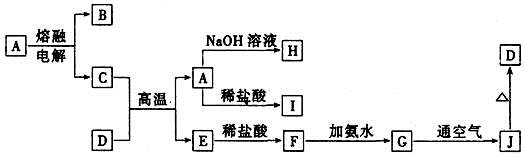
��ش��������⣺�����ƶ����ҵ�ͻ�Ƶ��ǹؼ���A��һ�ָ��۵����ʣ���֪AΪAl2O3��D��һ�ֺ���ɫ���壬��֪DΪFe2O3��BΪO2��CΪAl,EΪFe,FΪFeCl2,GΪFe(OH)2,JΪFe(OH)3��HΪNaAlO2��IΪAlCl3��
��1�����A���ʵ������缫��ӦʽΪ___________��C��D�ڸ����·�Ӧ�������÷�Ӧ��Ҫ�����һ���Լ���____________________(д��ѧʽ)
��2��д��G��J��Ӧ��ʵ�������뻯ѧ����ʽ____________________________________��__________________________________
��3��H ��I��Ӧ�����ӷ���ʽΪ___________________________________________
��4�������ӷ���ʽ��ʾI���������ھ�ˮ��ԭ��___________________________________
�ο��𰸣���1��2O2����4e��=O2? KClO3����1�֣�
��2�����ɵİ�ɫ����Ѹ�ٱ�Ϊ����ɫ���ձ�Ϊ���ɫ
4Fe(OH)2+O2+2H2O=4Fe(OH)3
��3��Al3++3AlO2��+6H2O=4Al(OH)3����4��Al3++ 3H2O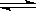 Al(OH)3(����)+ 3H+
Al(OH)3(����)+ 3H+
��������������ƶ����ҵ�ͻ�Ƶ��ǹؼ���A��һ�ָ��۵����ʣ���֪AΪAl2O3��D��һ�ֺ���ɫ���壬��֪DΪFe2O3��BΪO2��CΪAl,EΪFe,FΪFeCl2,GΪFe(OH)2,JΪFe(OH)3��HΪNaAlO2��IΪAlCl3��
��1������ʧȥ���ӣ��缫��ӦʽΪ2O2����4e��=O2��Al��Fe2O3��Ӧ��Ҫ��ȼ��KClO3��
��2��Fe(OH)2��Fe(OH)3�з�����ʵ������̲��к���ϸ�ҳ�����֪ʶ�㣬���ɵİ�ɫ����Ѹ�ٱ�Ϊ����ɫ���ձ�Ϊ���ɫ����ѧ����ʽΪ4Fe(OH)2+O2+2H2O=4Fe(OH)3��
��3��NaAlO2��AlCl3��Ӧ��˫ˮ�ⷴӦ�����ӷ���ʽΪ��Al3++3AlO2��+6H2O=4Al(OH)3����
��4��AlCl3ˮ���ԭ����Al3+����ˮ������Al(OH)3(����)�����������������ӷ���ʽΪ��Al3++ 3H2O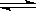 Al(OH)3(����)+ 3H+��
Al(OH)3(����)+ 3H+��
���������⿼��������ת����ϵ��Ӧ�ã��������ʵ�Ӧ�ã���Ҫ�������仯�������������仯�������ʵ��ۺ�Ӧ�ã��ؼ��Ƿ�Ӧ����ͷ�Ӧ������Ӧ���жϣ�������Ӧ�ķ����жϡ�
�����Ѷȣ�����
2���ƶ��� ͼ��X��Y��ZΪ���ʣ�����Ϊ��ѧ�����֮���������ת����ϵ�����ֲ�������ȥ�������У�A�׳ƴ�����������E�Dz�����ˮ�������������������ᷴӦ��
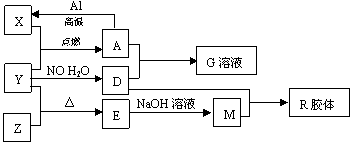
�ش��������⣺
��1����ɵ���Y��Ԫ�������ڱ��е�λ����__________��M�д��ڵĻ�ѧ������Ϊ__________��R�Ļ�ѧʽ��__________��
��2��һ�������£�Z��H2��Ӧ����ZH4��ZH4�ĵ���ʽΪ__________��
��3����֪A��1molAl��Ӧת��ΪXʱ���������ʾ�Ϊ���壩���ų�aKJ������д���÷�Ӧ���Ȼ�ѧ����ʽ��__________________________��
��4��д��A��D��ϡ��Һ��Ӧ����G�����ӷ���ʽ��____________________��
��5����4mol D��ϡ��Һ�У�����X��ĩ���������������ɵ�����ֻ��һ�֣���������ϵ�л���
n(X2+)��n��X���仯��ʾ��ͼ�������n(X2+)�����ֵ��

�ο��𰸣���1���ڶ����ڵڢ�A�壻���Ӽ������ۼ���H2SiO3��H4SiO4����2��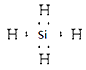 ��3��8Al(s)��3Fe3O4(s)��9Fe(s)��4Al2O3(s) ��H��-8aKJ/mol
��3��8Al(s)��3Fe3O4(s)��9Fe(s)��4Al2O3(s) ��H��-8aKJ/mol
��4��3Fe3O4��28H+��NO3-=9Fe3+��14H2O��NO��?��5��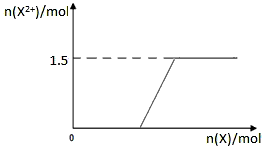
���������
�����Ѷȣ�һ��
3���ƶ��� A��B��CΪ������Ҫ�Ĺ�ҵԭ�ϣ���ɫ��Ӧ��Ϊ��ɫ������A�������Ƹ�㣬B������ȥ�����ۣ�����֮���ת����ϵ����
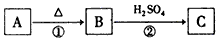
��ش�
(1)��Ӧ�ٵĻ�ѧ����ʽ��__________________��
(2)B��ˮ��Һ��c(H+)______c(OH-)(�>����<��)��ԭ����____________(�����ӷ���ʽ��ʾ) ��
(3)��B��ˮ��Һ�еμ�BaCl2��Һ���а�ɫ�������ɡ������ó����ֳ����ݣ�һ���еμӹ���HNO3��������__________________����Ӧ�����ӷ���ʽ��__________________����һ�����ȼ������C����Һ��������˺����������ٵμӹ�����HNO3���������ܽ⣬��Ӧ�����ӷ���ʽ��____________��
�ο��𰸣�(1)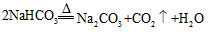
(2)<��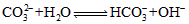
(3)��ɫ�����ܽ⣬�����ݲ�����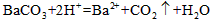 ��
��
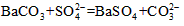
���������
�����Ѷȣ�һ��
4������� W��X��Y��ZΪԭ������������������ֶ���������Ԫ�أ�����W��һ��ԭ�Ӻ���û�����ӣ�Y��ԭ�����������������ڲ��������3����Y��Z���γ����ֳ��������ӻ�����Z2Y��Z2Y2��X��Y���γ����ֻ��������Է�������֮��Ϊ7��11����ش�
��1��Z��Ԫ�����ڱ��е�λ����______��
��2��X��Z��Ԫ��ԭ�ӵĴ���������֮��Ϊ______��
��3���õ���ʽ��ʾ������W2Y���γɹ���______��
��4����W��X����Ԫ����ɵ���ѧ��ѧ����������ף�����Է�������Ϊ78���ײ����ܷ����ķ�Ӧ��______������ţ���
����������Ӧ��?����������Ӧ������Һ�巴Ӧ��?�������Ը��������Һ��Ӧ
��5����W��X��Y����Ԫ����ɵ��л����ң���Է�������Ϊ60����W��X��Y��Z����Ԫ����ɵ����������Է�������Ϊ84�������ֽ⣮��֪�������Ӧ�ܷų����壬д������Һ�����Һ��Ӧ�����ӷ���ʽ��______��
�ο��𰸣�W��X��Y��ZΪԭ������������������ֶ���������Ԫ�أ�W��һ��ԭ�Ӻ���û�����ӣ���WӦΪHԪ�أ�
Y��ԭ�����������������ڲ��������3������������Ӳ�������ֱ�Ϊ2��6��ӦΪOԪ�أ�
Y��Z���γ����ֳ��������ӻ�����Z2Y��Z2Y2����ZΪNaԪ�أ��γɵĻ�����ֱ�ΪNa2O��Na2O2��
X��Y���γ����ֻ��������Է�������֮��Ϊ7��11����Է��������ֱ�Ϊ28��44��ӦΪCO��CO2��XΪCԪ�أ�
��1��ZΪNaԪ�أ�ԭ������Ϊ11��ԭ�Ӻ�����3�����Ӳ㣬����������Ϊ1����Ӧ�����ڱ��������ڢ�A�壬�ʴ�Ϊ���������ڢ�A�壻
��2��X��Z�ֱ�ΪC��Na����������������ֱ�Ϊ2��8������Ԫ��ԭ�ӵĴ���������֮��Ϊ2��8=1��4���ʴ�Ϊ��1��4��
��3��W2YΪH2O�����ڹ��ۻ�����õ���ʽ��ʾ���γɹ���Ϊ
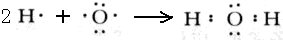
��
�ʴ�Ϊ��
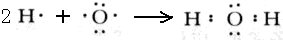
��
��4����W��X����Ԫ����ɵ���ѧ��ѧ����������ף�����Է�������Ϊ78��ӦΪ���������ȶ������������Ը��������Һ��Ӧ���ڴ�������������ȡ����Ӧ����ȼ�գ��ܼӳɣ��ʴ�Ϊ���ܣ�
��5����W��X��Y����Ԫ����ɵ��л����ң���Է�������Ϊ60��ӦΪCH3COOH��Ϊ���ᣬ��W��X��Y��Z����Ԫ����ɵ����������Է�������Ϊ84�������ֽ⣬���ΪNaHCO3��
���߷�Ӧ�����ӷ���ʽΪCH3COOH+HCO3-�TCH3COO-+CO2��+H2O��
�ʴ�Ϊ��CH3COOH+HCO3-�TCH3COO-+CO2��+H2O��
���������
�����Ѷȣ�һ��
5������� ��A��B��C���ֳ����Ľ������ʣ�A�ڿ�����ȼ�����ɵ���ɫ���壻BҲ���ڿ����о���ȼ�գ�����ҫ�۵İ⣻C��һ����������ˮ������Ӧ����H2��һ�ֺ�ɫ���塣����������Ϣ�ش��������⣺
(1)д����ѧʽA??B??C??
(2)д��ѧ����ʽ��A�ڿ�����ȼ��?
��C��ˮ������Ӧ?
��A��ˮ��Ӧ?
�ο��𰸣�(1)A? Na??B? Mg??C? Fe??
(2)��? ?
?
��?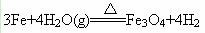 ?
?
��? 2Na+2H2O===2NaOH+H2��?
�����������
�����Ѷȣ���