1、选择题 实验是化学研究的基础,如图所示的实验操作正确的是
A.干煤SO2
B.实验室制取并收集O2
C.装置气密性的检查
D.吸收NH3
参考答案:C
本题解析:分析:A、二氧化硫是酸性氧化物和碱反应;
B、氧气是比空气重的气体,用向上排气法收集;
C、装置气密性主要是利用装置中压强变化和液面变化分析判断;
D、氨气和硫酸反应生成硫酸铵易发生倒吸;
解答:A、二氧化硫是酸性氧化物和碱反应,通过碱石灰被吸收,不能用来干燥,故A错误;
B、氧气是比空气重的气体,应用向上排气法收集,故B错误;
C、装置中注射器推入压强增大,液体在长颈漏斗中上升,说明气密性完好,故C正确;
D、硫酸吸收氨气反应会引起倒吸,故D错误;
故选C.
点评:本题考查了化学实验方案的正误判断,气体收集,干燥净化,气密性检查方法判断,题目难度中等.
本题难度:困难
2、填空题 乙二酸和乙二醇在不同条件下反应,会生成三种不同的酯,其中普通酯是一个乙二醇分子跟一个乙二酸分子反应生成的分子式为C4H6O5的酯,另一种是分子式为C4H4O4的环状酯,还有一种高分子酯,试写出它们的结构简式:
(1)普通酯_________________________________________________。
(2)环状酯__________________________________________________。
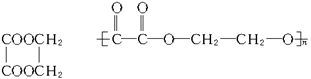
(3)高分子酯________________________________________________。
参考答案:HOOC―COOCH2CH2OH
本题解析: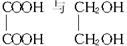 均有两个官能团,两分子间可脱一分子水生成HOOC―COOCH2CH2OH,可脱两分子水生成
均有两个官能团,两分子间可脱一分子水生成HOOC―COOCH2CH2OH,可脱两分子水生成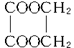 ;n个
;n个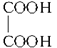 与n个
与n个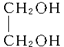 分子间可脱2n分子水生成
分子间可脱2n分子水生成
本题难度:简单
3、选择题 下列叙述正确的是( )
A.常温下,浓硫酸不与铜反应,是因为铜被钝化
B.可用铁罐来进行贮存、运输冷的浓硫酸
C.SO3具有氧化性,SO2只有还原性
D.SO2、Cl2的漂白原理相同
参考答案:A.常温下,Fe、Al遇浓硫酸或浓硝酸发生钝化,铜属于金属性较不活泼的金属,浓硫酸和铜须在加热的条件下反应,常温下不反应不属于钝化,故A错误;
B.常温下金属Fe与浓硫酸发生钝化反应,会在金属表面形成致密的氧化膜,阻止反应进一步发生,可用铁罐来进行贮存、运输冷的浓硫酸,故B正确;
C.SO3中硫+6价,为硫的最高价,所以只具有氧化性,SO2中硫+4价,处于中间价态,所以既具有还原性,又具有氧化性,如SO2通入饱和H2S溶液中析出浅黄色沉淀,反应生成S,SO2中S元素的化合价降低,具有氧化性,SO2通入氯水使之褪色,反应生成硫酸和盐酸,S元素的化合价升高,说明SO2具有还原性,故C错误;
D.氯气漂白,实际上是氯气与水反应生成的次氯酸具有强氧化性,起漂白作用,二氧化硫漂白原理是二氧化硫与水生成的亚硫酸和有机色素结合为不稳定的无色物质,两者原理不同,故D错误;
故选B.
本题解析:
本题难度:简单
4、实验题 (14分)某校化学小组学生利用下图所示装置进行“乙二酸(俗名草酸)晶体受热分解”的实验,并验证分解产物中有CO2和CO(图中夹持装置已略去)。(已知草酸钙难溶于水,草酸沸点150℃)
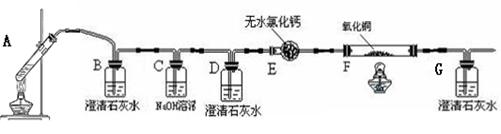
(1)装置C的作用是______________________,装置E的作用是 _____________________
(2)乙二酸受热分解的反应方程式是?
(3)①证明分解产物中有CO2的现象是??
②证明分解产物中有CO的现象是?
(4)该装置有不足之处,请写出弥补不足之处的理由和具体方法:
? ?
?
参考答案:

本题解析:略
本题难度:一般
5、选择题 下图小试管中盛有几毫升水,与大试管连通的U型细玻璃管内放有少量水(已染成红色)。如沿小试管壁小心地慢慢注入3?mL浓硫酸,静置片刻后,U型细玻璃管中可观察到的液面现象是?
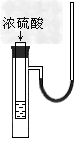
[? ]
A.?左高右低?
B.?左低右高
C.?左右一样高?
D.?来回振动
参考答案:B
本题解析:
本题难度:简单