1��ѡ���� ���й��ڡ���ɫ��Ӧ����������ȷ����? (? )
A��ֻ�н������ʲ�����ɫ��Ӧ��
B��ֻ�н��������������ɫ��Ӧ
C��ֻ��ijЩ�������仯���������ɫ��Ӧ
D��ֻ�н������Ӳ�����ɫ��Ӧ
�ο��𰸣�C
�����������ɫ��Ӧ��ijЩ���������ǵĻ���������ɫ����������ʱʹ���������������ɫ�ķ�Ӧ����ѡC
�����Ѷȣ���
2��ѡ���� ��������ѧ����ָ�ü�ͥ������Ʒ�����л�ѧʵ�飬�Ӷ��Ի�ѧ����ѧϰ��̽���Ļ������ʵ���ڡ�������ѧ���в�����ɵ���
A����������ˮ�к���Cl �C
B������ʳ���в����ⵥ��
C���������ڼ��������·�������
D�����鵰���ʿ������ڴ���
�ο��𰸣�A
�����������������ˮ�к���Cl �C��Ҫ������������Һ����Ȼ����ɣ�����ǿ��Եģ���ѡA��
�����Ѷȣ���
3��ѡ���� ������ʵ��װ�ý�����Ӧʵ�飬�ܴﵽʵ��Ŀ�ĵ���(����)

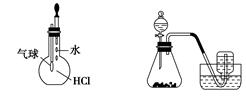
�ס����������������ҡ�����?����������������������
A��װ�üף���ȥ��ϩ�л��е�����SO2
B��װ���ң���Ũ��������1 mol/L������
C��װ�ñ�������HCl������ˮ�е��ܽ���
D��װ�ö�����ͭ��Ũ���ᷴӦ��ȡNO2
�ο��𰸣�C
���������A���ϩҲ�ܱ����Ը��������Һ������Ӧ������������Һ��ȥ��ϩ�е�SO2������B�Ũ�����ϡ��Ӧ���ձ��н��У�����ƿ��������������Һ������C�HCl��������ˮ��ѹǿѸ�ټ�С�������ģ���ȷ��D�NO2��������ˮ���ռ�������
�����Ѷȣ�һ��
4������� ��°��������ҹ����������Ļ���ר�ң������Ƽ���������ش��ף����������������Ƽ�����������Ƽ������ͼ����ʵ������ģ�⡰�����Ƽ������ȡ̼������һ����ʵ��װ�ã�ʵ�鲽��Ϊ��
�����Ӻ�װ�ã����������ԣ���������װ��ҩƷ��
���ȴ�D�ķ�Һ©������������Ũ��ˮ��ֱ�����������岻������C�еı���NaCl��Һ���ܽ�ʱ����ͨ��A�в��������壮Ƭ�̺��ձ���������ɫ���壨̼�����ƣ���������C��ͨ���������壬ֱ�������й������Ϊֹ��
�۹����ձ������õĻ����õ�̼�����ƹ��壮
������Һ�м����������Ȼ��ƹ��壬������Ӧ��
NaCl��s��+NH4Cl��aq��=NaCl��aq��+NH4Cl��s�����������ˣ��˳�����������ʣ�
����Һ��ע���ձ�C�У��ظ�ʹ�ã�������һ���Ʊ���
�Իش��������⣺
��1������װ��A�����Եķ�����______��
��2���ձ�C�з�����Ӧ�Ļ�ѧ����ʽΪ______��
��3��A�г�ѡ�õĹ���Ϊ______��B��Ӧѡ�õ�Һ��Ϊ______��
��4��������б�������D�з�����Ӧ���������������A�з�����Ӧ�������壬ԭ����______��
��5����������ڽϸ��¶ȣ���60�棩�»����ڽϵ��¶��£���0�桫10�棩�½��к��ʣ�______����ϸߡ��ϵ͡���
��6������������õ��Ȼ�茶����г������������Ȼ��ƺ�̼�����ƣ�Լռ5%��8%��������Ƽ�ʵ��֤�����ù���ijɷִ����Ȼ�泥���Ҫд����������������ͽ��ۣ�______��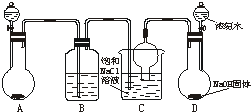
�ο��𰸣���1������װ�������ԣ���Ҫ������װ���ڵ�ѹǿ�仯���жϣ�������סװ��A����ƿ�����ȣ�������Bƿ�в����ܿں�C����߲����ܿ�������ð���������ÿ����������ڲ��γ�һ��ˮ����˵��װ��A����벿�����������ã�
�ʴ�Ϊ��������סװ��A����ƿ�����ȣ�������Bƿ�в����ܿں�C����߲����ܿ�������ð���������ÿ����������ڲ��γ�һ��ˮ����˵��װ��A����벿�����������ã�
��2���ձ�C�з�����Ӧ�Ƕ�����̼�Ͱ���ͨ�뱥���Ȼ�����Һ�з�Ӧ����̼�����ƾ�����Ȼ�淋ķ�Ӧ����ѧ����ʽΪ��NH3+CO2+H2O+NaCl=NaHCO3��+NH4Cl��
�ʴ�Ϊ��NH3+CO2+H2O+NaCl=NaHCO3��+NH4Cl��
��3��Aװ�����Ʊ�������̼����ķ�Ӧ�����Թ���ΪCaCO3�����ɵĶ�����̼�����к����Ȼ��⣬������ȥ̼�����������γɣ�����Ӧ�ñ���̼��������Һ���Ȼ�����Һ��ȥ��
�ʴ�Ϊ������NaHCO3��Һ��ˮ��ʳ��ˮ��
��4��������б�������D�з�����Ӧ���������������A�з�����Ӧ�������壬��ΪNH3��ˮ�е��ܽ�ȱ�CO2����ͨNH3���������ո����CO2���Ӷ����ɸ����NaHCO3��
�ʴ�Ϊ��NH3��ˮ�е��ܽ�ȱ�CO2����ͨNH3���������ո����CO2���Ӷ����ɸ����NaHCO3��
��5�������������Һ�м����������Ȼ��ƹ��壬������Ӧ��NaCl��s��+NH4Cl��aq��=NaCl��aq��+NH4Cl��s�����¶�Խ���Ȼ�淋��ܽ�����������Ȼ�淋ľ�������������Ӧ���¶Ƚϵ�?�������������Ȼ�茶��壬�ʴ�Ϊ���ϵͣ�
��6������������õ��Ȼ�茶����г������������Ȼ��ƺ�̼�����ƣ�Լռ5%��8%������Ƽ�ʵ��֤�����ù���ijɷִ����Ȼ�泥��������Ȼ�淋ķֽ����Ϊ���壬�¶Ƚ��Ͱ������Ȼ���������������ɹ����Ȼ���������Ϊ��ȡ������Ʒ���Թ��У��þƾ��Ƽ��ȣ������Թ��϶��а������ɣ����Թܿ��а�ɫ���壩�����ʣ�༫�����Ĺ��壬�Ӷ�֤�����ù���ijɷִ����Ȼ�泥�
�ʴ�Ϊ��ȡ������Ʒ���Թ��У��þƾ��Ƽ��ȣ������Թ��϶��а������ɣ����Թܿ��а�ɫ���壩�����ʣ�༫�����Ĺ��壬�Ӷ�֤�����ù���ijɷִ����Ȼ�泥�
���������
�����Ѷȣ�һ��
5��ѡ���� ������ʵ�鷽���ܴﵽҪ�����
A����������ƽ����25.20g NaCl����
B����10mL��Ͳ��ȡ2.5mLϡ����
C�����ձ�ȷ����150mL 0.1mol/L��������Һ
D��������ƿ������Һ�ж���ʱ��������ˮ�����������ý�ͷ�ι�����������Һ
�ο��𰸣�B
���������������ƽ����Ͳ������ֻ�ܹ�����һλС�������ų�A���ձ��Ǵ�����ȡ��Һ���������������ȷ��ȡ��Һ���ų�C��������Һ������ʱ����ˮ������ֻ���������ƣ��ų�D����ΪB
�����Ѷȣ���