| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点讲解《常见的化学电源》考点特训(2019年冲刺版)(八)
 (3)1g的氢气完全燃烧生成液态水释放出142.9kJ的热量写出其完全燃烧的热化学方程式:?。 (4)利用氢气和CO合成二甲醚的三步反应如下: ① 2H2(g) + CO(g)  ?CH3OH(g);ΔH =-90.8 kJ・mol-1 ?CH3OH(g);ΔH =-90.8 kJ・mol-1② 2CH3OH(g)  ?CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ・mol-1 ?CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ・mol-1③ CO(g) + H2O(g)  ?CO2(g) + H2(g);ΔH=-41.3 kJ・mol-1 ?CO2(g) + H2(g);ΔH=-41.3 kJ・mol-1总反应:3H2(g) + 3CO(g)  ?CH3OCH3(g) + CO2 (g)的ΔH=? ?CH3OCH3(g) + CO2 (g)的ΔH=?(5)氢氧燃料电池能量转化率高,具有广阔的发展前景。现用氢氧燃料电池进行下图所示实验:  ①氢氧燃料电池中,正极的电极反应式为?。 ②上图装置中,某一铜电极的质量减轻3.2g,则 a 极上消耗的O2在标准状况下的体积为 ?L。 (6)有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制取新型燃料电池。则正极电极方程式?。 参考答案:20.(15分) 本题解析:1、电解水消耗了大量的电力,锌和稀硫酸反应制得氢气量少,分解天然气也需要消耗大量的能源。?光解海水只需要太阳能就可以了既经济又环保。 本题难度:一般 2、选择题 某蓄电池放电、充电的反应式为:Fe+Ni2O3+3H2O ①放电时,Fe为正极,Ni2O3为负极; ②充电时,阴极上的电极反应式是:Fe(OH)2+2e-=Fe+2OH-; ③充电时,Ni(OH)2为阳极; ④蓄电池的电极必须浸在某碱性溶液中. A.①②③ B.①②④ C.①③④ D.②③④ 参考答案:①、由放电时的反应可以得出铁做还原剂失去电子,Ni2O3做氧化剂得到电子,即正极为Ni2O3、负极为Fe,故①错误; 本题解析: 本题难度:一般 3、选择题 ?“纸质电池”于2006年被美国《时代》周刊评为年度8大最佳创新技术之一。这种“软电池”采用薄层纸片作为载体和传导体,在一边附着锌,在另一边附着二氧化锰。电池总反应为: 参考答案:B 本题解析:略 本题难度:一般 4、选择题 如图是一种航天器能量储存系统原理示意图.下列说法正确的是( ) |
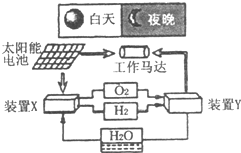
参考答案:A、装置X每消耗1molH2O,可生成1molH2,0.5molO2,共1.5mol,体积为33.6L,故A错误;
B、存在能量转化形式有太阳能、机械能、化学能、电能,则不只是三种,故B错误
C、装置Y为燃料电池,氧气在正极得电子被还原,电极反应式是:4OH--4e-=2H2O+O2↑,故C正确;
D、在装置X中,电解水生成H2、O2,实现了电能与化学能的转化;在装置Y中构成燃料电池,化学能转化为电能,作用于马达实现了电能与机械能的转化,故D错误.
故选C.
本题解析:
本题难度:简单
5、选择题 固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的。它以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应,下列判断正确的是
[? ]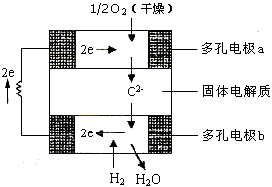
A.有O2放电的a极为电池的负极
B.有H2放电的b极为电池的正极
C.a极对应的电极反应为O2+2H2O+4e- = 4OH-
D.该电池的总反应方程式为
参考答案:D
本题解析:
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学试题《有机物燃烧规律的.. | |