1��ѡ���� �ö��Բ������缫���ֱ����������ʣ�����ͬ����ʱ������ָ���ĵ缫�������������������ǣ�������
A�����ڵ�NaCl��������
B��NaCl��Һ��������
C��NaOH��Һ��������
D��Na2SO4��������
�ο��𰸣�A��������ڵ�NaClʱ��������ӦΪ��2Cl--2e-=Cl2������ת��1mol����ʱ���������������ʵ�����0.5mol��������36.5g��
B�����NaCl��Һʱ�������Ϸ����缫��Ӧ��2H++2e-=H2������ת��1mol����ʱ���������������ʵ�����0.5mol��������1g��
C���������������Һ�������Ϸ����缫��Ӧ��2H++2e-=H2������ת��1mol����ʱ���������������ʵ�����0.5mol��������1g��
D�������������Һ�������ϵĵ缫��ӦΪ��4OH--4e-�T2H2O+O2������ת��1mol����ʱ���������������ʵ�����0.25mol��������8g��
���Ե���ͬ����ʱ��ָ���ĵ缫��������������������A��
��ѡA��
���������
�����Ѷȣ�һ��
2������� �ڰ���ͼװ�ý��е��Ĺ����У�ͨ��һ��ʱ��������ձ������缫���������ӣ�
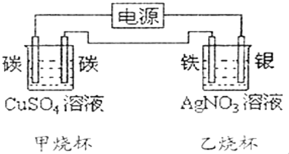
��1�����ձ��У����������ĵ缫��Ӧ��������______��������______
��2�����ձ��з�����Ӧ�Ļ�ѧ����ʽ�ǣ�______
��3��������̼-̼-��-���ĸ��Ǽ����������ܽ����ʵ����ʵ���֮����______��
�ο��𰸣���1��ͨ��һ��ʱ��������ձ������缫���������ӣ��������������������������������Һ����������Һ������ԭ���ǵ��ԭ���������缫��ӦΪ��Ag++e-=Ag�������缫��ӦΪ��Ag-e-=Ag+���ʴ�Ϊ��Ag++e-=Ag��Ag-e-=Ag+��
��2�����ձ��к������ӵ�Ϊ��������ߵ�̼�����������������ͭ��Һ����ͭ�����������ᣬ��ط�ӦΪ��2CuSO4+2H2O?ͨ��?.?2Cu+O2��+2H2SO4��
�ʴ�Ϊ��2CuSO4+2H2O?ͨ��?.?2Cu+O2��+2H2SO4��
��3�����������缫��ӦΪ2Cu2++4e-=2Cu�������缫��ӦΪ4OH--4e-=2H2O+O2�����ҳ��е缫��Ӧ�������缫��ӦΪ4Ag-4e-=4Ag+�������缫��ӦΪ4Ag++4e-=4Ag�����ݵ����غ����õ���������̼-̼-��-���ĸ��Ǽ����������ܽ����ʵ����ʵ���֮����2��1��4��4���ʴ�Ϊ��2��1��4��4��
���������
�����Ѷȣ�һ��
3��ѡ���� 1L?1mol?L-1?AgNO3��Һ����Ag��������Fe�������ĵ����е�⣬����������2.16gʱ�������ж��в���ȷ���ǣ�������
A����Һ��Ũ����Ϊ?1?mol?L-1
B�������ϲ���112?mL?����״���£�?O2
C��ת�Ƶĵ�����ԼΪ1.204��1022��
D����Ӧ����0.02?mol����������
�ο��𰸣�Ag����������������ӦʽΪAg-e-=Ag+��AgNO3��ҺΪ�������Һ������������Ag++e-=Ag��
A��������������֪���ù���Ϊ��ƣ��������Һ��Ũ�Ȳ��䣬��A��ȷ��
B��������ӦʽΪAg-e-=Ag+������������������B����
C��n��Ag��=2.16g108g/mol=0.02mol����ת�Ƶĵ�����ԼΪ0.02��6.02��1023=1.204��1022������C��ȷ��
D����n��Ag��=0.02mol��������ӦʽΪAg-e-=Ag+����������Ag++e-=Ag����Ӧ����0.02?mol��������������D��ȷ��
��ѡB��
���������
�����Ѷȣ���
4������� �����̿���Ҫ�ɷ�ΪMnO2)�Ʊ�KMnO4��ʵ�����̿ɱ�ʾ���£�
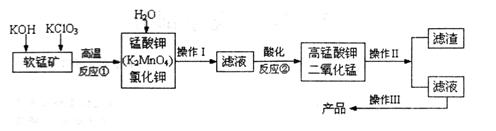
(1)�������������____________��
(2)��ѭ�����õ�����____________(�ѧʽ����
(3)��Ӧ�ڵIJ����У����������뻹ԭ��������ʵ���֮����______��
(4)��Ӧ���С��ữ��ʱ����ѡ���������е�______(����ĸ��ţ�
A��ϡ����?B��ϡ����?C��ϡ����
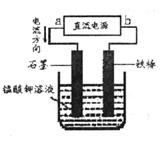
(5)����������ҺҲ���Եõ�������أ���������ӦʽΪ��2H2O+2e-=2OH-+H2��������ͼ��b��____________�������ص�������Ӧʽ��____________�������������ռ���2.24L H2(��״��������õ������� ��____________�ˡ�(��ʾ�������ӷŵ�˳��MnO42->OH-��
�ο��𰸣���16�֣�
��1������?��2�֣�
��2��MnO2?��2�֣�
��3��2:1?��2�֣�
��4��A?��2�֣�
��5����?��2�֣���MnO42-��e-=MnO4-?��3�֣���31.6?��3�֣�
����������������������Ĺؼ���Ҫ���������ʲô���ʣ�����ʲô��Ӧ����η���ȣ�ͨ������������Ҫ�ܹ���һ�����յ�����ת��Ϊ���ʵ����̡���һ����KOH��KClO3��MnO2��Ӧ���õ�K2MnO4���Ӷ�����д����Ӧ����ʽΪ6KOH+3MnO2+KClO3=3K2MnO4+KCl+3H2O��Ȼ�����ˮ�ܽ������������ʣ��õ�K2MnO4��KCl���ڶ���������Һ�ữ���õ�������غͶ������̣�Ϊһ�绯��Ӧ���̴�+6��Ϊ+7��+4����Ӧ����ʽΪ3MnO42-+4H+=2MnO4-+MnO2+2H2O��ͨ�����˷���MnO2���������Һ�����յõ���Ʒ������������MnO2����ѭ�����á�
��4����������������������ǿ�����ԣ�����ʹ�����ᣨ���л�ԭ�ԣ���
��5����Ϊ���Ե�⣬����û�в��뷴Ӧ�����������븺����������������������Ӧ�������ʧ�������ɸ�����������ݵ��ӵ�ʧ�غ���Խ�����ؼ��㡣
�����Ѷȣ�����
5��ѡ���� ��ͼ��ʾ��������װ������ͭ��Һ��ѡ�ò�ͬ���ϵĵ缫���е�⡣�±���˵����ȷ����

?
| �缫����
| ͨ���ı仯
|
����
| ����
|
A
| ʯī
| ʯī
| �����������ӣ���Һ��pH����
|
B
| ͭ
| ͭ
| ������������������������
|
C
| ��
| ��
| �����������������仯
|
D
| ��
| ��
| �����������ӣ���Һ��Ũ�Ȳ���
�ο��𰸣�B
�������������ʯī��Ϊ�缫�������ͭ��Һ��������OH���ŵ������������Һ�ļ��Լ�����pH���ͣ�����Cu2���ŵ�����ͭ��A����ȷ������ͭ�缫�������ͭ��Һ�������ڴ�ͭ���ᴿ��ѡ��B��ȷ���������缫�������ͭ��Һ������Cu2���ŵ�����ͭ��������ʧȥ���Ӷ��ܽ⣬C����ȷ�����ò������������������������ͭ��Һ����Ȼ������Cu2���ŵ�����ͭ��������ʧȥ���Ӷ��ܽ⣬����Һ��Cu2��Ũ�ȼ�С��Fe2������DҲ����ȷ��
�����Ѷȣ�һ��
|