1��ѡ���� ��ѧ��Ӧ�У���ʱ���ڡ�һ�����ʹ�������һ�������Բ�����ȫ��Ӧ������������з�Ӧ����������������ǣ�������
A��������MnO2��Ũ���ᷴӦ
B��������Zn��18?mol/L�����ᷴӦ
C��������Br2��FeI2��Ӧ
D��������H2��N2�ڴ��������·�Ӧ
�ο��𰸣�A���������MnO2��Ũ���ᷴӦʱ���淴Ӧ�Ľ��У�Ũ�����Ϊϡ���ᣬ��ϡ������������̲���Ӧ�����߾���ʣ�࣬��Aѡ��
B��Zn��Ũ�����ϡ������ɷ�Ӧ���������Zn��18?mol/L�����ᷴӦ����������ȫ��Ӧ����B��ѡ��
C��������ֻ���������ӣ��������ܽ������ӡ���������ȫ��������������Br2��FeI2��Ӧ��FeI2����ȫ��Ӧ����C��ѡ��
D��H2��N2�ڴ��������µķ�ӦΪ���淴Ӧ����Ӧ�ﲻ����ȫת��Ϊ��������߾�ʣ�࣬��Dѡ��
��ѡAD��
���������
�����Ѷȣ�һ��
2������� ����ݹ�ҵ��������й�֪ʶ�ش��������⣺
��1���������ڷ���¯�з�Ӧ�Ļ�ѧ����ʽΪ______��
��2�������Ṥҵ�����У�Ϊ��������SO2��ת�������ܳ���������ܣ��������м����Ƚ������ĽӴ��ң���ͼ���������ܱ���ϵ���������������R�������������г�N2�����Ҫ���Ϊ______
������ţ���
A��SO2
B��SO2��SO3
C��SO2��O2
D��SO2��O2��SO3
��3���Ӵ�������������У���Ӧ2SO2��g��+O2��g��
2SO3��g����H��0
�������й�ͼ����ȷ����______��ע��T2��T1��P2��P1������ţ���

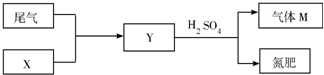
��4����ͼ�ǹ�ҵ������β�����ۺ����ã�����M���պ�ɽ���Ӵ���ѭ�������������ͼʾ�ж�X�ǣ������ƣ�______��д��Y�����ᷴӦ����M�Ļ�ѧ����ʽ______��

�ο��𰸣���1������ʯ�ڷ���¯�� ȼ�����ɶ������������������Ӧ�Ļ�ѧ����ʽΪ��4FeS2+11O2?����?.?2Fe2O3+8SO2���ʴ�Ϊ��4FeS2+11O2?����?.?2Fe2O3+8SO2��
��2������������ܣ�ʹ��Ӧ�ų�������ͨ���Ƚ���������ͨ��Ķ�������Ϳ������ڴ������淴Ӧ������R�������������г�N2�����Ҫ���Ϊ���������������
�ʴ�Ϊ��C��
��3����Ӧ2SO2��g��+O2��g������.��2SO3��g����H��0����Ӧǰ�����������С����Ӧ�Ƿ��ȷ�Ӧ��T2��T1��P2��P1�����ݻ�ѧƽ���ƶ�ԭ������ѡ�
A���ȹ���ƽ���¶ȸߴﵽƽ����Ҫ��ʱ��̣�����T2��T1�������Ƕ��������ת���ʣ���Ӧ���ȣ��¶�Խ��ƽ��������У���������ת���ʼ�С����A��ȷ��
B��ͼ���ж�һ�����ѹǿһ�����¶�Խ��ƽ�����������������ĺ���Լ�٣��¶�һ����ѹǿԽ��ƽ��������У�����������Խ��ͼ�����Ҫ��B��ȷ��
C��T2��T1���¶����ߣ������������淴Ӧ���ʶ�����ƽ��������У�ͼ��������Ӧ���ʴ���C����
D��ѹǿԽ������Խ��Ӧ�����������С�ķ�Ӧ������Ӧ��������ı��淴Ӧ��������Ķ࣬ƽ��������У���D����
�ʴ�Ϊ��AB��
��4������β����Ҫ�Ƕ����������壬�������̹�ϵ��β����X��������Y��Y�����ᷴӦ���ɵ����ƶ�YΪ��Σ����ԺͶ�������Ӧ������ε�X�ǰ�ˮ�����ɵ�YΪ������炙���������泥���Ӧ�Ļ�ѧ����ʽΪ����NH4��2SO3+H2SO4�T��NH4��2SO4+H2O+SO2�����ʴ�Ϊ����ˮ����NH4��2SO3+H2SO4�T��NH4��2SO4+H2O+SO2����
���������
�����Ѷȣ�һ��
3������� �����ǹ�ҵ��������Ϊ��Ҫ�IJ�Ʒ֮һ��
(1)��ҵ����������Ҫ��Ϊ_________��__________��__________�����Ρ�
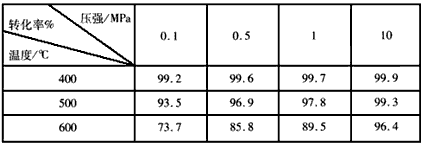
(2)�����ǵڶ��η�Ӧ���й�ʵ�����ݣ���ѡ������ʵ���������_______________��
(3)������߷�Ӧ���ʺ�SO2��ת���ʣ����д�ʩ���е���_________������ţ���
A����װ����ͨ�뵪���ұ����������
B����װ����ͨ�������ұ����������
C�����Ӹ���Ĵ���
D�������¶ȣ���ʱת��SO3
(4)����������β���к�������SO2������ʯ��ˮ���պ��������ᴦ�����˹����漰�Ļ�ѧ��Ӧ����ʽΪ_______________________��___________________��
(5)������ڶ��Σ��豸��������������Ϊ7%SO2��11%O2��82%N2������100��������Ļ�������ڷ�Ӧ���Ϊ96.7�������Ӧ����������N2��SO3�������Ϊ______����ʱSO2��ת����Ϊ______��
�ο��𰸣�(1)������������������
(2)400�桢0.1MPa(��ѹ)
(3)B
(4)SO2+Ca(OH)2=CaSO3��+H2O��CaSO3+H2SO4=CaSO4+SO2��+H2O
(5)410:33(��82:6.6)��94.3%
���������
�����Ѷȣ�һ��
4��ѡ���� ��CnHmCOOH����ʾ������0.1mol���ӳ�ʱ�����ĵⵥ��50.8g��ȡͬ��������ȫȼ������ˮ�Ͷ�����̼��3.4mol�����������
A��C15H31COOH
B��C17H35COOH
C��C15H27COOH
D��C17H31COOH
�ο��𰸣�D
���������������֪1mol�����4mol��ӳɣ���˵���������IJ����Ͷ�Ϊ4���ų�AB������1mol����ȫȼ������ˮ�Ͷ�����̼��34mol������ȼ��ͨʽ֪����ΪD��C17H31COOH��
�����Ѷȣ�һ��
5��ѡ���� �Ӵ����������У�����Ӵ��ҵ�������뾻�����������Ҫԭ����
[? ]
A����ֹ�����ж�
B����߷�ӦЧ��
C�����SO2ת����
D����ֹ������Ⱦ
�ο��𰸣�A
���������
�����Ѷȣ���