1、选择题 在常温下,下列操作不能区别浓硫酸和稀硫酸的是
[? ]
A.分别加入铁片
B.分别加入蔗糖
C.分别加入铜片
D.分别加入硫酸铜晶体
参考答案:C
本题解析:
本题难度:一般
2、选择题 某溶液中,只可能含有下列离子中的几种:现每次取100.00mL溶液进行实验:①第一份加入硝酸银溶液有沉淀产生;②第二份加入足量氯化钡溶液后得干燥沉淀6.27g,沉淀经足量盐酸洗涤,干燥后剩余2.33g.下列说法错误的是
A.C()=0.2?mol/L
B.C(K+)一定为0.6mol/L
C.氯离子可能存在
D.一定有和
参考答案:B
本题解析:分析:①第一份加入硝酸银溶液有沉淀产生,阴离子中Cl-,CO32-,SO42-;都可能生成沉淀;
②第二份加入足量氯化钡溶液后得干燥沉淀6.27g,沉淀经足量盐酸洗涤,干燥后剩余2.33g.说明沉淀是碳酸钡沉淀和硫酸钡沉淀,原溶液中一定含有CO32-,SO42-;根据离子共存判断,Mg2、Fe3+、Al3+不能存在;溶液电荷守恒,有阴离子必须有阳离子,所以一定含K+离子;综上所述溶液中一定含有K+,CO32-,SO42-;Cl-可能存在;
解答:①第一份加入硝酸银溶液有沉淀产生,阴离子中Cl-,CO32-,SO42-;都可能生成沉淀;
②第二份加入足量氯化钡溶液后得干燥沉淀6.27g,沉淀经足量盐酸洗涤,干燥后剩余2.33g.说明沉淀是碳酸钡沉淀和硫酸钡沉淀,原溶液中一定含有CO32-,SO42-;根据离子共存判断,Mg2、Fe3+、Al3+不能存在;溶液电荷守恒,有阴离子必须有阳离子,所以一定含K+离子;综上所述溶液中一定含有K+,CO32-,SO42-;Cl-可能存在;
A、依据题意生成碳酸钡沉淀质量=6.27g-2.33g=3.94g,物质的量=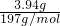 =0.02mol,CO32-离子浓度=
=0.02mol,CO32-离子浓度=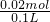 =0.2mol/L,故A正确;
=0.2mol/L,故A正确;
B、依据钾离子和碳酸根离子和硫酸根离子的电荷守恒计算,由于溶液中Cl-的存在不一定,所以钾离子的浓度不一定是0.6mol/L,故B错误;
C、依据分析判断,氯离子可能存在,故C正确;
D、依据生成沉淀溶液盐酸质量部分减小证明一定含有CO32-,SO42-;故D正确;
故选B.
点评:本题考查了常见离子检验的实验方法,离子反应的现象分析,离子性质的应用溶液电荷守恒的计算应用,离子共存的判断是解题关键.
本题难度:一般
3、填空题 阅读材料,回答问题:
(1)某无色液体A,通电时生成无色气体B和C,B能使带火星的木条着火,C能在空气中燃烧,发出淡蓝色火焰且只生成A。则B、C的化学式分别为________________________。
(2)若已知每摩尔气体C燃烧后生成A气体时放出285.8?kJ的热量,试写出其燃烧的热化学方程式:______________________________。
(3)有人认为,气体C是一种优质能源,你认为气体C作为能源的最突出的优点是______________________________。
(4)也有人认为气体C作为能源是不现实的,你的意见呢?你如果认为现实,答出现实的理由。如果认为不现实,则答出不现实的理由。(不少于20字)
_____________________________________________
参考答案:(1)O2、H2
(2)2H2(g)+O2(g)==2H2O(g) ΔH=-571.6?kJ/mol
(3)燃烧的产物是水,不会给环境带来任何污染
(4)不现实,现有的制取氢气方法耗能大,制取的成本太高,另外是氢气的熔沸点太低,给储存和运输带来困难。
本题解析:
本题难度:一般
4、选择题 下列根据实验操作和现象所得出的结论正确的是( )
A.某钾盐溶于盐酸,产生能使澄清石灰水变浑浊的无色无味气体,说明该钾盐是K2CO3
B.向溶液中先滴加稀硝酸,再滴加硝酸钡溶液,出现白色沉淀,溶液中一定含有SO42-
C.取少量溶液X,向其中加入适量盐酸,再加硝酸银溶液,出现白色沉淀,说明X溶液中一定含有Cl-
D.取少量溶液Y,向其中加入适量氢氧化钠溶液,加热,产生能使湿润的红色石蕊的试纸变蓝的气体,说明Y溶液中含有NH4+
参考答案:A、某钾盐溶于盐酸,产生能使澄清石灰水变浑浊的无色无味气体,说明该钾盐是KHCO3或K2CO3 ,故A错误;
B、向溶液中先滴加稀硝酸,再滴加硝酸钡溶液,出现白色沉淀,溶液中不一定含有SO42-,原溶液中含有亚硫酸根离子,被硝酸氧化后得到硫酸根离子也会生成白色沉淀,故B错误;
C、取少量溶液X,向其中加入适量盐酸,再加硝酸银溶液,出现白色沉淀,加入的盐酸中含有氯离子,也会产生白色沉淀,不能说明X溶液中一定含有Cl-;故C错误;
D、取少量溶液Y,向其中加入适量氢氧化钠溶液,加热,产生能使湿润的红色石蕊的试纸变蓝的气体,说明Y溶液中含有NH4+,使湿润的红色石蕊的试纸变蓝是气体氨气特有的性质,故D正确;
故选D.
本题解析:
本题难度:简单
5、实验题 实验室制乙烯时,常因温度过高而发生副反应,使部分乙醇与浓硫酸反应生成二氧化硫、二氧化碳、水蒸气和碳黑。
(1)请用下图编号为①②③④的装置设计一个实验,以验证上述反应混合气体中含有CO2,SO2和水蒸气。 用装置的编号表示装置的连接顺序(按产物气流从 左到右的顺序):___→____→___ →____
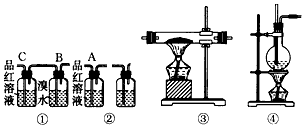
(2)实验时,装置①中C瓶的现象是____________,原因是____________。B瓶中的现象是____________;B瓶溶液的作用是____________。 若A瓶中品红溶液不褪色,说明_______________。
(3)装置③中加的固体药品是____________,以验证混合气体中有________________。装置②中盛放的溶液是________________,以验证混合气体中的________________。
(4)装置①在整套装置中所放位置的理由是____________________。
参考答案:(1)④;③;①;②
(2)品红褪色;SO2可使品红褪色;溴水褪色;除去多余的SO2;SO2已经除尽
(3)CuSO4粉末;H2O;澄清石灰水;CO2
(4)先除去SO2,以免影响实验现象
本题解析:
本题难度:一般