1、选择题 对于反应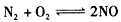 ,在密闭容器中进行,下列条件中能加快化学反应速率的是(假设温度不变)
,在密闭容器中进行,下列条件中能加快化学反应速率的是(假设温度不变)
[? ]
A.缩小体积使压强增大
B.体积不变充入N2使气体压强增大
C.体积不变充入Ne使气体压强增大
D.减小压强使体积增大?
参考答案:AB
本题解析:
本题难度:一般
2、选择题 用铁片与稀硫酸反应制备氢气时,下列措施不能使氢气生成速率加快的是(?)


A.铁片改为铁粉
B.稀硫酸改为98% 浓硫酸

C.对该反应体系加热
D.铁片改为锌片
参考答案:B
本题解析:略
本题难度:简单
3、填空题 (14分)碘在科研与生活中有重要应用,某兴趣小组用0.50 mol・L-1 KI、0.2%淀粉溶液、0.20 mol・L-1 K2S2O8、0.10 mol・L-1 Na2S2O3等试剂,探究反应条件对化学反应速率的影响。
已知:S2O82-+2I- 2SO42-+I2(慢) I2+2S2O32-
2SO42-+I2(慢) I2+2S2O32-  2I-+ S4O62-(快)
2I-+ S4O62-(快)
(1)向KI、Na2S2O3与淀粉的混合溶液中加入一定量的K2S2O8溶液,当溶液中的 耗尽后,溶液颜色将由无色变为蓝色,为确保能观察到蓝色,S2O32-与S2O82-初始的物质的量需满足的关系为:n(S2O32-)∶n(S2O82-) 。
(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
实验序号
| 体积V/mL
|
K2S2O8溶液
| 水
| KI溶液
| Na2S2O3溶液
| 淀粉溶液
|
①
| 10.0
| 0.0
| 4.0
| 4.0
| 2.0
|
②
| 9.0
| 1.0
| 4.0
| 4.0
| 2.0
|
③
| 8.0
| Vx
| 4.0
| 4.0
| 2.0
|
表中Vx mL,理由是 。
(3)已知某条件下,浓度c(S2O82-)反应时间t的变化曲线如图所示,若保持其他条件不变,请在答题卡坐标图中,分别画出降低反应温度和加入催化剂时c(S2O82-)-t的变化曲线示意图(进行相应的标注)
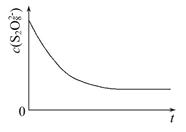
(4)碘也可用作心脏起搏器电源-锂碘电池的材料,该电池反应为:
2Li(s)+I2(s) 2LiI(s)ΔH
2LiI(s)ΔH
已知:①4Li(s)+O2(g) 2Li2O(s) ΔH1
2Li2O(s) ΔH1
②4LiI(s)+O2(g) 2I2(s)+2Li2O(s)ΔH2
2I2(s)+2Li2O(s)ΔH2
则电池反应的ΔH= ;碘电极作为该电池的 极。
参考答案:(1) Na2S2O3 <2
(2)2.0 保证反应物K2S2O8浓度改变,而其他的条件不变,才能达到实验目的;
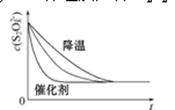
(3)
(4)(△H1-△H2)/2 正
本题解析:(1)根据题目所给信息可知,若溶液中仍存在Na2S2O3,则碘单质将不会存在,溶液不会变蓝色,所以只有将Na2S2O3消耗完时,溶液才会由无色变为蓝色;根据化学方程式,Na2S2O3与K2S2O8完全反应,溶液中不存在碘单质时,Na2S2O3与K2S2O8的物质的量之比为2:1,所以为确保能观察到蓝色,则Na2S2O3的量少些,则n(S2O32-)∶n(S2O82-)<2;
(2)实验①、②中KI溶液、Na2S2O3溶液、淀粉溶液的体积不变,且K2S2O8溶液与水的总体积是10.0mL,该实验的目的是探究反应物浓度对化学反应速率的影响,为保证反应物K2S2O8浓度改变,而其他的条件不变,才能达到实验目的,所以在实验③中K2S2O8溶液与水的总体积必须也是10.0mL,则Vx=2.0mL;
(3)降低温度,该反应的反应速率减慢,而使用催化剂则会加快反应速率,反应完全时溶液中c(S2O82-)不变,所以对应的图像为 ;
;
(4)在2Li(s)+I2(s) 2LiI(s)中I元素的化合价降低,发生还原反应,所以碘作电池的正极,根据盖斯定律可知,ΔH=(①-②)/2=(△H1-△H2)/2.
2LiI(s)中I元素的化合价降低,发生还原反应,所以碘作电池的正极,根据盖斯定律可知,ΔH=(①-②)/2=(△H1-△H2)/2.
考点:考查对实验现象的分析,化学反应速率与图像的关系,盖斯定律的应用
本题难度:困难
4、选择题 对于可逆反应:2SO2 + O2 ?2SO3(g)?△H<0,升高温度产生的影响为()
?2SO3(g)?△H<0,升高温度产生的影响为()
A.v正增大, v逆减小
B.v正减小, v逆增大
C.v正和v逆不同程度的增大
D.v正和v逆同等程度的增大
参考答案:C
本题解析:升高温度,同时加快正、逆反应速率,又因升高温度会造成化学平衡的移动,故正、逆反应速率的增大的程度不同。故选C。
点评:温度在加快反应速率中起到很重要的作用,另外化学反应都伴随着能量的变化,故改变温度必然会造成化学平衡的移动。
本题难度:一般
5、选择题 用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g) CH3OH(g) ΔH<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如下图所示。下列说法中正确的是( )
CH3OH(g) ΔH<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如下图所示。下列说法中正确的是( )

A.温度:T1>T2>T3
B.正反应速率:v(A)>v(C) v(B)>v(D)
C.平衡常数:K(A)>K(C) K(B)=K(D)
D.平均摩尔质量:M(A)<M(C) M(B)>M(D)
参考答案:C
本题解析:此反应为放热反应,温度越高CO转化率越低,所以T1<T2<T3,v(A)<v(B)<v(C),A、B选项错误,C选项正确;依据平均摩尔质量= ,气体总质量不变,依据转化率气体的总物质的量由小到大的顺序为A<B<D<C;D选项错误
,气体总质量不变,依据转化率气体的总物质的量由小到大的顺序为A<B<D<C;D选项错误
本题难度:一般