1、选择题 下列物质不能使品红溶液褪色的是( )
A.氯气
B.二氧化硫
C.漂白粉
D.氨气
参考答案:A.氯气通到品红溶液中,生成HClO使溶液褪色,故A不选;
B.二氧化硫与品红化合生成无色物质,能使品红溶液褪色,故B不选;
C.漂白粉中含ClO-,具有强氧化性,能使品红溶液褪色,故C不选;
D.氨气不具有强氧化剂,也不与品红反应,则不能使品红溶液褪色,故D选;
故选D.
本题解析:
本题难度:简单
2、选择题 下列说法不正确的是(?)
A.氯气是黄绿色的有毒气体,氯离子是无色、无毒、比氯原子结构稳定的粒子
B.氯原子易得电子,所以在化学反应中,氯元素化合价只会降低
C.新制的饱和氯水中,除水分子外,较多存在的粒子是Cl2分子
D.铜在氯气中燃烧生成棕黄色烟
参考答案:B
本题解析:误解C,原因是新制饱和氯水的成分含糊不清,只是根据Cl2+H2O====HCl+HClO和2HClO====2HCl+O2↑,误认为Cl2在水中应含有Cl2、H2O、HClO、H+、Cl-、ClO-、OH-多种粒子。殊不知,在新制的饱和氯水中,Cl2很少与水反应,反应也只是少部分反应,故含较多Cl2是正确的。再者,没见过铜在氯气中燃烧的现象,无法判断D是否正确,也有可能出现误选。
对于氯原子,最外层有7个e-,在化学反应中易得e-,但是不是只得e-,它也能在化学反应中自身氧化还原形成正价化合物。例:Cl2+H2O====HCl+HClO、Cl2+2NaOH====NaCl+NaClO+H2O等反应中,HClO、NaClO中的氯元素均显+1价,可见B是不对的。
本题难度:简单
3、选择题 用普通圆底烧瓶将某卤化钠和浓硫酸加热至500℃,发现产生无色气体,则该卤化钠是
A.NaF
B.NaCl
C.NaBr
D.NaI
参考答案:B
本题解析:略
本题难度:一般
4、选择题 将0.15 mol的MnO2与过量的12 mol・L-1的浓盐酸反应,和50 mL 12 mol・L-1的浓盐酸与足量的MnO2反应两者产生的Cl2相比(其他反应条件相同)?
A.一样多?
B.前者较后者多?
C.后者较前者多?
D.无法比较?
参考答案:B?
本题解析:浓盐酸与足量的MnO2反应时,随着反应的进行,盐酸浓度变小,后者反应会停止,有一部分HCl不能转变成Cl2。
本题难度:一般
5、实验题 某学生应用下图所示的装置来研究物质的性质,其中气体X的主要成分是氯气,杂质是空气和水蒸气
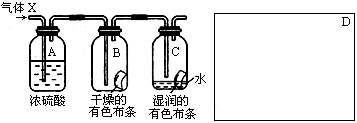
回答下列问题:
(1)该项研究(实验)的主要目的是?。
(2)浓H2SO4的作用是?,与研究目的直接相关的实验现象是?。
(3)该实验装置设计上存在的缺陷为?,请在上图的D处画出能克服该缺陷的装置。
参考答案:(1)比较干燥C12与湿润C12谁有漂白性;
(2)吸收气体X中的水;? B中的布条不褪色,C中的布条褪色;
(3)Cl2会污染空气;如图: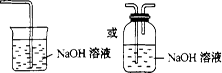 (其他装置合理也可)
(其他装置合理也可)
本题解析:该实验是气体X通过浓硫酸干燥氯气,干燥的氯气通入B,不能使干燥的有色布条褪色。再通入湿润的有色布条,布条褪色,证明干燥氯气不具有漂白性。氯气和水反应生成盐酸和次氯酸,方程式为:Cl2+H2O=HCl+HClO,次氯酸具有漂白性,同时考虑氯气有毒,应进行尾气处理,不能随意排放到空气中,可用碱溶液来吸收:Cl2+2NaOH=NaCl+NaClO+H2O。
(1)本实验为对比实验,将氯气分别通入干燥布条和湿润布条,根据实验现象的不同来探究氯气具有漂白性的条件。因此该项研究(实验)的主要目的是比较干燥C12与湿润C12谁有漂白性。
(2)浓硫酸具有吸水性,常用作干燥剂,在实验中吸收气体X中的水的作用。与研究目的直接相关的实验现象是B中的布条不褪色,C中的布条褪色。
(3)氯气有毒,应进行尾气处理,不能随意排放到空气中,可用碱溶液来吸收,所以该实验装置设计上存在的缺陷为Cl2会污染空气,改进的方法是加上尾气处理装置。
点评:该题以氯气的性质实验探究为载体,侧重对学生实验能力的考查,涉及气体的净化、除杂、性质检验、尾气处理以及实验分析与评价,有利于培养学生规范、严谨的实验设计能力,有利于提升学生的学科素养。
本题难度:一般