1、填空题 在硝酸生产过程所排放出来的废气中含有NO和NO2,它们污染环境,现用氨催化还原法将它们转化为无毒气体____________(填名称),直接排入空气中,写出有关反应的化学方程式:________________,假设NO和NO2物质的量之比恰好为1:1,则两者的混合物相当于一种酸酐,写出由烧碱溶液吸收这种酸酐的化学方程式:________________________
参考答案:氮气;6NO2+8NH3 7N2+12H2O、6NO+4NH3
7N2+12H2O、6NO+4NH3 5N2+6H2O;NO+NO2+2NaOH=2NaNO2+H2O
5N2+6H2O;NO+NO2+2NaOH=2NaNO2+H2O
本题解析:
本题难度:一般
2、选择题 难溶于水的非金属氧化物是
[? ]
A.MnO2
B.CO2
C.NO2
D.SiO2
参考答案:D
本题解析:
本题难度:简单
3、选择题 现代城市空气污染物之一NO主要来源于汽车尾气,汽车尾气中产生NO的原因是( ? )
A.汽车燃料油(如汽油、柴油)中含氮,NO是其燃烧产物
B.是空气中的N2和汽车燃料油发生了化学反应
C.空气中的N2与O2在汽车汽缸内的高温环境下电火花放电发生反应的产物
D.是汽车排出的高温尾气导致空气中的N2和O2发生化合反应
参考答案:C
本题解析:
本题难度:一般
4、简答题 汽车尾气中的NO,是造成大气污染的物质之一,但NO又是工业生产硝酸的中间产物,另外NO在人体的血管系统内又有传送信息的功能,有三位教授因此项研究成果而获得1998年诺贝尔奖.
(1)汽车尾气中NO的来源是______.
A.汽油、柴油中含氮,是其燃烧产物
B.是空气中的N2与汽油、柴油的反应产物
C.是空气中的N2与O2在汽车气缸内的高温环境下的反应产物
D.是汽车高温尾气导致了空气中N2与O2的化合反应
(2)写出NO造成酸雨的两个化学反应方程式______.
(3)在汽车尾气排放管中安装一个“催化转换器”(用铂、钯合金作催化剂),可将尾气中另一种有害气体CO跟NO反应转化为无毒气体,并促使汽油、柴油等物质充分燃烧及SO2的转化.
①写出CO与NO反应的化学方程式:______.
②“催化转化器”的缺点是在一定程度上提高了空气的酸度,其原因是______.
(4)控制或者减少城市汽车尾气污染的方法可以有______.
A.开发氢能源B.使用电动车
C.使用含铅汽油?D.严禁车辆行驶.
参考答案:(1)汽车尾气中NO的来源于空气中的N2与O2在汽车气缸内的高温环境下的反应产物NO,故选:C;
(2)硝酸型酸雨的形成过程:一氧化氮在空气中会与氧气反应,生成二氧化氮,二氧化氮有与空气中的水反应,生成了硝酸和一氧化氮,故答案为:2NO+O2=2NO2;3NO2+H2O=2HNO3+NO;
(3)①因CO跟NO反应转化为无毒气体,从CO、NO的化合价分析,可以猜测出“无毒气体”的成分是N2和CO2;
故答案为:2CO+2NO?催化剂?.?2CO2+N2;
②由于“催化转化器”促进了SO2的转化,生成的SO3增多,SO3+H2O=H2SO4,提高了空气的酸度.
故答案为:SO2转化为SO3,产生了硫酸酸雾;
(4)因使用清洁能源和不使用产生污染的能源可减少城市汽车尾气污染,严禁车辆行驶是不切实际,使用含铅汽油会产生污染,故答案为:A、B.
本题解析:
本题难度:一般
5、填空题 为了有效实现NO和NO2的相互转化,设计如下实验:按图组装好实验装置,并检查装置气密性,实验前用排水法收集半瓶NO气体.
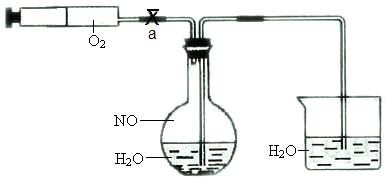
(1)打开止水夹,推动针筒活塞,使O2进入平底烧瓶.?关上止水夹,首先观察到烧瓶中的现象:______,产生此现象的化学反应方程式为:______.
(2)轻轻摇动平底烧瓶,观察到烧瓶中的现象为:①______②______.产生此现象的化学反应方程式为______.
参考答案:(1)无色的NO能与O2反应产生红棕色的NO2,故答案为:烧瓶中气体由无色变为红棕色;2NO+O2=2NO2.
(2)轻轻摇动平底烧瓶,使得NO2与水发生反应3NO2+H2O=2HNO3+NO,所以烧杯中红棕色气体又变为无色,烧瓶中液面上升,故答案为:烧杯中红棕色气体又变为无色;烧杯中水倒吸到烧瓶中(或烧瓶中液面上升)(合理答案同样给分);
3NO2+H2O=2HNO3+NO.
本题解析:
本题难度:一般