|
�߿���ѧ���⡶Ӱ������ˮ������ء���Ƶ����Ԥ�⣨2019�����°棩(��)
2020-08-13 04:31:47
�� �� �� ��
|
1��ʵ���� (8��)�����£���ijһԪ��HA��NaOH��Һ�������ϣ�������Һ��Ũ�Ⱥͻ�Ϻ�������Һ��pH���±���
ʵ��
���
| HA���ʵ���
Ũ��(mol��
L��1)
| NaOH���ʵ�
��Ũ��(mol��
L��1)
| �����Һ��
pH
| ��
| 0.2
| 0.2
| pH��a
| ��
| c1
| 0.2
| pH��7
| ��
| 0.2
| 0.1
| pH>7
| ��
| 0.1
| 0.1
| pH��9
|
��ش�
(1)�������������ʵ���������Ӽ������������
��a________7(�>������<������)����HAΪǿ�
��a________7(�>������<������)����HAΪ���ᡣ
(2)�������л����Һ������Ũ��c(A��)��c(Na��)�Ĵ�С��ϵ��(����)
A��ǰ�ߴ�
B�����ߴ�
C���������
D�����ж�
| (3)�ӱ���ʵ����������HA��________��(�ǿ��������)���û����Һ������Ũ���ɴ�С��˳����___________________________________________��
(4)����ʵ�����û����Һ����ˮ�������c(OH��)��________mol��L��1��
�ο��𰸣�(1)��">"(2)C
(3)��"c(Na��)>c(A��)>c(OH��)>c(H��)
(4)10��5
���������(1)����������ʵ���Ũ�ȵ�HA��NaOH��Һ��ϣ���HAΪǿ�ᣬ�����ǡ���кͣ�pH��7����HAΪ���ᣬ����A����ˮ�����Ϻ����ҺpH>7��
(3)0.2 mol/L HA��0.1 mol/L��NaOH���������һ�Ϻ�pH>7������HAΪ���ᣬ���������غ��֪c(Na��)>c(A��)>c(OH��)>c(H��)
(4)c(OH��)ˮ����10��5
�����Ѷȣ�һ��
2������� ��ҵ���õ�ⱥ��NaCl��Һ�ķ�������ȡNaOH��Cl2��H2����������Ϊԭ������һϵ�л�����Ʒ����Ϊ�ȼҵ��
��1����������Ĥ��������ʳ��ˮʱ��Cl2����NaOH��ֽӴ������²������NaClO��H2����Ĥ��������ʳ��ˮ��Ӧ�����ӷ���ʽΪ?��
��2���ȼҵ���ܸߣ�һ�ֽ�������ȼ�ϵ������ϵ��¹��տ��Խڣ��磩��30�����ϡ������ֹ�������У�������ϵĴ�����ת����ϵ����ͼ��ʾ�����еĵ缫δ��������õ�����Ĥ��ֻ����������ͨ����
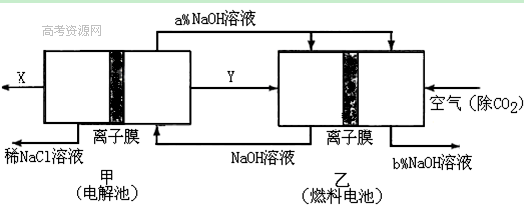
�پ����Ƶı���NaCl��ҺӦ��ͼ�е��ص�?����д���� ���ҡ�����ע�롣
��ͼ��X��____?__���ѧʽ�����������ҵĵ缫��ӦʽΪ��?_?��ͼʾ������������Һ��������a����b���Ĺ�ϵ��???������ĸ����?
A. a%=b%? B. a%��b%? C. a%��b%
�ۼ��е����ӽ���ĤΪ?��������ӽ���Ĥ���������ӽ���Ĥ������
��3���ȼҵ�IJ���NaOH�벻ͬ���ʷ�Ӧ�������ɲ�ͬ���Ρ���֪�����£�Ũ�Ⱦ�Ϊ0.1 mol/L��4��������ҺpH���±���
����
| Na2CO3
| NaHCO3
| NaClO
| NaHSO3
| pH
| 11.6
| 9.7
| 10.3
| 5.2
|
?
����˵���У�����ȷ����?������ĸ��
a������ˮ�м���NaHCO3������������ˮ�д������Ũ��
b��������Һ�У�ˮ�ĵ���̶�������NaClO
c�������£���ͬ���ʵ���Ũ�ȵ�H2SO3��H2CO3��HClO��pH������H2SO3
d��NaHSO3��Һ������Ũ�ȴ�С˳��Ϊc��Na+��> c��H+��>c��HSO3-�� >c��SO32-��>c��OH-��
�ο��𰸣�
��1��Cl����H2O��ClO�� + H2��
��2������?�� Cl2? O2 + 4e- + 2H2O = 4OH-? C?�� �����ӽ���Ĥ
��3��bcd
���������������ˮ�м���NaHCO3��,̼�����������ᷴӦ��������ˮ�ķ�Ӧ������У�����������ˮ�д������Ũ�ȣ���ȷ��������Һ�У�ˮ�ĵ���̶�������ˮ��̶����ģ�Ҳ���Ǽ�����ǿ�ģ�ӦΪ̼���ƣ�������NaClO���������£���ͬ���ʵ���Ũ�ȵ�H2SO3��H2CO3��HClO��pH������Ӧ�������������ģ�Ҳ�����������м�����ǿ��������Ӧ�������ᣬ��̼������������ᣬ����NaHSO3��Һ������Ũ�ȴ�С˳��Ϊc��Na+��>c��HSO3-��> c��H+�� >c��SO32-��>c��OH-��������
�����Ѷȣ�һ��
3������� 10��ʱ����NaHCO3������Һ����ø���Һ��pH�������±仯
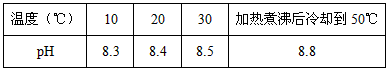
��1����ͬѧ��Ϊ������Һ��pH���ߵ�ԭ����HCO3-��ˮ��̶����ʼ�����ǿ���÷�Ӧ�����ӷ���ʽ��____________________��
��2����ͬѧ��ȼ���Ca(HCO3)2��Һ�������___________________������ΪNaHCO3��ҺpH���ߵ�ԭ����NaHCO3���ȷֽ⣬������Na2CO3�����ƶ�ˮ��̶ȣ�Na2CO3_________NaHCO3������ڡ���С�ڡ���
��3����ͬѧ��Ϊ�ס��ҵ��ж϶�����֡�����Ϊ��
��ֻҪ�ڼ�����к����Һ�м����������Լ�X����������������˵��__________����ס����ҡ����ж���ȷ���Լ�X��______________(����ĸ)
A. Ba(OH)2��Һ B.BaCl2��Һ C.NaOH��Һ D.�����ʯ��ˮ
�ڽ����Ⱥ����Һ��ȴ��10�棬����Һ��pH________(����ڡ��������ڡ����ڡ�)8.3����˵����һ�ж���ȷ��
�ο��𰸣���1��HCO3-+H2O H2CO3+OH- H2CO3+OH-
��2�����ǣ�����
��3�����ң�B���ڵ���
���������
�����Ѷȣ�һ��
4��ѡ���� һ�������£�CH3COONa��Һ����ˮ��ƽ�⣺CH3COO-+H2O CH3COOH+OH-������˵����ȷ���� CH3COOH+OH-������˵����ȷ����
[? ]
A����������NaOH���壬c(CH3COO-)����
B����������FeCl3���壬c(CH3 COO-)��С
C��ϡ����Һ����Һ��pH����
D��������������õ������Ի����Һ��c( Na+) >c(CH3COO-)>c(H+) >c( OH-)
�ο��𰸣�AB
���������
�����Ѷȣ�һ��
5��ѡ���� �������ӷ���ʽ�У�����ˮ�ⷴӦ����
A��HCO3��+H2O H3O++CO32�� H3O++CO32��
B��HCO3��+H2O H2CO3+OH�� H2CO3+OH��
C��CO2+H2O HCO3��+H+ HCO3��+H+
D��CH3COOH CH3COO��+H+ CH3COO��+H+
�ο��𰸣�B
���������A��������̼��������ӵĵ��롣
B��ȷ��
C������ˮ��Ҳ���ǵ��롣
D�������ڵ��롣
�����Ѷȣ���
|