1��ѡ���� ��NAΪ�����ӵ���������ֵ��������������ȷ����
A��1 mol��������NH2���к�������Ϊ10NA
B����״���£�2.24 L18O2���������ӵ���Ŀ��2NA
C����״���£�22.4 L C8H18�к��еĹ��ۼ�����Ϊ25NA
D���ڷ�ӦCaO + 3C = CaC2 + CO���У�ÿ����1 mol CO��ת�Ƶĵ�����Ϊ3NA
�ο��𰸣�B
���������1��������1����ԭ�Ӻ�2����ԭ�ӹ��ɣ���ԭ�Ӻ���7�����ӣ���ԭ�Ӻ���1�����ӣ���1����������9�����ӣ�1mol��������9mol���ӣ���A��������n=V/Vm����״��������Ħ�����Ϊ22.4L/mol����18O2Ϊ0.1mol��1��18O��������Ϊ18��8=10��1��18O2����20�����ӣ���0.1mol18O2����2mol���ӣ���B��ȷ��̼ԭ��������4��C8H18�ڱ�״������Һ�����ʣ���˲���ȷ�������ʵ�����Ҳ����ȷ���������ۼ�������C����̼Ԫ����0��Ϊ��1�ۣ���������Ϊ2��̼Ԫ����0����Ϊ+2�ۣ���������Ϊ2����CaO+3C=CaC2+CO����2e�������ڸ����ʵ�ϵ��֮�ȵ������ʵ���֮�ȣ���ÿ����1molCO���÷�Ӧת��2mol���ӣ���D����
�����Ѷȣ���
2��ѡ���� ͬ��ͬѹ�£���������CH4��SO2��Ƚϣ�����������ȷ���ǣ�
A���ܶȱ��ǣ�4 ��1
B������ȣ�4 ��1
C��ԭ�Ӹ����ȣ�5 ��3
D���������ȣ�1 ��4
�ο��𰸣�B
�����������
�����Ѷȣ�һ��
3��ѡ���� ���й�ϵ��ȷ����
A�������ʵ�����Na2O2��Na2O �������Ӹ���֮��Ϊ2:1
B����״���£��������CO2��CO����ԭ����֮��Ϊ2:1
C��pH��ͬ��H2SO4(aq)��CH3COOH(aq)�е�c(H+)֮��Ϊ2:1
D����Ũ�ȵ�(NH4)2SO4 (aq)��NH4Cl(aq)��c(NH4+)֮��Ϊ2:1
�ο��𰸣�B
���������A�������ʵ�����Na2O2��Na2O ��1Ħ��Na2O2����1Ħ�����������ӣ������Ӹ���֮��Ϊ1:1������B����״���£��������CO2��CO�����ʵ�����ͬ����ԭ����֮��Ϊ2:1����ȷ��C��pH��ͬ��c(H+)��ͬ������D�����Ҫ����ˮ�⣬ˮ��̶Ȳ�ͬ������
�����Ѷȣ�һ��
4������� ��8�֣���1��2 molO3��3 molO2������֮��_______��������֮��_______��ͬ��ͬѹ�µ��ܶ�֮��_____������ԭ����֮��_______�����֮��_______��
��2��O3��Cl2�������Ƶ����ʣ�������������ˮ����������֪����������ʱ������ԭΪ��ͼ�̬������ͬ״����10 L O3��________L Cl2�����������൱��
��3�����廯����A����ʽ�ɱ�ʾΪOxFy����֪ͬ��ͬѹ��10 mL A���ȷֽ�����15 mL O2��10 mL F2����A�Ļ�ѧʽΪ________���ƶϵ�����Ϊ_______________________
�ο��𰸣�(1)1��1��2��3��3��2��1��1��2��3
(2)30��(3)O3F2�������ӵ����ɺ������غ㶨��
�����������1����m=nM֪���������������Ϊ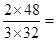 1��1��������֮�ȵ������ʵ���֮�ȣ�2��3��ͬ��ͬѹ���ܶȱȵ���ʽ���ȣ�3��2��������6mol��ԭ�ӣ�����ȵ������ʵ����ȣ�2��3
1��1��������֮�ȵ������ʵ���֮�ȣ�2��3��ͬ��ͬѹ���ܶȱȵ���ʽ���ȣ�3��2��������6mol��ԭ�ӣ�����ȵ������ʵ����ȣ�2��3
��2���ɻ��ϼ۵ĸı��֪��һ�����ӿɵ�6�����ӣ���һ���������ӿɵ�2�����ӣ������ɰ����ӵ����ɿ�֪������ȵ������ʵ����ȣ����������ܵõ�����ȣ�10��6=x��2����֪��ͬ״����10 L O3��30L Cl2�����������൱
(3)�ɰ����ӵ����ɿ�֪��2A+3O2=2F2����ԭ���غ��A�Ļ�ѧʽΪO3F2
�����Ѷȣ���
5������� 4mLO2��3mLNXHY��y��x���Ļ��������120�桢1.01��105Pa�µ�ȼ��ȫ��Ӧ�ָ���ԭ�¶Ⱥ�ѹǿʱ����÷�Ӧ��N2��O2��H2O��������������ܶȼ�С
��
��1���÷�Ӧ�Ļ�ѧ����ʽΪ______��
��2��NXHY�ķ���ʽΪ______��
�ο��𰸣���1���ɲ���֪O2��������Ӧǰ�������غ㣬������������ͬ��ͬѹ�²ⶨ�����ݦ�=mV֪���ܶ�������ɷ��ȣ���Ӧ���������V=��4+3��mL�£�1-310��=10mL��
���������ڷ�Ӧ���������3mL���ɷ�Ӧ�Ļ�ѧ����ʽ��
����yO2 +4NxHy �T2xN2 +2yH2O��V
����������4mL�������� �� �� 2x+y-4 mL
����������3mL���������� ���� 3mL
�������� 2x+y-4=4�����۵�x=2��y=4�������⣬
�����䷽��ʽΪN2H4+O2�TN2+2H2O��
�ʴ�Ϊ��N2H4+O2�TN2+2H2O��
��2�����ݣ�1��֪x=2��y=4������NXHY�ķ���ʽΪN2H4��
�ʴ�Ϊ��N2H4��
���������
�����Ѷȣ�һ��