1、选择题 硫代硫酸钠溶液与稀硫酸反应的化学方程式为:Na2S2O3+H2SO4==Na2SO4+SO2+S↓+H2O,下列各组实验中最先出现浑浊的是
[? ]
? 反应温度/℃? Na2S2O3溶液? 稀H2SO4? H2O
? ? V/mL?c/(mol・L-1)? V/mL?c/(mol・L-1)? V/mL?
A? 25? ?5? 0.1? 10?0.1? 5
B?25? 5?0.2? 5?0.2? 10
C? 35? ?5? ?0.1?10? 0.1? 5
D? 35? 5?0.2? 5? 0.2? 10
参考答案:D
本题解析:
本题难度:一般
2、选择题 在温度和压强不变时,1LNO2高温分解(2NO2?2NO+O2),达到平衡时体积变为1.2L,这时NO2的转化率为( )
A.40%
B.20%
C.60%
D.5%
参考答案:令参加反应的NO2的体积为V,则:
? 2NO2?2NO+O2? 体积增大△V
? 2? (2+1)-2=1
? V? 1.2L-1L=0.2L
所以:2:1=V:0.2L
解得:V=0.4L
所以NO2的转化率=0.4L1L×100%=40%
故选A.
本题解析:
本题难度:简单
3、选择题 在可逆反应CO(g)+H2O(g)  CO2(g)+H2(g)(正反应为放热反应)中,改变下列条件,不能使v正增大的是( )。
CO2(g)+H2(g)(正反应为放热反应)中,改变下列条件,不能使v正增大的是( )。
A.升高温度
B.降低温度
C.使用催化剂
D.增大CO浓度
参考答案:B
本题解析:不论反应是放热还是吸热,升高温度会增大反应速率,而降低温度会减慢反应速率;增大反应物浓度,加快反应速率。
本题难度:一般
4、实验题 (12分)某同学为了探究锌与硫酸反应过程中的速率变化,他在100mL稀硫酸中加入足量的锌粉,标况下用排水集气法收集反应放出的氢气,实验记录如下(累计值):
时间(min)
| 1
| 2
| 3
| 4
| 5
|
氢气体积(mL)(标准状况)
| 50
| 120
| 232
| 290
| 310
|
(1)哪一时间段(指0~1、1~2、2~3、3~4、4~5min)反应速率最大______________,原因是______________________________________________。
(2)哪一时间段的反应速率最小________________,原因是___________________。
(3)求2~3分钟时间段以硫酸的浓度变化来表示的该反应速率(设溶液体积不变,要写出计算过程)______________________________________________________。
(4)该同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
①上述实验中涉及到的离子反应方程式有??
?;
②硫酸铜溶液可以加快氢气生成速率的原因是?;
③实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4等4种溶液,可与实验中CuSO4?溶液起相似作用的是?;
④该同学通过实验进一步研究了硫酸铜的量对氢气生成速率的影响。该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因
?。
参考答案:(1) 2~3min(1分),温度对反应速率影响占主导作用(1分)。
(2) 4~5min(1分),浓度对反应速率影响占主导作用(1分)。
(3) 2~3min产生的V(H2)=" 232" mL -120mL="112" mL=0.112L
n(H2)=? =0.005mol
H2SO4? ~? H2↑
1? 1?
n(H2SO4)? 0.005mol
所以n(H2SO4) =0.005mol
因此硫酸的反应速率为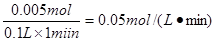 ="0.05" mol/(L?min)(2分)
="0.05" mol/(L?min)(2分)
(4)①Zn+Cu2+=Zn2++Cu(1分);Zn+2H+=Zn2++H2↑(1分)
②? CuSO4与Zn反应产生的Cu与Zn形成原电池加快了氢气产生的速率。(1分);
③? Ag2SO4(1分);
④加入一定量的 CuSO4后,生成的单质Cu会沉积在Zn的表面,降低了Zn与溶液的接触面积(2分)。
本题解析:(1)根据表中数据可知,在0~1、1~2、2~3、3~4、4~5min内收集到的氢气分别是(ml)50、70、112、58、20。所以2~3min内反应速率最大,这是由于反应是放热反应,温度对反应速率的影响超过了浓度对反应速率的影响。
(2)4~5min内收集到的气体最少,所以反应速率最小。这是由于随着反应的进行,反应物
的浓度减小,此时浓度对反应速率的影响超过了温度对反应速率的影响。
(3)略
(4)加入硫酸铜后,新可以置换出铜,从而构成铜锌原电池,锌作负极,加快反应速率。有
关离子方程式为Zn+Cu2+=Zn2++Cu(、Zn+2H+=Zn2++H2↑。由于银的金属性也弱于锌的,所
以也能和锌构成原电池,因此与硫酸铜相似的是硫酸银。如果硫酸铜太多,则生成的单质Cu
会沉积在Zn的表面,降低了Zn与溶液的接触面积,从而降低反应速率。
本题难度:一般
5、选择题 化学反应速率是通过实验测定的,下列化学反应速率的测量中,测量依据不可行的是(?)?
选项
| 化学反应
| 测量依据(单位时间内)
|
A
| CO(g)+H2O(g)=CO2(g)+H2(g)
| 压强变化
|
B
| Zn+H2SO4=ZnSO4+H2
| H2体积
|
C
| 2NO2?N2O4
| 颜色深浅
|
D
| Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
| 沉淀质量
参考答案:A
本题解析:化学反应速率用单位时间内反应物的浓度的减少或生成物浓度的增加量来表示。A、不可行,该反应是体积不变的反应,反应前后压强不变;B、可行,单位时间内H2体积变化多,速率快;C、可行,2NO2 N2O4,NO2是红棕色气体,N2O4是无色气体,可以用单位时间内气体颜色的变化来衡量反应的快慢。D、可行,单位时间内产生的沉淀的质量越高,速率越快。选A。 N2O4,NO2是红棕色气体,N2O4是无色气体,可以用单位时间内气体颜色的变化来衡量反应的快慢。D、可行,单位时间内产生的沉淀的质量越高,速率越快。选A。
本题难度:一般
|