|
高考化学必考知识点《绿色化学》试题强化练习(2019年最新版)(二)
2020-08-13 04:54:27
【 大 中 小】
|
1、实验题 (15分)高纯氧化铁(α―Fe2O3)是现代电子工业的重要材料。实验室用硫铁矿烧渣(主要成分为Fe2O3、FeO,还含有SiO2等杂质)为原料制备高纯氧化铁的步骤如下:

回答下列问题:
 ?(1)上述实验所涉及的反应中,有一个反应既属于化合反应,又属于氧化还原反应。写出该反应的离子方程式:?。 ?(1)上述实验所涉及的反应中,有一个反应既属于化合反应,又属于氧化还原反应。写出该反应的离子方程式:?。
(2)实验室欲用18.4mol・L-1的浓硫酸配制100mL 5.0mol・L-1的硫酸
溶液,所用的玻璃仪器胶头滴管、量筒、烧杯、玻璃棒外,还有
?(填写仪器名称)。
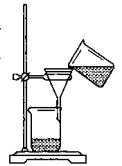
(3)某同学用右图所示装置进行过滤操作。
①请指出其中的错误之处:?;
②过滤后,洗涤过滤器中少量沉淀的方法是?。
(4)某同学用下图所示装置(尾气吸收装置未画出)实验向溶液Y中通入NH3和CO2
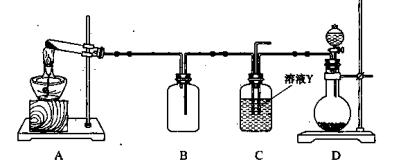
①下列为实验室制备NH3和CO2的备选药品:
a.NH4Cl? b.CaCO3(块状)? c.Ca(OH)2?d.NaOH
e.浓氨水? f.稀盐酸? g.稀硫酸
则上述装置A处的试管中所放药品的最佳选择为?和?(用药品序号填空);装置D处药品的最佳选择为?和?(用药品序号填空)。
②下列各项制备实验中,也可利用装置D处仪器完成的是?(填序号)。
A.MnO2与浓盐酸反应制备Cl2
B.Cu与浓硫酸反应生成SO2
C.由KMnO4分解制O2
D.乙醇与乙酸反应制备乙酸乙酯
| E.Zn与稀硫酸反应制备H2
③写出上述装置A处的试管中所发生反应的化学方程式?。
④若通入一定量的NH3和CO2后,装置C处的溶液中只含有S、N、H、O四种元素。用pH试纸测定该溶液pH的方法是?;若该溶液呈中性,则溶液中的NH+4和SO2-4的物质的量浓度间的数量关系为?。(离子的浓度用符号[NH+4]和[SO2-4]表示)
参考答案:

本题解析:略
本题难度:一般
2、选择题 “绿色化学”是当今社会提出的一个新概念.在“绿色化学工艺”中,理想状态是反应中原子全部转化为欲制得产物,即原子的利用率为100%.在用丙炔合成甲基丙烯酸甲酯
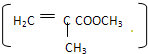
的过程中,欲使原子的利用率达到最高,在催化剂作用下还需要其他的反应物是( )
A.CO和CH3OH
B.CO2和H2O
C.CH2=CH2和CO
D.CH3OH和H2
参考答案:A
本题解析:
本题难度:简单
3、选择题 在“绿色化学”工艺中,理想状态是反应物中的原子全部能转化为目标产物,即原子利用率为100%.在下列反应类型中,能体现这一原子最经济性原则的是( )
A.化合反应
B.分解反应
C.置换反应
D.复分解反应
参考答案:A.化合反应是多种物质生成一种物质,反应物中的所有原子都转化到生成物中,原子利用率达到100%,符合绿色化学的要求,故A正确;
B.分解反应是一种反应物反应,生成物有两种或两种以上,原子利用率小于100%,不符合绿色化学的要求,故B错误;
C.置换反应是由一种单质跟一种化合物起反应,生成另一种单质和另一种化合物的反应,原子利用率小于100%,不符合绿色化学的要求,故C错误;
D.复分解反应主要是物质相互交换成分,两种化合物相互交换成分生成另两种化合物的反应,原子利用率小于100%,不符合绿色化学的要求,故D错误;
故选A.
本题解析:
本题难度:一般
4、选择题 下列关于化工生产原理的叙述中,均符合目前工业生产实际的是
A.氯碱工业中,氢氧化钠在电解槽的阴极区产生
B.氯气和氢气混合在光照条件下生成氯化氢,用水吸收得到盐酸
C.二氧化硫在接触室被氧化成三氧化硫,三氧化硫在吸收塔内被水吸收制成浓硫酸
D.合成氨工业中,利用氨易液化,分离出N2、H2循环使用,总体上提高了氨的产率
参考答案:AD
本题解析:A、电解氯化钠溶液,正确;B、氯气和氢气混合在光照条件下会爆炸,危险,错误;C、三氧化硫在吸收塔内被水吸收制成浓硫酸,易形成酸雾,错误;D、合成氨是可逆反应,有平衡,正确。
本题难度:一般
5、选择题 下列做法符合“绿色化学”思想的是( )
A..将实验室的有机废液直接倒入下水道
B.用燃气热水器代替太阳能热水器
C.回收利用废旧电池
D.在通风橱中制取SO2不用NaOH溶液吸收尾气
参考答案:A.将实验室的有机废液直接倒入下水道会污染下水道中的水,污染环境,不符合“绿色化学”要求,故A错误;
B.用燃气热水器代替太阳能热水器会增大大气污染物的排放,增加化石能源的消耗,不符合“绿色化学”要求,故B错误;
C.回收利用废旧电池可减少电池对环境的污染,符合“绿色化学”要求,故C正确;
D.在通风橱中制取SO2不用NaOH溶液吸收尾气会污染空气,不符合“绿色化学”要求,故D错误;
故选C.
本题解析:
本题难度:简单
|