1、填空题 工业生产硝酸的尾气中含有氮氧化物NOx(NO和NO2的混合物,假设不含N2O4),对生态环境和人类健康带来较大的威胁。
(1)工业上可用氨催化吸收法处理NOx,反应原理为:
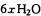 。某化学兴趣小组模拟该处理过程的实验装置如下(夹持装置已略去):
。某化学兴趣小组模拟该处理过程的实验装置如下(夹持装置已略去):

①装置A中发生反应的化学方程式为?。
②装置D中碱石灰的作用是?。
(2)工业上也常用Na2CO3溶液吸收法处理NOx。已知:NO不能与Na2CO3溶液反应,
NO+ NO2+Na2CO3=2NaNO2+ CO2;2NO2+Na2CO3= NaNO2+ NaNO3+CO2.
①当NOx被Na2CO3溶液完全吸收时,x的值不可能是?(填字母)。
A.1.3? B.1.6?C.1.8
②将1 mol NOx通入Na2CO3溶液中,被完全吸收时,溶液中生成的NO―3、NO―2两种离子的物质的量随x变化关系如图所示:

图中线段a表示?离子随x值变化的关系;若用溶质质量分数为21.2%的Na2CO3溶液吸收,则需要Na2CO3溶液至少?g。
参考答案:(1)①2NH4Cl +Ca(OH)2? ?CaCl2?+ 2NH3↑ + 2H2O
?CaCl2?+ 2NH3↑ + 2H2O
②除去气体中含有的水蒸气(2)①? A② NO2ˉ?250
本题解析:(1)①氯化铵与消石灰反应的化学方程式为: 2NH4Cl +Ca(OH)2? ?CaCl2?+ 2NH3↑ + 2H2O;②装置D中碱石灰的作用是为了除去气体中含有的水蒸气;(2)①由方程式可知,NO单独不能被吸收,NO和NO2混合气体被NaOH溶液被完全吸收,满足n(NO2):n(NO)≥1,当n(NO2):n(NO)=1时x值最小,x最小值为2+1/2=1.5,因为混有NO,所以x最大值<2,故x的取值范围为1.5≤x<2,故选A;②
?CaCl2?+ 2NH3↑ + 2H2O;②装置D中碱石灰的作用是为了除去气体中含有的水蒸气;(2)①由方程式可知,NO单独不能被吸收,NO和NO2混合气体被NaOH溶液被完全吸收,满足n(NO2):n(NO)≥1,当n(NO2):n(NO)=1时x值最小,x最小值为2+1/2=1.5,因为混有NO,所以x最大值<2,故x的取值范围为1.5≤x<2,故选A;②
本题难度:困难
2、填空题 (10分)在下图所示的物质转化关系中(部分反应条件及产物省略),化合物A由短周期元素组成,B是常见的无色液体,C是能使湿润的红色石蕊试纸变蓝色的气体,E是淡黄色粉末,D、F、G均为无色气体。

完成下列问题:
(1)写出A的化学式?。
(2)组成F的元素在周期表中位于??周期?族。
(3)B的电子式是?。
(4)反应①的化学方程式:?。
(5)反应②的离子方程式:?。
参考答案:(1)NH4HCO3 或(NH4)2CO3,?(2) 第2? VIA?(3)
(4)4NH3+5O2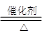 ?4NO+6H2O ?(5)3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O
?4NO+6H2O ?(5)3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O
本题解析:根据“C是能使湿润的红色石蕊试纸变蓝色的气体,E是淡黄色粉末”,确定C为NH3,E为Na2O2,再根据“B是常见的无色液体”确定B为H2O,然后依次可确定F为O2,G为NO,H为NO2,I为HNO3,D为CO2,最后确定A为NH4HCO3 或(NH4)2CO3,据此便可回答相关问题。
本题难度:一般
3、选择题 某单质跟足量浓硝酸反应时(还原产物只有NO2)每有0.5mol的单质反应就消耗2molHNO3,则单质中的元素氧化后的化合价可能是下列中的:
①+1?②+2?③+3?④+4
A.②
B.④
C.②④
D.①③
参考答案:C
本题解析:也就是说每有1mol的单质反应就消耗4molHNO3
设A与硝酸反应后得到的硝酸盐中为+n价,则硝酸盐为A(NO3)n,由化合价的升降守恒得:
n=(4-n)×1,求得n=2
如果A为非金属,它与硝酸反应后呈n价,则由化合价升降守恒可知:n=4
故答案为C
本题难度:一般
4、选择题 NO在人体内起着多方面的重要生理作用。下列关于NO的说法错误的是
A.NO是具有刺激性气味的红棕色气体
B.NO是汽车尾气的有害成分之一
C.NO常温下遇到O2就化合成NO2
D.NO2与水反应,有NO生成
参考答案:A
本题解析:NO是无色无味的气体。
本题难度:简单
5、填空题 (8分) 化合物A俗称石灰氮,以前是一种常用的肥料,其含氮量为35.0%,含钙量为50%。它可以用CaCO3通过下列步骤制得:

请回答下列问题:
(1)写出化学式:A________________、B________________;
(2)CaC2是__________________(填“离子”或“共价”)化合物;
(3)A与水完全反应的现象是产生白色沉淀并放出有刺激性气味的气体,写出A与水完全反应的化学方程式_______________________________________________________。
参考答案:
(1) CaCN2?(2分)?CaO(2分)
(2)离子(1分)
(3)CaCN2+3H2O=CaCO3↓+ 2NH3↑ (3分)
本题解析:略
本题难度:简单