1、填空题 标出下列反应中电子转移的方向和数目并回答问题:3H2O2+2H2CrO4=2Cr(OH)3+3O2+2H2O
(1)该反应中的还原剂是______,被还原的元素______,还原产物是______;
(2)反应转移了0.3mol电子,则产生的气体在标准状态下体积约为______.
2、填空题 工业上制备的高锰酸钾是锰的重要化合物和常用的氧化剂.以下是工业上用软锰矿制备高锰酸钾的一种工艺流程.
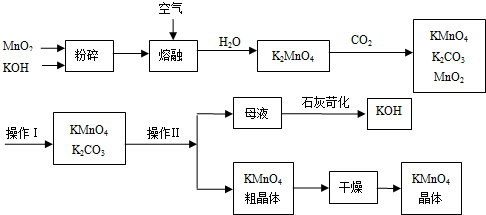
①KMnO4稀溶液是一种常用的消毒剂.其消毒原理与下列物质相同的是______(填代号).
a.84消毒液(NaClO溶液) b.双氧水 c.苯酚 d.75%酒精
②高锰酸钾保存在棕色试剂瓶,下列试剂保存不需要棕色试剂瓶的是______(填代号).
a.浓硝酸 b.硝酸银 c.氯水 d.烧碱
③上述流程中可以循环使用的物质有、(写化学式)______.
④若不考虑物质循环与制备过程中的损失,则1molMnO2______可制得molKMnO4.
⑤该生产中需要纯净的CO2气体.若实验室要制备纯净的CO2,所需试剂最好选择(选填代号)______.
a.石灰石 b.稀HCl c.稀H2SO4 d.纯碱.
3、选择题 下列反应中,化合物不作氧化剂的是( )
A.用锌和稀硫酸反应制取氢气
B.用氢气和灼热的氧化铜反应制取铜
C.用氯气和石灰乳反应制取漂白粉
D.用碳和高温水蒸气反应制取氢气
4、填空题 A、B、C、D、E是五种中学常见的单质,已知A、B、C、D在常温下均为气体.E是地壳中含量居第二位的金属.D可分别跟A、B、C在一定的条件下化合,生成X、Y、Z;Y、Z与Ne的电子数相等,A是第三周期的元素.有关的转化关系如下图所示(反应条件均已略去):
(1)A的化学式为______,B的化学式为______,C的电子式为______.
(2)Z和W在催化剂和加热的条件下反应生成C和Y,这是一个很有意义的反应,可以消除W对环境的污染,该反应的化学方程式为______.
(3)将N溶液滴入G的溶液中会产生W,写出上述变化的离子反应方程式:______.
(4)Z与N恰好反应后产物溶解在水中,所得溶液的pH(填“大于”、“小于”或“等于”)______7,用离子反应方程式表示其原因为______.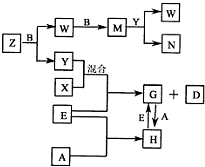
5、选择题 下列说法正确的是( )
A.酸性氧化物就是非金属氧化物
B.纯净物与混合物的区别是看是否只含有一种元素
C.强弱电解质的区别是溶液的导电能力的大小
D.氧化还原反应的判断依据是反应过程中元素的化合价是否发生变化