| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点大全《离子共存》高频试题巩固(2019年最新版)(六)
参考答案:C 本题解析:A、T1时KW=1×10-14,T2时KW=1×10-13,随温度升高,KW增大,所以图中T1<T2,错误;B、Z点时,pH=6.5,错误;C、水溶液都存在Kw= c(H+)×c(OH-),正确;D、M区域内c(H+)<c(OH-),溶液呈碱性,Fe3+与氢氧根离子结合成氢氧化铁沉淀,不能大量共存,错误,答案选C。 本题难度:一般 2、选择题 在下列各溶液中,离子一定能大量共存的是 |
参考答案:B
本题解析:A. 在强碱性溶液中Mg2+会发生沉淀反应而不能大量共存,错误;B. 室温下,pH=1的盐酸中,离子之间不会发生任何反应,可以大量共存,正确;C. 含有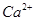 的溶液中:
的溶液中: 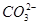 会发生沉淀反应而不能大量存在,错误;D. 由水电离产生的
会发生沉淀反应而不能大量存在,错误;D. 由水电离产生的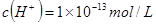 的溶液可能呈酸性也可能呈碱性,若溶液是酸性溶液,则H+、
的溶液可能呈酸性也可能呈碱性,若溶液是酸性溶液,则H+、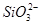 会放出沉淀反应而不能大量共存,错误。
会放出沉淀反应而不能大量共存,错误。
考点:考查溶液中离子大量共存的知识。
本题难度:困难
3、选择题 下列各组离子,在所给条件下一定能大量共存的是( )
A.在pH=1溶液中:Fe2+、K+、NO3-、Cl-
B.使紫色石蕊试液变红色的溶液中:K+、Na+、Ca2+、HCO3-
C.在含有大量AlO2-的溶液中:NO3-、Na+、Cl-、Al3+
D.在由水电离出的c(H+)?c(OH-)=10-26的溶液中:K+、Na+、Cl-、SO42-
参考答案:A.pH=1溶液,显酸性,Fe2+、H+、NO3-离子之间发生氧化还原反应,则不能共存,故A错误;
B.紫色石蕊试液变红色的溶液,显酸性,HCO3-与氢离子反应生成水和碳酸根离子,则不能共存,故B错误;
C.AlO2-、Al3+离子之间相互促进水解生成沉淀,则不能共存,故C错误;
D.由水电离出的c(H+)?c(OH-)=10-26的溶液,c(H+)=10-13mol/L,溶液为酸或碱溶液,无论酸或碱溶液,该组离子之间不反应,能共存,故D正确;
故选D.
本题解析:
本题难度:简单
4、选择题 25℃时,0.01 mol・L-1两种弱酸溶液的pH如表,下列说法正确的是
A.相同pH的两种酸溶液中,CH3COOH溶液中水电离的c(H+)较大
B.物质的量浓度相同的CH3COONa与NaCN 溶液中,CH3COONa溶液pH较大
C.等体积pH相同的两种酸溶液,分别滴加NaOH溶液至恰好中和,消耗等量的NaOH
D.HCN的电离平衡常数(Ka)与CN―的水解平衡常数(K)存在如下关系:Ka?K=Kw
参考答案:D
本题解析:A、pH相同,两种酸溶液的c(OH―)相同,则水电离的c(OH―),因此水电离的c(H+)也相同,错误;B、由已知条件可知,电离程度:CH3COOH>HCN,则水解程度:CH3COONa<NaCN,则CH3COONa溶液pH较小,错误;C、pH相同时,c(CH3COOH)<c(HCN),由c?V可知,n(CH3COOH)<n(HCN),故HCN消耗的NaOH较多,错误;D、Ka=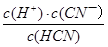 ,K=
,K=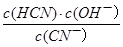 ,Kw=c(H+)?c(OH―),故Ka?K=Kw,正确。
,Kw=c(H+)?c(OH―),故Ka?K=Kw,正确。
本题难度:一般
5、选择题 一定能在下列溶液中共存的离子组是(?)
A.加入铝粉有气体放出的溶液中:Na+、NH4+、NO3-、Cl-
B.加入NaOH溶液后加热既有气体放出又有沉淀生成的溶液中:Mg2+、NH4+、SO42-、Na+
C.pH=0.3的溶液中:Na+、Al3+、SO42-、CO32-
D.存在较多H+、SO42-、NO3-的溶液中:Al3+、CH3COO-、Cl-、K+
参考答案:B
本题解析:A、与铝反应放气体的溶液可能是酸性也可能是碱性,若是碱性,则溶液中OH-与NH4+不能大量共存,错误;B、加入NaOH溶液分别生成Mg(OH)2沉淀和NH3气体,且原溶液离子可共存,正确;C、pH=0.3的溶液显酸性,CO32-与H+不能大量共存,且Al3+与 CO32-双水解也不能大量共存,错误;D、H+与CH3COO-生成弱电解质CH3COOH不能大量共存,错误。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点总结《物质的分类.. | |