1、选择题 两种金属的混合物粉末15 g,与足量的盐酸反应时,恰好得到11.2L标准状况下的氢气,下列各组金属能构成符合上述条件的混合物的是
A.Na和Ag
B.Cu和Zn
C.Al和Fe
D.Mg和Al
参考答案:C
本题解析:用平均值法:11.2 L标准状况下氢气的物质的量为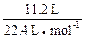 即0.5mol,得到电子为:0.5mol×2=1mol,即金属失去1mol电子的平均质量为15g,必有一物质失去1mol电子其质量大于15g,而另一种物质失去1mol电子其质量小于15g.A项:Na失1mol电子其质量为23g,Ag不反应可看成大于15g,所以A不正确.B项:Zn:
即0.5mol,得到电子为:0.5mol×2=1mol,即金属失去1mol电子的平均质量为15g,必有一物质失去1mol电子其质量大于15g,而另一种物质失去1mol电子其质量小于15g.A项:Na失1mol电子其质量为23g,Ag不反应可看成大于15g,所以A不正确.B项:Zn: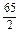 =32.5g、Cu看成大于15g.Cu、Zn均大于15g,故不符合;C项:Al:
=32.5g、Cu看成大于15g.Cu、Zn均大于15g,故不符合;C项:Al: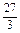 =9g、Fe:
=9g、Fe: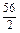 =28g,C符合.D项:Mg:
=28g,C符合.D项:Mg: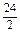 =12g、Al:9g,都小于15g,故D不符合.
=12g、Al:9g,都小于15g,故D不符合.
本题难度:一般
2、实验题 (6分)实验室常用甲装置制取氯气
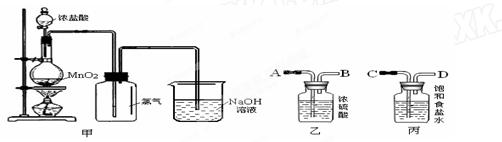
(1)写出实验室制取氯气的化学方程式并标明电子的转移______________ ___________________
___________________
(2)甲同学认为该装置制得的氯气不纯,在收集氯气之前应补充乙、丙两实验装置,你认为应如何连接(用ABCD字母连接) _____________饱和食盐水的作用是_________ _________
_________
参考答案: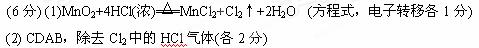
本题解析:略
本题难度:一般
3、实验题 下图是实验室制备四氯化硅的装置示意图。已知:四氯化硅遇水极易反应。
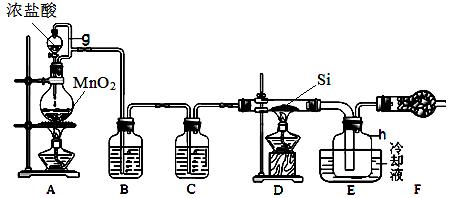
请回答下列问题:
(1)写出装置A中发生反应的化学方程式?。
(2)装置A中g管的作用是?。
干燥管F中碱石灰的作用是?。
该组实验装置中存在的缺陷是?。
参考答案:(1)MnO2+4HCl(浓) MnCl2+Cl2↑ +2H2O;
MnCl2+Cl2↑ +2H2O;
(2)使溶液顺利滴下(2分)
(3)防止空气中的水蒸气进入h装置与四氯化硅反应(2分)
(4)缺少吸收多余氯气的装置,导致污染环境(2分)
本题解析:
(1)实验室用二氧化锰氧化浓盐酸制备氯气,MnO2+4HCl(浓) MnCl2+Cl2↑ +2H2O
MnCl2+Cl2↑ +2H2O
(2)装置A中g管使分液漏斗与烧瓶连通,使溶液顺利滴下;(3)防止空气中的水蒸气进入h装置与四氯化硅反应;(4)氯气有毒,不能直接排放空气中,缺少吸收多余氯气的装置,导致污染环境。
本题难度:一般
4、选择题 如图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。已知:2KMnO4+16HCl=2KCl+5Cl2↑+2MnCl2+8H2O。对实验现象的“解释或结论”正确的是(?)

选项
| 实验现象
| 解释或结论
|
A
| a处变蓝,b处变红棕色
| 氧化性:Cl2>Br2>I2
|
B
| c处先变红,后褪色
| 氯气与水生成了酸性物质
|
C
| d处立即褪色
| 氯气与水生成了漂白性物质
|
D
| e处变红色
| 还原性:Fe2+>Cl-
|
?
参考答案:D
本题解析:a处变蓝,b处变红棕色,说明Cl2分别与KI、NaBr作用生成I2、Br2,可证明氧化性:Cl2>I2,Cl2>Br2,无法证明I2与Br2之间氧化性的强弱,A项错误;c处先变红,说明氯气与水生成酸性物质,后褪色,则证明氯气与水生成具有漂白性物质,B项错误;d处立即褪色,也可能是氯气与水生成酸性物质中和了NaOH,C项错误;e处变红说明Cl2将Fe2+氧化为Fe3+,证明还原性:Fe2+>Cl-,D项正确。
本题难度:一般
5、选择题 某无色混合气体可能含有CO2、CO、H2O(水蒸气)、H2中的一种或几种,依次进行如下连续处理(假定每步处理均反应完全):
①通过碱石灰时,气体体积变小;
②通过赤热的氧化铜时,固体变成红色;
③通过白色硫酸铜粉末时,粉末变成蓝色;
④通过澄清石灰水时,溶液变浑浊。
由此可以确定原混合气体中( )
A.一定含有CO2、H2O,至少含有H2、CO中的一种
B.一定含有H2O、CO,至少含有CO2、H2中的一种
C.一定含有CO、CO2,至少含有H2O、H2中的一种
D.一定含有CO、H2,至少含有H2O、CO2中的一种
参考答案:D
本题解析:通过碱石灰时,气体体积减小,故可能含有H2O或CO2。通过赤热的氧化铜时,固体变红,又由③④可知,一定含有CO和H2。
本题难度:一般