1��ѡ���� ���ֽ����Ļ�����ĩ15 g�������������ᷴӦʱ��ǡ�õõ�11.2L��״���µ����������и�������ܹ��ɷ������������Ļ�������
A��Na��Ag
B��Cu��Zn
C��Al��Fe
D��Mg��Al
�ο��𰸣�C
�����������ƽ��ֵ����11��2 L��״�������������ʵ���Ϊ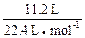 ��0.5mol���õ�����Ϊ��0.5mol��2=1mol��������ʧȥ1mol���ӵ�ƽ������Ϊ15g������һ����ʧȥ1mol��������������15g������һ������ʧȥ1mol����������С��15g��A�Naʧ1mol����������Ϊ23g��Ag����Ӧ�ɿ��ɴ���15g������A����ȷ��B�Zn��
��0.5mol���õ�����Ϊ��0.5mol��2=1mol��������ʧȥ1mol���ӵ�ƽ������Ϊ15g������һ����ʧȥ1mol��������������15g������һ������ʧȥ1mol����������С��15g��A�Naʧ1mol����������Ϊ23g��Ag����Ӧ�ɿ��ɴ���15g������A����ȷ��B�Zn��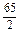 =32.5g��Cu���ɴ���15g��Cu��Zn������15g���ʲ����ϣ�C�Al��
=32.5g��Cu���ɴ���15g��Cu��Zn������15g���ʲ����ϣ�C�Al��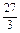 =9g��Fe��
=9g��Fe��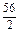 =28g��C���ϣ�D�Mg��
=28g��C���ϣ�D�Mg��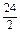 =12g��Al��9g����С��15g����D�����ϣ�
=12g��Al��9g����С��15g����D�����ϣ�
�����Ѷȣ�һ��
2��ѡ���� ��������A�������в���������ģ���һ�ּ��Ը߶������Դ�Ⱦ��������������ʱ��Ҫ����ʹ�ù������ᡢ�������������ȡ��Ȱ���һ�ֳ�Ч�����л���������������ˮ���Է������ֽⷴӦ�����������ɱ��������һ�㺬����������4��5�����й��Ȱ�(NH2Cl��������Cl�Ļ��ϼ�Ϊ��1��)��˵������ȷ����
A���Ȱ���ˮ�������ֽ�IJ���ΪNH2OH��HCl
B���Ȱ�������ԭ����Ư������
C���Ȱ���Ũ�����Ͽɲ�������
D���Ȱ��еĵ�Ԫ��Ϊ��3��
�ο��𰸣�A
�����������������������Ϊ���У�1�۵��ȣ����к�ǿ�������ԡ��Ȱ���ˮ�������ֽⷴӦ�IJ�����NH3��HClO��HClO���к�ǿ�������ԡ��Ȱ�����ԭ����Ư�����ƣ�A�����B����ȷ��C����ȷ����1�۵��Ⱥͣ�1�۵��������������¿ɷ������з�Ӧ����������
�����Ѷȣ���
3��ѡ���� ����˵����ȷ������ǣ�������
�������Ӻ���ԭ�ӵ�����һ������+5�۵���ֻ���������ԣ����������ܱ���ԭ�Ӷ�һ�����ӣ�������Ⱦ��������ԡ����ԣ��־��л�ԭ�ԣ���Cl2�������Ա������ǿ����Һ������ˮ��ͬһ�����ʣ�
A���ڢܢ�
B���٢�
C���ۢܢ�
D���ڢ�
�ο��𰸣�����ԭ�ӵ�����������δ�ﵽ8��������1�������γ������ӣ��������������ﵽ��8���ӣ��Ƚ��ȶ�������ԭ���ȶ��Ķ࣬�����Ӻ���ԭ�ӵ����ʲ�һ�����ʢٴ���
��+5�۵������м��̬��������������Ҳ���л�ԭ�ԣ��ʢڴ���
������������ԭ�ӵõ�һ�������γɵģ������ܱ���ԭ�Ӷ�һ�����ӣ��ʢ���ȷ��
�������е������ӼȾ����������־������ԣ�����������Ԫ�ص���ͼۣ������Ӿ��л�ԭ�ԣ��ʢ���ȷ��
��������ǿ��������������������������ӵ������ԣ�����Cl2�������Ա������ǿ���ʢ���ȷ��
��Һ�����������ӳ�Һ̬�Ǵ������ˮ��������ˮ��Һ�ǻ����ʢ���
�����������ۢܢ�
��ѡC��
���������
�����Ѷȣ�һ��
4������� ij��ѧ��ȤС����ʵ��������������ʯ���顾Ca��OH��2����ȡƯ�ۣ�
��֪2Cl2+2Ca��OH��2�TCaCl2+Ca��ClO��2+2H2O
����ȤС�����������ʵ��װ�ã���������ʵ�飺
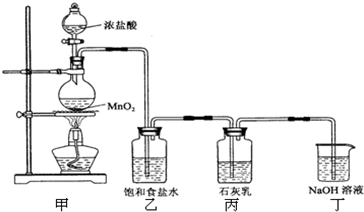
��ش��������⣺
��1��ʵ�����ü�װ�������Ʊ��������䷴Ӧ�Ļ�ѧ����ʽ��______��
��2����ҵ�ϵ�ⱥ��ʳ��ˮ���Ʊ��������仯ѧ����ʽ��______��
��3����װ�õ�������______����װ�õ�������______��
��4������ȤС����������Ũ������8.7g?MnO2�Ʊ��������������������������ʯ���鷴Ӧ���������������Ƶ�Ca��ClO��2______g����С���Ա���֣�ʵ���ϲ�����Ca��ClO��2����������С������ֵ��Ϊ��̽����ԭ��С���Ա������������ϵõ��������ͼ�ķ�ӦΪ���ȷ�Ӧ���¶Ƚϸ�ʱ�������ͼ�ܷ������·�Ӧ��6Cl2+6Ca��OH��2
?5CaCl2+Ca��ClO3��2+6H2O
��5��Ϊ�����Ca��ClO��2�IJ��ʣ��ɶԱ�װ�����ʵ��Ľ����������һ�ָĽ�������______��
�ο��𰸣���1��ʵ������ȡ��������Ũ����Ͷ������̷���������ԭ��Ӧ�����Ȼ��̡�������ˮ����Ӧ�Ļ�ѧ����ʽΪ��
MnO2+4HCl��Ũ��?��?.?MnCl2+Cl2��+2H2O��
�ʴ�Ϊ��MnO2+4HCl��Ũ��?��?.?MnCl2+Cl2��+2H2O��
��2����ҵ�ϵ�ⱥ��ʳ��ˮ���Ʊ����������Ȼ��ƺ�ˮ��ͨ�������µ�ⷴӦ�����������ơ���������������Ӧ�Ļ�ѧ����ʽΪ��2NaCl+2H2O?ͨ��?.?H2��+Cl2��+2NaOH��
�ʴ�Ϊ��2NaCl+2H2O?ͨ��?.?H2��+Cl2��+2NaOH��
��3��Ũ����Ͷ������̷�Ӧ�����лᷢ���Ȼ������壬����ͨ������ʳ��ˮ�������dz�ȥCl2�л��е�HCl���壻�ձ��е�����������Һ�����չ��������������ŷŵ���������Ⱦ����������β��������
�ʴ�Ϊ����ȥCl2�л��е�HCl���壻����β��������
��4��������Ũ������8.7g MnO2�Ʊ��������������������������ʯ���鷴Ӧ���������������Ƶ�Ca��ClO��2���������ݷ�ӦMnO2+4HCl��Ũ��?��?.?MnCl2+Cl2��+2H2O��2Cl2+2Ca��OH��2�TCaCl2+Ca��ClO��2+2H2O���õ�������ϵ��8.7g MnO2���ʵ���Ϊ0.1mol��
2MnO2��Ca��ClO��2
2? 1
0.1mol? 0.05mol
���������������Ƶ�Ca��ClO��2 ����=0.05mol��143g/mol=7.15g���ʴ�Ϊ��7.15��
��5�����ݣ�4���� ��Ϣ��Ӧ�ڸ��¶��·�������Ӧ�����ԸĽ���ʩ���ѱ�װ�÷����ˮ�У����ⷢ����Ӧ��6Cl2+6Ca��OH��2?��?.? 5CaCl2+Ca��ClO3��2+6H2O��
�ʴ�Ϊ������װ������װ����ˮ�������У�
���������
�����Ѷȣ�һ��
5��ѡ���� ����ˮ����������ˮ��������������ԭ��������ȷ����
A�����������Ķ���
B������������ˮ��Ӧ���ɵ�HClO����ǿ������
C������ ������Ư����
D������������ˮ��Ӧ���ɵ�HCl����ǿ����
�ο��𰸣�B
�����������������ˮ����ˮ��Ӧ���ɵĴ��������ǿ�����ԣ���ɱ�����������Կ���������ˮ��������ѡB��
�����������ǻ���������Ŀ��飬�ѶȲ�����Ĺؼ���Ҫ��ס����������ԭ��������������ѧ����������������
�����Ѷȣ�һ��