1、选择题 常温下,在V L密闭容器中有a mol NO气体,压强为b kPa,若再充入a mol O2,保持温度不变,反应后容器内的压强(?)
A.等于1.5b kPa
B.等于2b kPa
C.小于1.5b kPa
D.大于1.5b kPa
参考答案:C
本题解析:由反应:2NO+O2====2NO2,可知O2过量a/2 mol,生成NO2为a mol,即气体共1.5a mol,实际存在隐反应:2NO2 N2O4,气体的总物质的量小于1.5 a mol,根据pV=nRT知答案为C。
N2O4,气体的总物质的量小于1.5 a mol,根据pV=nRT知答案为C。
本题难度:简单
2、实验题 一无色气体,可能由CO2、HCl、NH3、NO2、NO、H2中的一种或几种组成。将此无色气体通过盛有浓H2SO4的洗气瓶,发现气体体积减少。继续通过装有固体Na2O2的干燥管,发现从出气管出来的气体颜色显红棕色,再将该气体全部通入盛满水倒立于水槽中的试管内,发现最后试管里仍然为一满试管液体。由此可推知:①原气体中一定含有_____________,一定不会有?____________;②最终结果可知原气体中____?__与____?___气体的体积比为____?___。
参考答案:①CO2 ?NH3?NO? ;?HCl? NO2? H2?(4分)
②NO ;? CO2 ;? 2:3?(3分)
本题解析:略
本题难度:简单
3、实验题 (13分)现给你一试管二氧化氮,其他药品和仪器自选。试设计实验,要求尽可能多地使二氧化氮被水吸收。
?
| 实验步骤
| 现象
| 解释(可用化学方程式表示)
|
(1)
| ?
| ?
| ?
|
(2)
| ?
| ?
| ?
|
(3)
| ?
| ?
| ?
|
?
参考答案:
?
实验步骤
现象
解释(可用化学方程式表示)
(1)
将一支充满NO2的试管倒放在盛有水的水槽中
红棕色气体逐渐消失,水位上升,最后水充满整个试管的2/3,无色气体充满1/3(上部)
3NO2+H2O====2HNO3+NO
(2)
制取少量氧气
―
2KClO3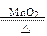 2KCl+3O2↑
2KCl+3O2↑
或2H2O2 2H2O+O2↑
2H2O+O2↑
(3)
将氧气慢慢地通入步骤(1)的试管中
无色气体变为红棕色气体,又变为无色气体,但气体体积逐渐缩小,液面不断上升
2NO+O2====2NO2
3NO2+H2O====2HNO3+NO
本题解析:根据3NO2+H2O====2HNO3+NO及2NO+O2====2NO2可知,4NO2+O2+2H2O====
4HNO3,即可补充氧气使二氧化氮能尽可能多地溶于水。
本题难度:简单
4、填空题 (9分)氮及其化合物在生活、生产和科技等方面有重要的应用。请回答下列问题:
(1)氮元素基态原子的价电子排布式为? ?;
(2)在氮气分子中,氮原子之间存放着?个σ键和?个π键;
(3)N2分子中氮氮键的键长?(填“大于”、“小于”或“等于”)
F2分子中氟氟键的键长;
(4)氮元素的氢化物――NH3是一种易液化的气体,该气体易液化的原因
是? ?。
(5)配合物[Cu(NH3)4]C12中含有4个配位键,若用2个N2H4代替其中2个NH3,得到的配合物[Cu(NH3)2(N2H4)2]C12中含有配位键的个数为?。
参考答案:
(1)略? 2分
(2)1;2? 2分
(3)小于? 1分
(4)氨分子之间容易形成氢键,使其沸点升高而容易液化? 2分
(5)4? 2分
本题解析:略
本题难度:简单
5、选择题 下列实验中,颜色的变化与氧化还原反应无关的是
A.SO2使酸性KMnO4溶液褪色
B.Na2O2投入酚酞溶液中溶液先变红后褪色
C.向FeSO4溶液中滴NaOH溶液,生成的沉淀由白色变成灰绿色,最后变成红褐色
D.往紫色石蕊试液中通入氨气,溶液变蓝
参考答案:D
本题解析:A.SO2有还原性,能够被酸性KMnO4氧化而使酸性KMnO4溶液褪色,错误;B.Na2O2投入酚酞溶液中因为与水反应产生NaOH,所以溶液先变红,同时产生的H2O2有强氧化性,又把红色物质氧化为无色,所以溶液而后褪色,错误;C.向FeSO4溶液中滴NaOH溶液,首先产生白色的氢氧化亚铁沉淀,由于该物质不稳定,容易被空气中的氧气氧化为氢氧化铁沉淀,所以白色沉淀会迅速变为灰绿色,最后变成红褐色,错误;D.往紫色石蕊试液中通入氨气,由于氨水显碱性,所以能够使紫色石蕊试液变为蓝色。未发生氧化还原反应,正确。
本题难度:一般