1、选择题 下列各组物质发生化学反应时,由于反应物的量不同而导致生成不同产物的是
①CO2与NaOH溶液?
②NaHCO3溶液与盐酸?
③AgNO3溶液与氨水
④C与O2?
⑤AlCl3溶液与氢氧化钠溶液.
A.除③外
B.除②外
C.除②③⑤外
D.除②⑤外
参考答案:B
本题解析:分析:①二氧化碳和氢氧化钠反应能生成碳酸钠或碳酸氢钠;
②碳酸氢钠和盐酸反应生成氯化钠、二氧化碳与水;
③硝酸银和氨水能生成氢氧化银沉淀,氢氧化银能和氨水生成络合物;
⑤碳和氧气能生成二氧化碳或一氧化碳;
⑥氯化铝和氢氧化钠溶液反应生成氢氧化铝或偏铝酸钠.
解答:①向氢氧化钠溶液中通入二氧化碳,当二氧化碳不足量时,二氧化碳和氢氧化钠反应生成碳酸钠,当二氧化碳过量时,二氧化碳和氢氧化钠反应生成碳酸氢钠,故①正确.
②NaHCO3溶液与盐酸混合,碳酸氢钠和盐酸反应生成氯化钠和二氧化碳、水,故②错误.
③AgNO3溶液与氨水混合,当氨水不足量时,生成氢氧化银;当氨水过量时,生成银氨溶液,故③正确.?
④当氧气不足时,碳和氧气反应生成一氧化碳,当氧气过量时,碳和氧气反应生成二氧化碳,故④正确.
⑤AlCl3溶液与氢氧化钠反应混合,氢氧化钠不足时生成氢氧化铝沉淀,氢氧化钠过量生成偏铝酸钠,故⑤正确.
故选B.
点评:本题考查了化学反应与量的关系、物质性质等,难度不大,掌握物质的性质是关键,注意氢氧化铝是两性氢氧化物,银氨溶液的配制.
本题难度:一般
2、选择题 M、N、X、Y均为常见的物质,它们之间有如下转化关系(反应条件和其它产物已略去):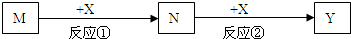
下列选项符合的是
A.M:N2,X:O2
B.M:Al,X:NaOH
C.M:Fe,X:Cu2+
D.M:Ca(OH)2,X:Na2CO3
参考答案:A
本题解析:分析:依据转化关系的特征是M和X能反应两部连续反应说明变化过程中存在变价元素的物质,结合选项中的物质进行分别推断.
解答:A、M:N2,X:O2 存在转化关系:N2 NO
NO NO2;符合转化关系,故A正确;
NO2;符合转化关系,故A正确;
B、M:Al,X:NaOH存在转化关系:Al NaAlO2,不能继续和氢氧化钠溶液反应,故B错误;
NaAlO2,不能继续和氢氧化钠溶液反应,故B错误;
C、Fe,X:Cu2+存在转化关系:Fe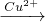 Fe2+,不能继续和铜离子溶液反应,故C错误;
Fe2+,不能继续和铜离子溶液反应,故C错误;
D、Ca(OH)2,X:Na2CO3存在转化关系:Ca(OH)2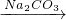 CaCO3,不能继续反应,故D错误;
CaCO3,不能继续反应,故D错误;
故选A.
点评:本题考查了物质转化关系的应用,物质性质的应用,主要考查镁、铝、铁氢氧化钙等物质的性质应用,较简单.
本题难度:困难
3、选择题 某条件下,已知由C2H4和O2组成的混和气体的密度为相同条件下H2密度的14.5倍,则混和气体中C2H4的质量分数为
A.75%
B.25%
C.27.6%
D.72.4%
参考答案:D
本题解析:分析:混和气体的密度为相同条件下H2密度的14.5倍,则混合气体的平均相对分子质量为14.5×2=29,可计算出两种气体的物质的量之比,进而计算质量关系.
解答:混和气体的密度为相同条件下H2密度的14.5倍,
则混合气体的平均相对分子质量为14.5×2=29,
设混合气体中含有xmolC2H4,ymolO2,
则有 =29,
=29,
解之得x:y=3:1,
则ω(C2H4)=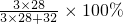 =72.4%,
=72.4%,
故选D.
点评:本题考查混合物的计算,题目难度不大,本题注意相对密度的运用,注意题中为质量的含量,为易错点,答题时注意审题.
本题难度:一般
4、选择题 1mol?Na218O2?与1mol?CO2?充分反应,下列说法正确的是
A.生成碳酸钠的质量为106?g
B.生成氧气的体积为11.2?L
C.生成的氧气中,1?mol该氧气含有18?mol中子
D.电子转移的数目约为6.02×1023个
参考答案:D
本题解析:分析:发生反应2CO2+2Na218O2=2Na2C18OO2+18O2↑,1mol?Na218O2?与1molCO2恰好反应生成1mol碳酸钠与1mol氧气,
A.生成的碳酸钠中含有18O,碳酸钠的摩尔质量为108g/mol;
B.氧气所处的状态不一定是标准状况,气体摩尔体积不一定是22.4L/mol;
C.生成的氧气为18O2,18O原子质子数为18-8=10,18O2分子中含有中子数为20,中子物质的量为氧气物质的量的20倍;
D.反应中过氧化钠起氧化剂、还原剂作用,各占一半,起还原剂作用的过氧化钠为0.5mol,反应中氧元素化合价由-1价升高为0价,再根据N=nNA计算.
解答:发生反应2CO2+2Na218O2=2Na2C18OO2+18O2↑,1mol?Na218O2?与1molCO2恰好反应生成1mol碳酸钠与1mol氧气,
A.生成的碳酸钠中含有18O,碳酸钠的摩尔质量为108g/mol,故碳酸钠的质量为1mol×108g/mol=108g,故A错误;
B.氧气所处的状态不一定是标准状况,气体摩尔体积不一定是22.4L/mol,1mol氧气的体积不一定是22.4L,故B错误;
C.生成的氧气为18O2,18O原子质子数为18-8=10,18O2分子中含有中子数为20,中子物质的量为氧气物质的量的20倍,故1mol该氧气含有20mol中子,故C错误;
D.反应中过氧化钠起氧化剂、还原剂作用,各占一半,起还原剂作用的过氧化钠为0.5mol,反应中氧元素化合价由-1价升高为0价,转移电子的数目=0.5mol×2×6.02×1023mol-1=6.02×1023个,故D正确;
故选D.
点评:本题考查过氧化钠与二氧化碳反应、氧化还原反应、常用化学计量的有关计算等,难度中等,理解反应中过氧化钠起氧化剂与还原剂作用是解题关键.
本题难度:困难
5、选择题 下列物质中,只具有还原性的是
A.Cl2
B.Na
C.H2SO4
D.SO2
参考答案:B
本题解析:Cl元素通常有-1、+1、+3、+5、+7价,因此Cl2既有强氧化性,又有还原性;Na只有+1价,因此Na只具有还原性,H2SO4具有氧化性,SO2中S元素的化合价既可升高为+6价,具有还原性,又可降低为0价,具有氧化性。
本题难度:一般