1、选择题 一定条件下,反应2NO2(g)?2NO(g)+O2(g),下列哪一种状态可能没有达到化学反应限度( )
A.速率比:V(NO2):V(NO):V(O2)=2:2:l时的状态
B.混合气体的平均相对分子质量保持不变时的状态
C.生成NO2的速率与生成O2的速率比等于2:l时的状态
D.体系中的颜色保持不变时的状态
参考答案:A.V(NO2):V(NO):V(O2)=2:2:l说明了反应中各物质的转化量的关系,不能说明该反应达到平衡状态,故A符合;
B.该反应是一个反应前后气体的物质的量增大的反应,当混合气体的平均相对分子质量保持不变时的状态时,该反应达到平衡状态,故B不符合;
C.当生成NO2的速率与生成O2的速率比等于2:l时的状态时,该反应达到平衡状态,故C不符合;
D.二氧化氮是红棕色气体,一氧化氮和氧气无色,当反应达到平衡状态时,二氧化氮的浓度不变,则体系中混合气体颜色不变,所以能说明该反应达到平衡状态,故D不符合;
故选A.
本题解析:
本题难度:一般
2、填空题 恒容容积为VL的密闭容器中发生2NO2 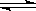 2NO+O2反应。反应过程中NO2的物质的量随时间变化的状况如图所示。
2NO+O2反应。反应过程中NO2的物质的量随时间变化的状况如图所示。

(1)若曲线A和B表示的是该反应在某不同条件下的反应状况,则该不同条件是 。
A.有、无催化剂 B.温度不同
C.压强不同 D.体积不同
(2)写出该反应的化学平衡常数K的表达式: ,并比较K800℃ K850℃(填“>”、“<”或“=”)。
(3)求算在B条件下从反应开始至达到平衡,氧气的反应速率v(O2)= 。
(4)不能说明该反应已达到平衡状态的是 。
A.v正(NO2)=v逆(NO) B.c(NO2)=c(NO)
C.气体的平均摩尔质量不变 D.气体的密度保持不变

若起始温度相同,分别向三个容器中充入2molNO和1molO2 ,则达到平衡时各容器中NO物质的百分含量由大到小的顺序为(填容器编号) 。
参考答案:(12分)(1)B (2)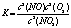 K800℃<K850℃
K800℃<K850℃
(3)v(O2)=1/40Vmol/(L・S)(4) BD (5) ①②③
本题解析:(1)根据图像可知,B曲线表示的反应速率快,达到平衡的时间少,且平衡时NO2的物质的量小于A曲线达到平衡时NO2的物质的量。由于正反应是体积增大的可逆反应,增大压强平衡应该向逆反应方向移动,NO2的物质的量增大,CD不正确;催化剂不能改变平衡状态,A不正确;所以改变的条件只能是升高温度,这说明升高温度平衡向正反应方向移动,所以正反应是吸热反应,答案选B。
(2)化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,因此根据方程式可知,该反应的平衡常数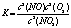 。正反应是吸热反应,升高温度平衡向正反应方向移动,平衡常数增大,所以K800℃<K850℃。
。正反应是吸热反应,升高温度平衡向正反应方向移动,平衡常数增大,所以K800℃<K850℃。
(3)根据图像可知,反应进行到2s时反应达到平衡状态,此时NO2的物质的量减少了0.20mol-0.10mol=0.10mol,则氧气的物质的量就增加了0.05mol,所以氧气的反应速率是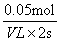 =1/40Vmol/(L・S)。
=1/40Vmol/(L・S)。
(4)在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态。A中反应速率的方向相反,且满足速率之比是相应的化学计量数之比,A可以说明。B中反应速率的方向是相同的,速率之比是相应的化学计量数之比,因此B中的关系始终是成立,B不能说明。混合气的平均相对分子质量是混合气的质量和混合气的总的物质的量的比值,质量不变,但物质的量是变化的,所以C可以说明。密度是混合气的质量和容器容积的比值,在反应过程中质量和容积始终是不变的,D不能说明,答案选BD。
(5)该反应是体积减小的、放热的可逆反应,所以③中容器中的压强始终大于②中的压强,压强大有利于NO的转化。①中是绝热的,则反应中温度高,但温度越高,越不利于NO的转化,所以达到平衡时各容器中NO物质的百分含量由大到小的顺序为①②③。
考点:考查外界条件对平衡状态的判断、外界条件对平衡状态的影响、平衡常数、反应速率的计算
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,在注重考查学生基础知识的同时,侧重考查学生灵活运用基础知识解决实际问题的能力。该题的关键是明确平衡状态的含义、判断依据以及外界条件对平衡状态的影响,然后结合图像和勒夏特例原理灵活运用即可,有利于培养学生的应试能力和逻辑推理能力。
本题难度:困难
3、选择题 T℃时,将气体X与气体Y置于一密闭容器中,反应生成气体Z,反应过程中各物质的浓度变化如图(I)所示。保持其他条件不变,在T1.T2两种温度下,Y的体积分数变化如图(Ⅱ)所示。 下列结论正确的是
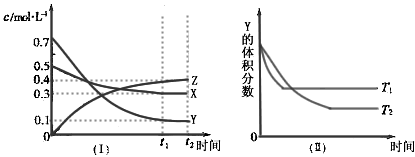
[? ]
A.t2时,保持其它条件和物质状态不变,增加压强,化学平衡向逆反应方向移动
B.T℃时,若各物质起始浓度为:0.4mol/L X、0.4mol/L Y、0.2mol/L Z。保持其他条件不变,达到平衡时Z的浓度为0.4mol/L
C.图(Ⅱ)中T1>T2,则正反应是吸热反应
D.其他条件不变,升高温度,正.逆反应速率均增大,且X的转化率增大
参考答案:B
本题解析:
本题难度:一般
4、选择题 在一固定容积的密闭容器中进行如下反应:N2+3H2 2NH3△H < O在一定温度下反应达到平衡状态,若将平衡体系中各物质的浓度都增加到原来的2倍,下列叙述正确的是
2NH3△H < O在一定温度下反应达到平衡状态,若将平衡体系中各物质的浓度都增加到原来的2倍,下列叙述正确的是
A.化学平衡不发生移动
B.化学平衡向正反应方向移动
C.化学平衡向逆反应方向移动
D.正反应速率增大,逆反应速率减小