1������� ��15�֣���֪A��B��C��D���ֶ�����Ԫ�أ����ǵĺ˵������������Aԭ�ӡ�Cԭ�ӵ�L�ܲ��У���������δ�ɶԵĵ��ӣ�C��Dͬ���塣 E��F���ǵ�������Ԫ�أ�Eԭ�Ӻ�����4��δ�ɶԵ��ӣ�Fԭ�ӳ������ܲ�ֻ��1�������⣬������ܲ��Ϊȫ����������������Ϣ��գ�
�Ż�̬Dԭ���У�����ռ�ݵ�����ܲ����?�����ܲ���е�ԭ�ӹ����Ϊ?��
��E2�����ӵļ۲�����Ų�ͼ��?��Fԭ�ӵĵ����Ų�ʽ��?��
��AԪ�ص�����������Ӧ��ˮ��������ԭ�Ӳ�ȡ�Ĺ���ӻ���ʽΪ?��? BԪ�ص���̬�⻯���VSEPRģ��Ϊ?��
�Ȼ�����AC2��B2C��������DAB����Ϊ�ȵ����壬���ǽṹ���ƣ�DAB���ĵ���ʽΪ?��
����������ɫ��Ӧ����ɫ�����ڽ�����������E3������λ��AB�����ɣ���λ��Ϊ6����ˮ��Һ��������ʵ������E2�����ӵĶ��Լ��飬����E2�����ӵ����ӷ���ʽΪ?��
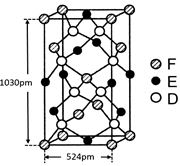
��ij�ֻ�������D��E��F����Ԫ����ɣ��侧����ͼ��ʾ�����仯ѧʽΪ?���þ������µ���Ϊ�����Σ���������洹ֱ������ͼ����ʾ��������ʽ����þ�����ܶȣ�
d=?g/cm3��
�ο��𰸣���M?9��?��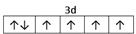 ? 1s22s22p63s23p63d104s1 (��[Ar]3d104s1) ��
? 1s22s22p63s23p63d104s1 (��[Ar]3d104s1) ��
�� sp2 �� ������ ����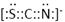 �� ��3Fe2��+2Fe(CN)63��=Fe3[Fe(CN)6]2�� ��
�� ��3Fe2��+2Fe(CN)63��=Fe3[Fe(CN)6]2�� ��
��CuFeS2?��?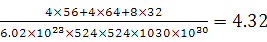
�����������������ɵ�A��C��B��N��C��O��D��S��E��Fe��F��Cu���Ż�̬Sԭ�Ӻ�������Ų���1s22s22p63s23p4���ɼ�����ռ�ݵ�����ܲ���M�㣻��M�ܲ���1��s�����3��p�����5��d�����һ�����е�ԭ�ӹ������9������Fe2�����ӵļ۲�����Ų�ͼ��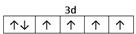 �������ܲ��Ų����ɿ�֪��29��Ԫ��Cuԭ�ӵĵ����Ų�ʽ��1s22s22p63s23p63d104s1 (��[Ar]3d104s1)����CԪ�ص�����������Ӧ��ˮ����H2CO3����ԭ��C��ȡ�Ĺ���ӻ���ʽΪsp2�ӻ���NԪ�ص���̬�⻯���VSEPRģ��Ϊ�������͡��Ȼ�����CO2��N2O��������SCN����Ϊ�ȵ����壬���ʵĽṹ���ơ�����Ҳ���ơ����ǽṹ���ƣ�SCN���ĵ���ʽΪ
�������ܲ��Ų����ɿ�֪��29��Ԫ��Cuԭ�ӵĵ����Ų�ʽ��1s22s22p63s23p63d104s1 (��[Ar]3d104s1)����CԪ�ص�����������Ӧ��ˮ����H2CO3����ԭ��C��ȡ�Ĺ���ӻ���ʽΪsp2�ӻ���NԪ�ص���̬�⻯���VSEPRģ��Ϊ�������͡��Ȼ�����CO2��N2O��������SCN����Ϊ�ȵ����壬���ʵĽṹ���ơ�����Ҳ���ơ����ǽṹ���ƣ�SCN���ĵ���ʽΪ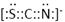 ������������ɫ��Ӧ����ɫ˵������K+�����ڽ�����������Fe3������λ��CN�����ɣ���λ��Ϊ6����������[Fe(CN)6] 3+�������Ļ�ѧʽ��K3[Fe(CN)6]. ����Fe2�����ӵļ��鷽�����������Һ�м���K3[Fe(CN)6].��Һ������������������ɫ�����軯��������,��֤������Fe2���������ӷ���ʽΪ3Fe2��+2Fe(CN)63��=Fe3[Fe(CN)6]2�� ����ij�ֻ�������D��E��F����Ԫ����ɣ����侧��ʾ��ͼ��֪������S��8; Fe��8��1/8+6��1/2=4��Cu:8��1/8+4��1/2+1=4������Fe:Cu:S=4:4:8=1:1:2���仯ѧʽΪCuFeS2?���þ������µ���Ϊ�����Σ���������洹ֱ������ͼ����ʾ��������ʽ����þ�����ܶȣ�
������������ɫ��Ӧ����ɫ˵������K+�����ڽ�����������Fe3������λ��CN�����ɣ���λ��Ϊ6����������[Fe(CN)6] 3+�������Ļ�ѧʽ��K3[Fe(CN)6]. ����Fe2�����ӵļ��鷽�����������Һ�м���K3[Fe(CN)6].��Һ������������������ɫ�����軯��������,��֤������Fe2���������ӷ���ʽΪ3Fe2��+2Fe(CN)63��=Fe3[Fe(CN)6]2�� ����ij�ֻ�������D��E��F����Ԫ����ɣ����侧��ʾ��ͼ��֪������S��8; Fe��8��1/8+6��1/2=4��Cu:8��1/8+4��1/2+1=4������Fe:Cu:S=4:4:8=1:1:2���仯ѧʽΪCuFeS2?���þ������µ���Ϊ�����Σ���������洹ֱ������ͼ����ʾ��������ʽ����þ�����ܶȣ�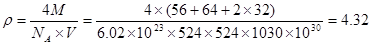 g/cm3��
g/cm3��
�����Ѷȣ�һ��
2������� ��֪A��BΪ������Ԫ�أ���ԭ�ӵĵ�һ�����ĵ��������±���ʾ��
������(kJ/mol)
| I1
| I2
| I3
| I4
|
A
| 932
| 1821
| 15390
| 21771
|
B
| 738
| 1451
| 7733
| 10540
|

(1)ijͬѧ����������Ϣ���ƶ�B�ĺ�������Ų���ͼ��ʾ����ͬѧ�����ĵ����Ų�ͼΥ����?��
��2��ACl2������A���ӻ�����Ϊ?��
��3��������Ϊһ�������Դ�����������Ĵ������⣬C60������������ϡ���֪���ʯ�е�C��C�ļ���Ϊ154.45pm��C60��C��C����Ϊ145-140pm����ͬѧ�ݴ���ΪC60���۵���ڽ��ʯ������Ϊ�˹۵��Ƿ���ȷ?�����ȷ������ȷ�����������������жϵ����ɣ�?��
��4����ѧ�Ұ�C60�ͼز�����һ��������һ�ָ���ϩ������侧����ͼ��ʾ���������ڵ���ʱ��һ�ֳ����塣д����̬��ԭ�ӵļ۵����Ų�ʽ?����������Kԭ�Ӻ�C60���ӵĸ�����Ϊ?��

��5��C��Si��Nԭ�ӵ縺���ɴ�С��˳����?��NCl3���ӵ�VSEPRģ��Ϊ?��
�ο��𰸣���ÿ��2�֣�(1)�������ԭ��?��2��? sp�ӻ�?
��3��?��? C60Ϊ���Ӿ��壬�ۻ�ʱ�ƻ����Ƿ��Ӽ��������������ƻ����ۼ�?
��4��? 4s1��? 3�U1?��5��N>C>Si����������
�����������1������A��B�ĵ��������ݿ�֪�����ǵ���������Զ���ڵڶ������ܣ����Զ��ǵڢ�A��Ԫ�ء�ͬ�������϶��£�����������ǿ����һ��������С������A��Be��B��Mg������B�ĺ�������Ų���ͼ��ʾ����ͬѧ�����ĵ����Ų�ͼΥ���������ԭ����
��2��BeCl2��ֱ���ͽṹ����˷�����Be���ӻ�����Ϊsp�ӻ���
��3��C60Ϊ���Ӿ��壬�ۻ�ʱ�ƻ����Ƿ��Ӽ��������������ƻ����ۼ��������ʯ��ԭ�Ӿ��壬�ۻ�ʱ�ƻ����ǹ��ۼ���
��4�����ݹ���ԭ����֪����̬��ԭ�ӵļ۵����Ų�ʽΪ4s1�����ݾ����ṹ��֪��������Kԭ�Ӻ�C60���ӵĸ����ֱ���12��1/4��3��8��1/8��1�������֮��Ϊ3�U1��
��5���ǽ�����Խǿ���縺��Խ����C��Si��Nԭ�ӵ縺���ɴ�С��˳����N>C>Si��NCl3�����е�ԭ�Ӻ��еŶԵ��Ӷ����ǣ�5��3��1����2��1������VSEPRģ��Ϊ�������壬��ʵ�ʿռ乹���������Ρ�
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣�����ۺ���ǿ�������߿���������ע�ضԻ���֪ʶ���̺�ѵ����ͬʱ�������ض�ѧ�������������ͽ��ⷽ����ָ����ѵ��������������ѧ�������������Ϳռ���������������ѧ��������û���֪ʶ���ʵ�����������������ѧ����ѧ��������
�����Ѷȣ�һ��
3��ѡ���� X��Y��Z��M��WΪ���ֶ�����Ԫ�ء�X��Y��Z��ԭ���������ε�����ͬ����Ԫ�أ�������������֮��Ϊ15��X��Z���γ�XZ2���ӣ�Y��M�γɵ���̬�������ڱ�״̬�µ��ܶ�Ϊ0.76g ? L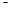 1��W����������X��Y��Z��M����Ԫ��������֮�͵�1/2 ������˵����ȷ����(? )
1��W����������X��Y��Z��M����Ԫ��������֮�͵�1/2 ������˵����ȷ����(? )
A��ԭ�Ӱ뾶��W>Z>Y>X>M
B��XZ2��X2M2��W2Z2��Ϊ���ۻ�����
C����XԪ���γɵĵ��ʲ�һ����ԭ�Ӿ���
D����Y��Z��M����Ԫ���γɵĻ�����һ��ֻ�й��ۼ�
�ο��𰸣�C
��������������⣺Y��M�γɵ���̬�������ڱ�״̬�µ��ܶ�Ϊ0.76g ? L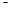 1����û������Ħ������M=Vm�ѣ�M��17g/mol,�������ȷ��MΪH,��YΪN, ����X��Y��Z��ԭ���������ε�����ͬ����Ԫ�أ�������������֮��Ϊ15��ȷ��XΪC��YΪO,��WΪNa���Ӷ�ȷ����ΪC��
1����û������Ħ������M=Vm�ѣ�M��17g/mol,�������ȷ��MΪH,��YΪN, ����X��Y��Z��ԭ���������ε�����ͬ����Ԫ�أ�������������֮��Ϊ15��ȷ��XΪC��YΪO,��WΪNa���Ӷ�ȷ����ΪC��
�����Ѷȣ�һ��
4��ѡ���� ϡ���ǹ�ҵζ������Сƽ˵�����ж���ʯ�ͣ�������ϡ������ϡ��Ԫ���棨Ce����Ҫ�����ڶ���ʯ�У��������ڿ������������䰵������ʱȼ�գ���ˮ�ܿ췴Ӧ����֪���泣���Ļ��ϼ�Ϊ+3��+4�������ԣ�Ce4+>Fe3+������˵����ȷ���ǣ�?��
A����֪Ceԭ��������58,����Ϊ��ϵԪ��
B�����������ȶ��ĺ���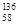 Ce��
Ce�� Ce��
Ce��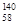 Ce��
Ce��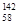 Ce�����ǻ�Ϊͬλ��
Ce�����ǻ�Ϊͬλ��
C����Ce��SO4��2��Һ��������������Һ��Ӧ�������ӷ���ʽΪ��Ce4++2Fe2+=Ce3++2Fe3+
D�������������Ļ�ѧ����ʽ�ɱ�ʾΪ��Ce+4HI=CeI4+2H2��
�ο��𰸣�AB
���������A.��ϵԪ���ǵ�57��Ԫ���絽71��Ԫ����15��Ԫ�ص�ͳ�ƣ�B.��������ͬ����������ͬ��һ��ԭ�ӻ���Ϊ��ϵԪ�أ�C.��ɲ��غ㣻D.�ɿ�Fe3+����I-��֪��Ce4+Ҳ������I-����CeI4�����ڣ�ӦΪCeI3.
�����Ѷȣ�һ��
5��ѡ���� ���ֶ�����Ԫ�ص�ԭ�Ӱ뾶����Ҫ���ϼۼ��±���
Ԫ�ط���
| X
| Y
| Z
| R
| T
|
ԭ�Ӱ뾶(nm)
| 0.130
| 0.090
| 0.102
| 0.118
| 0.073
|
��Ҫ���ϼ�
| ��2
| ��2
| ��2����4����6
| ��3
| ��2
|
?
���ݱ�����Ϣ���ж�����˵����ȷ����
A��������ϡ���ᷴӦ�����ʿ�����R��Y��X
B�����Ӱ뾶��T2����X2��
C��Ԫ������������Ӧˮ����ļ��ԣ�Y��R��X
D���������������ϵ����׳̶ȣ�Z��T
�ο��𰸣�B
���������X��Y����Ҫ���ϼ��ǣ�2�ۣ����ڵڢ�A�塣ͬ�������϶���ԭ�Ӱ뾶���������X��Mg��Y��Be��Z��T���У�2�ۣ�����λ�ڵڢ�A�塣����Z��SԪ�أ�T��OԪ�ء�R����Ҫ���ϼ��ǣ�3�ۣ�ԭ�Ӱ뾶����Mg��S֮�䣬���R��AlԪ�ء�A��������þǿ��Be��Al�����þ��ϡ����ķ�Ӧ������죬A����ȷ��B����������Ų���ͬ�����������뾶��ԭ���������������С��������Ӱ뾶��T2����X2����B��ȷ��C��������Խǿ����������Ӧˮ����ļ���Խǿ��������þǿ��Be��Al������������þ�ļ�����ǿ��C����ȷ��D���ǽ�����Խǿ��Խ�������������ϣ��⻯����ȶ���Խǿ���ǽ�������O��S�����Ե������������ϵ����׳̶ȣ�Z��T��D����ȷ����ѡB��
�����Ѷȣ�һ��