| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点讲解《电解质和非电解质》高频试题巩固(2019年最新版)(六)
参考答案:A 本题解析:电解质是指溶于水溶液中或在熔融状态下就能够导电(电解离成阳离子与阴离子)的化合物。氨气的水溶液能导电,电离出阴阳离子的是一水合氨不是氨气,所以氨气是非电解质不是电解质,蔗糖是以分子的形式分散在水中形成的溶液不能导电,也不属于电解质;浓硫酸是溶液,属于混合物,也不属于电解质 本题难度:一般 2、选择题 下列对化学知识的认识正确的是 |
参考答案:B
本题解析:A、H2与T2为分子,质子数相同,中子数不同的原子互为同位素,故A错误;B、氯化铵、氯化银能完全电离,都属于强电解质,故B正确;C、某些离子化合物可能含有离子键,如NaOH、Na2SO4等,故C错误;D、CO不是酸性氧化物,故D错误。
考点:本题考查化学基本概念。
本题难度:一般
3、选择题 电解质和非电解质是对化合物的一种分类方式。下列关于电解质的说法正确的是:
A.液态HCl不导电,所以HCl不是电解质
B.NH3溶于水形成的溶液能导电,所以NH3是电解质
C.SO2溶于水能导电,所以SO2是电解质
D.BaSO4在水溶液中难导电,但熔融状态下能导电,所以BaSO4是电解质
参考答案:D
本题解析:A、HCl溶于水后所得溶液能导电,属于HCl是电解质,错误;B、NH3溶于水时,发生反应:NH3+H2O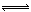 NH3?H2O,NH3?H2O发生电离使溶液导电,NH3本身不发生电离,错误;C、SO2溶于水时,发生反应:SO2 +H2O
NH3?H2O,NH3?H2O发生电离使溶液导电,NH3本身不发生电离,错误;C、SO2溶于水时,发生反应:SO2 +H2O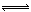 H2SO3,H2SO3发生电离使溶液导电,SO2本身不发生电离,错误;D、BaSO4不溶于水,BaSO4在水溶液中难导电,但熔融状态下能导电,所以BaSO4是电解质,正确。
H2SO3,H2SO3发生电离使溶液导电,SO2本身不发生电离,错误;D、BaSO4不溶于水,BaSO4在水溶液中难导电,但熔融状态下能导电,所以BaSO4是电解质,正确。
考点:本题考查电解质。
本题难度:一般
4、选择题 下列电离方程式中,正确的是
A.H2SO4=H2++SO42-
B.Ba(OH)2=Ba2++OH-
C.NaNO3=Na++NO3-
D.KMnO4=K++Mn2++4O2-
参考答案:C
本题解析:A.离子写错,应该是H2SO4=H++SO42-,错误; B.电荷不守恒,应该是Ba(OH)2=Ba2++2OH-;C.NaNO3=Na++NO3-符合电离的要求,正确;D.KMnO4是离子化合物,阳离子是K+,阴离子是MnO4-,KMnO4=K++ MnO4-,错误。
考点:考查电离方程式书写的正误判断的知识。
本题难度:简单
5、填空题 ⑴下列物质:①熔融氯化钠 ②盐酸 ③纯醋酸(CH3COOH) ④碳酸钙 ⑤酒精 ⑥二氧化碳 ⑦硫酸氢钠固体 ⑧铜 ⑨碳酸氢钠固体⑩氢氧化钡溶液,属于电解质的是 , 属于非电解质的是 ,能导电的是 。(用序号填空)
⑵写出物质③和⑨在水中反应的离子方程式: 。
⑶将物质⑦配制成溶液,逐滴滴入⑩中至Ba2+恰好沉淀完全,写出离子方程式: 。
参考答案:⑴①③④⑦⑨,⑤⑥,①②⑧⑩
⑵HCO3?+CH3COOH=H2O+CO2↑+CH3COO?
⑶H++SO42?+Ba2++OH?= BaSO4↓+ H2O
本题解析:⑴电解质是在水溶液或熔融状态下能导电的化合物,非电解质是在水溶液和熔融状态下都不能导电的化合物。根据定义可以作答。
⑵③纯醋酸(CH3COOH)不能拆成离子形式,⑨碳酸氢钠固体溶于水电离出HCO3?和Na+
⑶⑦NaHSO4= Na++ H++SO42?,Ba(OH)2=Ba2++2OH?;NaHSO4与Ba(OH)2反应,实质是H+与OH?,Ba2+与SO42?的反应。
考点:物质的分类和离子方程式的书写。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点整理《物质的组成.. | |